Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Số hạt mang điện nhiều hơn số hạt không mang điện của X là 14 → 2pX -nX = 14
Số hạt mang điện nhiều hơn số hạt không mang điện của Y là 16 → 2pY -nY = 16
Tổng số proton là 100 → pX + n.pY=100
Tổng số notron là 106→ nX + n. nY = 106
→ (2pX + 2n.pY) - (nX + n. nY ) = 200-106 = 84
→ (2pX -nX) - (2n.pY- n. nY) = 84 → 14 + 16n = 84 → n = 5

→ AX = 0,1504856. (100+106) = 31 ( P)
Số khối của của Y là 206 - 31 5 = 35

Vì hợp chất với hidro có dạng RH => X hoặc Y thuộc nhóm IA hoặc VIIA
*TH1: Y thuộc nhóm IA => CT hidroxit : YOH
theo đề ta có: Y/(Y+17)=0.35323
=>Y=9.28 (loại)
*TH2: Y thuộc nhóm VIIA=> CT hidroxit: HYO4
theo đề ta có: Y/(1+Y+16.4)=0.35323
=> Y=35.5 Cl
theo đề ta thấy: trung hòa A cần dùng dung dịch B. Mà B là axit => A là bazo
=> X thuộc nhóm IA => CTHH: XOH
PT: XOH + HClO4 -> XClO4 +H2O
0.15 0.15 (MOL)
m(XOH)=(50.16,8)/100=8,4=>M(XOH)=m/n=56=>X=39 (Kali)
Hợp chất với hiđro có dạng RH nên Y có thể thuộc nhóm IA hoặc VIIA.
Trường hợp 1 : Nếu Y thuộc nhóm IA thì B có dạng YOH
Ta có : \(\frac{Y}{17}=\frac{35,323}{64,677}\Rightarrow\)\(Y=9,284\) (loại do không có nghiệm thích hợp)
Trường hợp 2 : Y thuộc nhóm VIIA thì B có dạng HYO4
Ta có : \(\frac{Y}{65}=\frac{35,323}{64,377}\Rightarrow Y=35,5\), vậy Y là nguyên tố clo (Cl).
B (HClO4) là một axit, nên A là một bazơ dạng XOH
\(m_A=\frac{16,8}{100}.50g=8,4g\)
XOH + HClO4 \(\rightarrow\) XClO4 + H2O
\(\Rightarrow n_A=n_{HClO_4}=0,15L.0,1\text{/}L=0,15mol\)
\(\Rightarrow M_X+17g\text{/}mol=\frac{0,84g}{0,15mol}\)
\(\Rightarrow\) MX = 39 gam/mol, vậy X là nguyên tố kali (K).

Đáp án B
Trong nguyên tử X và Y có số hạt mang điện nhiều hơn hạt không mang điện lần lượt là 14 và 16
→ 2ZX - NX = 14 (1) và 2ZY - NY = 16
Tổng số proton là 100 → ZX + nZY = 100
Tổng số nơtron là 106 → NX +n NY = 106
→ 2ZX- 14 + n. [2ZY - 16] = 106 → 2. [ZX + nZY] -14 - 16n = 106
→ 2. 100-14 - 16n = 106 → n = 5
Có X chiếm 15,0486% về khối lượng

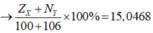
![]()
Giải hệ (1) và (2) → ZX = 15 và NX = 16 → X là P
Vậy công thức của hợp chất là PCl5.

Trong nguyên tử X và Y có số hạt mang điện nhiều hơn hạt không mang điện lần lượt là 14 và 16
→ 2ZX - NX = 14 (1) và 2ZY - NY = 16
Tổng số proton là 100 → ZX + nZY = 100
Tổng số nơtron là 106 → NX +n NY = 106
→ 2ZX- 14 + n. [2ZY - 16] = 106 → 2. [ZX + nZY] -14 - 16n = 106
→ 2. 100-14 - 16n = 106 → n = 5
Có X chiếm 15,0486% về khối lượng →
M
x
M
x
y
5
x 100% = 15, 0468
→
Z
x
+
N
y
100
+
106
× 100% = 15, 0468 → ZX + NY = 31 (2)
Giải hệ (1) và (2) → ZX = 15 và NX = 16 → X là P
Vậy công thức của hợp chất là PCl5.
Đáp án B.

Hợp chất của R và hidro: RH
\(\Rightarrow a\%=\dfrac{M_R}{M_R+1}.100\%\)
Hợp chất oxit cao nhất của R: R2O7
\(\Rightarrow b\%=\dfrac{2M_R}{2M_R+112}.100\%\)
\(\Rightarrow\dfrac{M_R}{M_R+1}+\dfrac{2M_R}{2M_R+112}=\dfrac{18176}{13359}\)
\(\Rightarrow M_R=35,5\left(g/mol\right)\)
→ R là Cl.

X tạo bởi chất ion với clo có công thức là XC1, vậy X là kim loại có hoá trị I.
Y cùng số nhóm với X vậy cũng có hoá trị I, công thức clorua của nó là YC1.
Ta có:
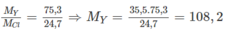
( M Y và M Cl lần lượt là NTK của nguyên tố Y và nguyên tố clo). Đó là Ag. Nguyên tố X cùng chu kì, cùng số thứ tự nhóm với Ag là kali (K))