Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Giả sử có 100 gam dung dịch HCl 32,85% thì khối lượng HCl là 32,85 gam.
nHCl= 32 , 85 36 , 5 = 0,90 mol
- Gọi số mol của CaCO3 là x (mol). Phản ứng:
CaCO3 + 2HCl → CaCl2 + H2O + CO2 (1)
x 2x x x
Từ (1) và đề ra: nHCldư = (0,90 - 2x) mol
Khối lượng dung dịch X sau phản ứng (1): 100 + 100x – 44x = (100 + 56x) gam
Theo đề ra: C%HCl = ( 0 , 90 - 2 x ) . 36 , 5 100 + 56 x . 100 % = 24,195% => x = 0,1 mol
Vậy sau p/ư (1) nHCl còn lại = 0,7mol
- Cho MgCO3 vào dung dịch X, có p/ư:
MgCO3 + 2HCl → MgCl2 + H2O + CO2 (2)
y 2y y y
Sau p/ư (2) nHCl dư = 0,7-2y
Khối lượng dung dịch Y là: (105,6 + 84y - 44y) gam hay (105,6 + 40y) gam
Từ (2) và đề ra: C%HCl trong Y = ( 0 , 7 - 2 y ) . 36 , 5 105 , 6 + 40 y . 100% = 21,11% => y = 0,04 mol
Dung dịch Y chứa 2 muối CaCl2, MgCl2 và HCl dư:
C%(CaCl2) = 0 , 1 . 111 107 , 2 . 100 % = 10 , 35 %
C%(MgCl2) = 0 , 04 . 95 107 , 2 . 100 % = 3 , 54 %

Đáp án A
Khi thêm lượng dư HCl vào Y thấy có khí thoát ra
=> Trong Y có (NH4)2CO3 => X là HCHO
⇒ n H C H O = 1 3 n A g = 1 ( m o l ) ⇒ m H C H O = 30 ( g ) ⇒ a % = 30 150 = 20

a)
$n_{CaCO_3} = 0,12(mol) ; n_{HCl} = 0,6(mol)
\(CaCO_3+2HCl\text{→}CaCl_2+CO_2+H_2O\)
Ban đầu 0,12 0,6 (mol)
Phản ứng 0,12 0,24 (mol)
Sau pư 0 0,36 0,12 (mol)
$V = 0,12.22,4 = 2,688(lít)$
b)
$n_{Cl^-} = 0,6(mol) ; n_{H^+} = 0,36(mol)$
$n_{Ca^{2+}} = 0,12(mol)$
$[Cl^-] = \dfrac{0,6}{0,2} = 3M$
$[H^+] = \dfrac{0,36}{0,2} = 1,8M$
$[Ca^{2+}] = \dfrac{0,12}{0,2} = 0,6M$
a,\(n_{CaCO_3}=\dfrac{12}{100}=0,12\left(mol\right);n_{HCl}=0,2.3=0,6\left(mol\right)\)
PTHH: CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Mol: 0,12 0,12
Ta có: \(\dfrac{0,12}{1}< \dfrac{0,6}{2}\)⇒ HCl dư,CaCO3 pứ hết
\(V_{CO_2}=0,12.22,4=2,688\left(l\right)\)

Phản ứng đầu không có kết tủa bị hòa tan, phản ứng sau có kết tủa bị hòa tan (nếu cả 2 phản ứng đều có kết tủa bị hòa tan thì số mol NaOH chênh lệch giữa 2 lần phải bằng số mol kết tủa chênh lệch của 2 lần)
Lần 2:
n A l ( O H ) 3 = 0 , 06 ⇒ n A l ( O H ) = 0 , 34 - 0 , 06 . 3 4 = 0 , 04 ⇒ n A l C l 3 = 0 , 06 + 0 , 04 = 0 , 1 ⇒ x = 1
Đáp án B

Đáp án D
Hướng dẫn Ta có : nHCHO = nAg / 4 => nHCHO = 1 mol => C%dung dịch fomalin = 1.30 / 75 .100% = 40%

Dung dịch vẫn còn màu xanh nghĩa là Cu2+ chưa bị điện phân hết.

Đáp án D


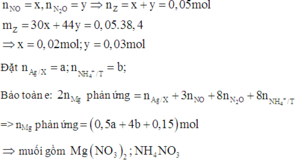
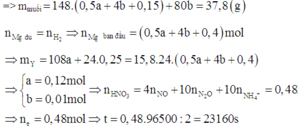
Đáp án B
Chọn 1 mol HCl ban đầu. Gọi n C a C O 3 = x
Có phản ứng: C a C O 3 + 2 H C l → C a C l 2 + C O 2 + H 2 O (1)
Do đó nồng độ phần trăm của HCl sau phản ứng (1) là:
Do đó sau phản ứng (1) dung dịch X có mx = 117,47; nHCl dư = 0,7728
Gọi n M g C O 3 = y . Có phản ứng:
Do trong quá trình tính toán, ta có nhiều bước làm tròn nên dẫn đến sai số.
Khi đó ta sẽ chọn đáp án gần với kết quả tính được nhất.