Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Hỗn hợp hơi gồm CnH2nO và H2O
=> nCnH2nO = nH2O= nO = 0,02
=>M = (18n+16 + 18)/2 = 15,5.2 => n = 2
=>X là C2H5OH (0,02 mol)
=> mX = 0,92

m giảm chính là kl oxi
=>nO=n(andehit)=nH2O=0,02 mol
=>n(sản phẩm )=0,04 mol =>msau=0,04.2.15,5=1,24 gam
=> m t=ms-mgiảm=1,24-0,32=0,92 gam
khối lượng rắn giàm là khối lượng của oxi tham gia p/ư oxi hóa ancol
n O = 0,32: 16 = 0,02 .
Giả sử ancol bậc 1 để viết p/ư minh họa
R-CH2OH + CuO ---> RCHO + H2O + Cu
R-CH2OH + O ---> RCHO + H2O
0.02 0,02 0,02 0,02
M hh hơi = 15,5.2 = 31 ; n hh hơi = 0,04 => m hh hơi = 0,04. 31 = 1,24 gam.
Bảo toàn khối lượng để tính m ancol = m hh hơi - m O
m = 1,24 - 0,32 = 0,92 gam

A(Fe, S) ==nung==> B(Fe, S, FeS) ==HCl==> C(H2, H2S)
B(Fe, S, FeS) ==nung==> (Fe2O3, SO2)
Bằng phương pháp sơ đồ đường chéo bạn dễ dàng tính được tỉ lệ nH2/nH2S = 1/3
Mà nH2 + nH2S = V
=> nH2 = 0,25V và nH2S = 0,75V
Sau khi viết tất cả các phương trình phản ứng, bạn dễ dàng tính được những kết quả sau :
nFe (trong B) = nH2 = 0,25V mol => mFe = 14V g
nFeS (trong B) = nH2S = 0,75V mol => mFeS = 66V g
Phản ứng của B với O2 :
4FeS + 7O2 = 2Fe2O3 + 4SO2
0,75V....1,3125V mol
S + O2 = SO2
x.....x
Ta có 1,3125V + x = V'' => nS = x = V'' - 1,3125V
=> mS = 32V'' - 42V
mB = mFe + mS + mFeS = 14V + 32V'' - 42V + 66V = 38V + 32V'' g
b. nS = V'' - 1,3125V => V'' > 1,3125V => V''/V > 1,3125

n CO2= 0,4 => n 0/oxit = 0,4
n fe= n H2= 0,2
=> m fe203 = 0,1 => n CuO= 0,1
=> m =

\(n_{Fe\left(NO_3\right)_3}=0,14mol\)
Đặt \(n_{Fe}=n_{FeO}=n_{Fe_2O_3}=n_{Fe_3O_4}=x\)
\(Fe\rightarrow Fe^{3+}\)
x x
\(FeO\rightarrow Fe^{3+}\)
x x
\(Fe_2O_3\rightarrow2Fe^{3+}\)
x 2x
\(Fe_3O_4\rightarrow3Fe^{3+}\)
x 3x
\(\Rightarrow7x=0,14\Rightarrow x=0,02\Rightarrow m=10,4g\)
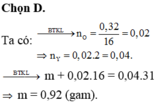
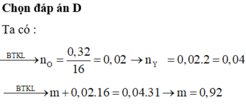
Đáp án D
Hỗn hợp hơi gồm CnH2nO và H2O
=> nCnH2nO = nH2O = nO = 0,02
=>M = (18n+16 + 18)/2 = 15,5.2 => n = 2
=>X là C2H5OH (0,02 mol)
=> mX = 0,92