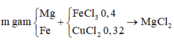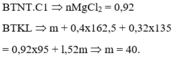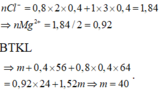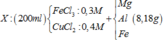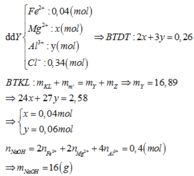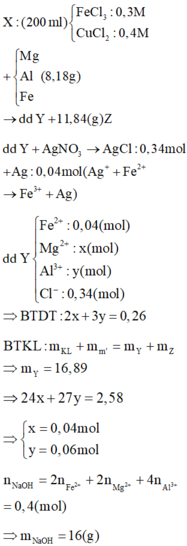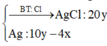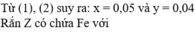Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Số mol các chất và ion trong dung dịch muối ban đầu là:


Dung dịch X gồm ![]()
Chất rắn Y gồm 2 kim loại là Cu và Fe.
Dung dịch X tác dụng với dung dịch AgNO3 dư;
Phản ứng tạo kết tủa: 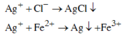
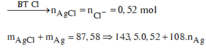
![]()
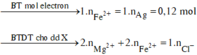
![]()
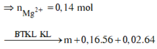
![]()
![]()
Đáp án C

Đáp án D
Ta có: n FeCl 3 = 0 , 16 ; n CuCl 2 = 0 , 12
Cho AgNO3 dư vào X thu được kết tủa gồm AgCl 0,72 mol (bảo toàn nguyên tố Cl) và Ag 0,06 mol.
Nếu cho NaOH dư vào X thì lượng NaOH phản ứng 0,78 mol, do vậy
n Al = 0 , 78 - 0 , 72 = 0 , 06 mol
Do n Ag = 0 , 06 → n Fe + 2 trong X = 0 , 06 mol
Ta có: n Fe 2 + < n FeCl 3 và khối lượng rắn tăng do vậy Fe dư
Gọi số mol Mg là a mol, Fe là b mol
→ m = 24a+56b+0,06.27
Rắn Y sẽ chứa Cu 0,12 mol và Fe 0,1+b mol
→ 1,8275m = 0,12.64+56(0,1+b)
Dung dịch X chứa MgCl2 a mol, AlCl3 0,06 mol và FeCl2 0,06 mol
→ a = 0 , 72 - 0 , 06 . 3 - 0 , 06 . 2 2 = 0,21 mol → b = 67 2800
→ m = 8 gam

Đáp án D
Quan sát quá trình 1:

BTKL có nH2O = 0,92 mol. Bảo toàn H chứng
tỏ trong X chứa 0,26 mol H+ dư như trên.
♦ Quá trình 2: để ý khí Y có M = 18,8
→ là H2 và NO. Quan sát quá trình chính:
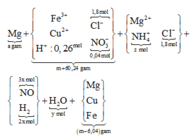
giải tỉ khối Y tìm tỉ lệ 2 khí NO : H2 là 3 : 2 rồi gọi các ẩn như sơ đồ:
• Ghép cụm: nH2O = 2nNO + 3nNH4 ⇄ y = 6x + 3z (1).
• bảo toàn nguyên tố N có: 3x + z = 0,04 mol (2).
• Bảo toàn nguyên tố H có: 4x + 2y + 4z = 0,26 mol (3)
Giải x = 0,01 mol; y = 0,09 mol; z = 0,01 mol ||→ bảo toàn điện tích có nMg2+ = 0,895 mol.
► Chỉ cần BTKL cả sơ đồ có ngay và luôn giá trị yêu cầu a = 21,84 gam