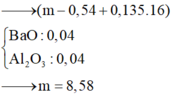Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

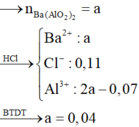
Gọi x, y lần lượt là số mol Ba, BaO
Hòa vào nước tạo 2.(x+y) mol OH-
Al còn dư suy ra số mol Al phản ứng bằng số mol OH- bằng 2(x+y)nH2 = nBa + 1,5nAl = x + 1,5.2.(x+y) = 0,135 (1)
nHCl = 0,11
ta có công thức:3nKt + nH+ = 4nAlO2-
=> nAlO2- = 0,08 = n Al phản ứng = 2(x+y) (2) Từ (1,2) => x=0,015=Ba; y=0,025=BaO
Al phản ứng=0,08
m = Ba + BaO + Al pư + Al dư = 8,58g => Đap an C

nAl dư = 0,54/27=0,02
Al(OH)4- + H+ -> Al(OH)3+H2O
x x x
Al(OH)3+3H+ -> Al3+ + 3H2O
0,11-x
Đặt nAl(OH)4- = x
Ta có : x-(0,11-x)/3=0,07 => x=0,08 => nAl pư = 0,08
nH2 = nBa+3/2nAl => nBa = 0,015
=> nBaO=(nAl-2nBa)/2=0,025
=>m=0,1.27+0,015.137+0,025.153=8,58g
=>C

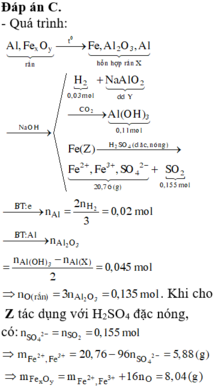
Mol \(Fe\) = 0,11 mol
Mol hh khí= 0,1 mol
BT klg\(\Rightarrow\)m hh khí=12,09-6,16=5,93g
Gọi mol \(Cl_2\) và mol \(O_2\) lần lượt là x và y
\(\Rightarrow\) x+y=0,1 và 71x+32y=5,93
\(\Rightarrow\)x=0,07 và y=0,03
Mol \(Cl-\) trong muối= 0,07.2=0,14 mol = mol \(AgCl\)
\(Fe\) có thể lên \(Fe+2\) và \(Fe+3\) nên
\(Fe\Rightarrow Fe^{+2}+2e\)
a mol. \(\Rightarrow\)2a mol
\(Fe\Rightarrow Fe^{+3}+3e\)
b mol \(\Rightarrow\)3b mol
\(Cl_2+2e\Rightarrow2Cl-\)
0,07 \(\Rightarrow\)0,14 mol
\(O_2+4e\Rightarrow2O_2-\)
0,03\(\Rightarrow\)0,12 mol
Mol e nhường= nhận\(\Rightarrow\)2a+3b=0,26 mol và tổng mol \(Fe\)là a+b=0,11 mol\(\Rightarrow\)a=0,07 và b=0,04
\(Fe^{2+}+Ag^+\Rightarrow Fe^{3+}+Ag\)
0,07 mol \(\Rightarrow\)0,07 mol
Số gam kết tủa = 0,07.108+0,14.143,5=27,65\(\Rightarrow\)chọn A
Đáp án b nhé :44,87...lưu ý khi tính ra số mol fe2+ = 0,07, mol fe3+=0,04 thì =>>> mol Cl- = 0,07x2 + 0,04x3= 0,26 mol.....==>> mol AgCl=0,26.......Để ý hòa tan bằng dd Hcl vừa đủ thì oxit phải chuyển thành hết muối clorua....ko đẻ ý điều này rất dễ nhầm đáp án là A...lừa đó ^^

n CO2= 0,4 => n 0/oxit = 0,4
n fe= n H2= 0,2
=> m fe203 = 0,1 => n CuO= 0,1
=> m =

Gọi số mol K và Al trong hỗn hợp x, y
2K + 2H2O → KOH + H2 (1)
x x (mol)
2Al + 2KOH + 2H2O → 2KAlO2 + 3H2↑ (2)
y y (mol)
Do x tan hết nên Al hết, KOH dư sau (2). Khi thêm HCl, ban đầu chưa có kết tủa vì:
HCl + KOH → KCl + H2O (3)
X – y x – y (mol)
Khi HCl trung hòa hết KOH dư thì bắt đầu có kết tủa:
KAlO2 + HCl + H2O → Al(OH)3 ↓ + KCl (4)
Vậy để trung hòa KOH dư cần 100 ml dung dịch HCl 1M.
Ta có: nHCl = nKOH dư sau phản ứng (2) = x – y = 0,1.1 = 0,1 (mol) (I)
Mặt khác: 39x + 27 y = 10,5 (II)
Từ (1) và (II) => x = 0,2; y = 0,1.
% nK = 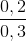 .100% = 66,67%;
.100% = 66,67%;
%nAl = 100% - 66,67% = 33,33%.
K + HOH --> KOH +1/2H2
Al + KOH + HOH --> KAlO2 +3/2H2
-Cho HCl vào bd kg có ket tua => KOH du
HCl + KOH --> KCl + HOH
-Sau đó có ket tua => KOH het => KAlO2 phan ung
KAlO2 + HCl + HOH --> Al(OH)3 + KCl
vì den 100ml dd HCl 1M co xuat hien ket tua nen => n(KAlO2) =n(HCl) = 0,1
=> n(Al) = 0,1
=> %Al = 25,71%
=> %K =74,29%
Luu y: hoi hóa xem bai giai co dung hay co van de nao kg gop ý dum nha thanks

Mg + HCl - MgCl2 + H2
Al + HCl - AlCl3 + H2
còn Cu đứng sau H nên không phản ứng với HCl.
nCuO = \(\dfrac{16}{80}=0,2\) mol
Pt: 2Cu + O2 --to--> 2CuO
0,2 mol<--------------0,2 mol
.....Mg + 2HCl --> MgCl2 + H2
0,2 mol<-----------0,2 mol
.....2Al + 6HCl --> 2AlCl3 + 3H2
....MgCl2 + 2NaOH --> Mg(OH)2 + 2NaCl
...0,2 mol<---------------0,2 mol
....AlCl3 + 3NaOH --> Al(OH)3 + 3NaCl
....Al(OH)3 + NaOH --> NaAlO2 + 2H2O
..........................................(tan)
...Mg(OH)2 --to--> MgO + H2O
0,2 mol<------------ 0,2 mol
nMgO = \(\dfrac{8}{40}=0,2\) mol
mCu = 0,2 . 64 = 12,8 (g)
mMg = 0,2 . 24 = 4,8 (g)
mAl = mhh - mCu - mMg = 20 - 12,8 - 4,8 = 2,4 (g)
% mCu = \(\dfrac{12,8}{20}.100\%=64\%\)
% mMg = \(\dfrac{4,8}{20}.100\%=24\%\)
% mAl = \(\dfrac{2,4}{20}.100\%=12\%\)