Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Đặt a, b, c lần lượt là số mol CH4, C2H4, C2H2 (trong 8,6 gam X)
Ta có: 16a + 28b + 26c = 8,6 (1)
b + 2c = 0,3 (2)
Mặt khác: Gọi số mol của CH4, C2H4, C2H2 trong 13,44 lít hỗn hợp X lần lượt là kx, ky, kz
![]() (3)
(3)
![]()
kc kc
Ta có
nkết tủa ![]() (4)
(4)
Lấy (3) chia (4) được
![]() (5)
(5)
Từ (1), (2) và (5) được

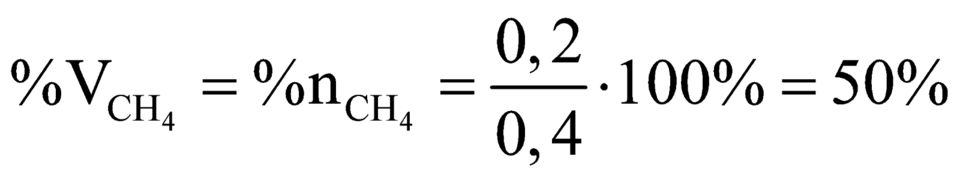

Đáp án C
Gọi số mol CH4, C2H4, C2H2 lần lượt là a, b, c
=> 16a + 28b + 26c = 8,6
Cho 8,6 gam X tác dụng vừa đủ với 0,3 mol Br2 => b + 2c = 0,3
Mặt khác 0,6 mol X tác dụng với AgNO3/NH3 thu được 36 gam kết tủa AgC≡CAg
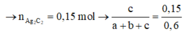
Giải hệ: a=0,2; b=0,1;c=0,1 nên %V CH4 =50%.

Đáp án C
Gọi số mol CH4, C2H4, C2H2 lần lượt là a, b, c => 16a + 28b + 26c = 8,6
Cho 8,6 gam X tác dụng vừa đủ với 0,3 mol Br2 => b + 2c = 0,3
Mặt khác 0,6 mol X tác dụng với AgNO3/NH3 thu được 36 gam kết tủa AgC≡CAg
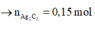
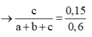
Giải hệ: a=0,2; b=0,1;c=0,1 nên %V CH4 =50%.

\(5gX\left\{{}\begin{matrix}CH_4:a\left(mol\right)\\C_2H_4:b\left(mol\right)\\C_2H_2:c\left(mol\right)\end{matrix}\right.\)
Cho X tác dụng với dung dịch \(AgNO_3\)/\(NH_3\) chỉ có \(C_2H_2\) phản ứng.
\(n_{\downarrow}=n_{C_2Ag_2}=\dfrac{24}{240}=0,1mol\)
\(C_2H_2+2AgNO_3+2NH_3\rightarrow C_2Ag_2\downarrow+2NH_4NO_3\)
0,1 0,1
\(\Rightarrow c=0,1mol\)
\(\Rightarrow16a+28b=5-0,1\cdot26=2,4\left(1\right)\)
Cho X tác dụng với brom:
\(n_{Br_2}=\dfrac{28}{160}=0,175mol\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
\(\Rightarrow b+2c=0,175\Rightarrow b=0,175-2\cdot0,1=-0,025\left(âm\right)???\)

Đáp án : D
Nhận thấy cứ 0,375 mol X làm mất màu 0,3375 mol Br2 → ![]() =
0
,
3375
0
,
375
= 0,9
=
0
,
3375
0
,
375
= 0,9
Goi số mol của CH4, C2H4 trong 26,8 gam lần lượt là x,y.
Ta có nC3H4 = n↓ = 0,2 mol
Ta có hệ ![]() →
→ ![]()
→ %CH4=
0
,
3
0
,
3
+
0
,
5
+
0
,
2
×100% = 30%

Đáp án A
Trong 13,4 gam A:![]()
Ta có: ![]()
![]()
16,8 lít(đktc) A(0,75 mol) tác dụng vừa đủ với 108 gam brom(0,675 mol)
(a+b+c) mol A tacd dụng vừa đủ với (b+2c) mol brom
Nhân chéo ta được: ![]()
![]()
Từ (1), (2) và (3) ![]()
Thể tích của CH4trong hỗn hợp là: ![]() %
%
Chọn A

nX= 13.44/22.4=0.6 mol
Gọi x,y,z lần lượt là số mol của CH4, C2H4 , C2H2
Ta có : 16x + 28y+ 26z=8.6 (1)
Cho X đi qua dd Brom thì chỉ có C2H4 và C2H2 pư
Suy ra : mBr2 pư = mC2H4 + mC2H2 = 48 g
=> nBr2 = y+2z = 48/160=0.3 mol (2)
Nếu cho X pư với AgNO3 trong môi trường NH3, chỉ có C2H2 pư, cho kết tủa vàng của bạc axetilua Ag2C2
nAg2C2= nC2H2 = z = 36/240= 0.15 mol
=> %C2H2 = \(\dfrac{0,15\cdot22,4}{13,44}\cdot100\) = 25%
Mà ta thấy trong 0.6 mol X có 0.15 mol C2H2 tức là gấp 4 lần => x+y+z=4z <=> x+y-3z=0 (3)
giải (1),(2),(3), ta được x = 0,2 ; y= 0.1; z= 0.1
=> %C2H4 = \(\dfrac{0,1\cdot22,4}{13,44}\cdot100\) = 25%
=>%CH4= 100- 25-25= 50%
Chức bạn học tốt !

a, PT: \(C_2H_2+AgNO_3+NH_3\rightarrow Ag_2C_{2\downarrow}+NH_4NO_3\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b, Ta có: \(V_{CH_4}=V_Y=0,56\left(mol\right)\Rightarrow\%V_{CH_4}=\dfrac{0,56}{6,72}.100\%\approx8,33\%\)
\(V_{C_2H_4}=V_X-V_{CH_4}=3,92\left(l\right)\Rightarrow\%V_{C_2H_4}=\dfrac{3,92}{6,72}.100\%\approx58,34\left(\%\right)\)
\(\Rightarrow V_{C_2H_2}=6,72-4,48=2,24\left(l\right)\Rightarrow\%V_{C_2H_2}=\dfrac{2,24}{6,72}.100\%\approx33,33\%\)
c, \(n_{Ag_2C_2}=n_{C_2H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow m_{Ag_2C_2}=0,1.240=24\left(g\right)\)
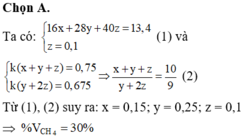
\(n_{hh_X}=0,2\left(mol\right)\)
Cho X tác dụng với AgNO3/NH3 chỉ có C2H2 td do các liên kết 3 đầu mạch còn 2 khí kia ko td
\(n_{kt}=n_{C2Ag2}=\frac{12}{12.2+108.2}=0,05\left(mol\right)\)
\(PTHH:C_2H_2+2AgNO_3+2NH_3\rightarrow C_2Ag_2+2NH_4NO_3\)
_________0,05___________________ 0,05______________
\(n_{Br2}=0,2\left(mol\right)\)
Khi cho tác dụng với Br2 thì C2H4 và C2H2 pứ
\(PTHH:C_2H_4+Br_2\rightarrow C_2H_4Br_2\) ( Do là anken nên chỉ td với 1 ph tử Br2)
__________0,1____0,1__________________
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\) (Ankin nên td với 2 ph tử Br2)
0,05____0,1____________________
Do C2H2 td với 0,1 mol Br2 nên số mol anken pứ với Br2=0,1 (0,2-0,1=0,1)
\(n_{hh_{ban.dau}}=n_{CH4}+n_{C2H4}+n_{C2H2}\)
\(0,2.=n_{CH4}+0,1+0,05\)
\(\Rightarrow n_{CH4}=0,05\left(mol\right)\)
\(\%V_{CH2}=\frac{0,05.22,4.100}{0,2.22,4}=25\%\)
\(\%V_{C2H4}=50\%\)
\(\%V_{C2H2}=25\%\)