Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Gọi M là kim loại chung cho Zn và Mg với hóa trị n
Sơ đồ phản ứng: M + H 2 SO 4 ( loãng , dư ) → M 2 ( SO 4 ) n ⏟ muối + H 2 ↑
Khí thu được là
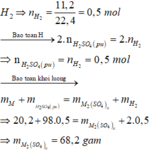

Quy đổi hỗn hợp gồm Al, Mg, Zn thành kim loại R (số oxi hóa +n)
Gọi số mol R là a (mol)
- Xét TN1:
\(n_{Cu}=\dfrac{3,2}{64}=0,05\left(mol\right)\)
- Xét TN2:
\(n_{Cl_2}=\dfrac{17,75}{71}=0,25\left(mol\right)\)
PTHH: Cu + Cl2 --to--> CuCl2
0,05->0,05
2R + nCl2 --to--> 2RCln
\(\dfrac{0,4}{n}\)<-0,2
=> \(n_R=\dfrac{0,4}{n}\left(mol\right)\)
- Xét TN1:
PTHH: 2R + 2nHCl --> 2RCln + nH2
\(\dfrac{0,4}{n}\)------------------->0,2
=> V = 0,2.22,4 = 4,48 (l)

nH2=4,48/22,4=0,2 mol
Fe +2HCl -->FeCl2+H2
0,2 0,2 mol
=>mFe=0,2*56=11,2 g
nSO2=10,08/22,4=0,45 mol
gọi số mol của Cu là a mol
bảo toàn e ta có
Cu\(^0\)-->Cu\(^{+2}\)+2e
a 2a S\(^{+6}\) + 2e -->S\(^{+4}\)
Fe\(^0\)--> Fe\(^{+3}\)+3e 0,45 0,9
0,2 0,6
=>a=0,15=>mCu=0,15*64=9,6 g
=>mhh=9,6+11,2=20,8g
=>%Cu=9,6*100/20,8=46,15%

Giả sử: \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Zn}=b\left(mol\right)\\n_{Cu}=c\left(mol\right)\\n_{Al}=d\left(mol\right)\end{matrix}\right.\)
_ Khi tác dụng với HCl.
Ta có: \(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
Theo ĐLBT mol e, có: 2a + 2b + 3d = 0,45.2 ⇒ 2a + 2b + 3d = 0,9 (1)
_ Khi tác dụng với H2SO4 đặc nóng.
Ta có: \(n_{SO_2}=\dfrac{10,64}{22,4}=0,475\left(mol\right)\)
Theo ĐLBT mol e, có: 2a + 2b + 2c + 3d = 0,475.2
⇒ 2a + 2b - 2c + 3d = 0,95 (2)
Trừ 2 vế của (1) và (2), có: c = 0,025 (mol)
\(\Rightarrow\%m_{Cu}=\dfrac{0,025.64}{14,7}.100\%\approx10,88\%\)
Bạn tham khảo nhé!
Đặt \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Zn}=b\left(mol\right)\\n_{Cu}=c\left(mol\right)\\n_{Al}=d\left(mol\right)\end{matrix}\right.\)
Ta có: \(\left\{{}\begin{matrix}n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\\n_{SO_2}=\dfrac{10,64}{22,4}=0,475\left(mol\right)\end{matrix}\right.\)
Bảo toàn electron: \(\left\{{}\begin{matrix}2a+2b+2c+3d=0,475\cdot2\\2a+2b+3d=0,45\cdot2\end{matrix}\right.\)
\(\Rightarrow2c=0,475\cdot2-0,45\cdot2=0,05\) \(\Rightarrow c=0,025\)
\(\Rightarrow\%m_{Cu}=\dfrac{0,025\cdot64}{14,7}\cdot100\%\approx10,88\%\)
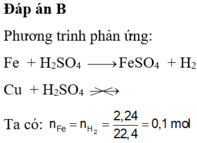


PTHH: Fe + H2SO4 ===> FeSO4 + H2
0,05........................................0,05
Mg + H2SO4 ===> MgSO4 + H2
0,1.............................................0,1
Zn + H2SO4 ===> ZnSO4 + H2
0,1...........................................0,1
nFe = 2,8 / 56 = 0,05 mol
nMg = 2,4 / 24 = 0,1 mol
nZn = 6,5 / 65 = 0,1 mol
Lập các số mol trên phương trình, ta có:
nH2 = 0,05 + 0,1 + 0,1 = 0,25 mol
=> VH2(đktc) = 0,25 x 22,4 = 5,6 lít
Nhưng còn HCl mà?