Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
a) PTHH: \(2A+2xHCl\rightarrow2ACl_x+xH_2\uparrow\)
\(2B+2yHCl\rightarrow2BCl_y+yH_2\uparrow\)
b) Ta có: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\) \(\Rightarrow m_{H_2}=0,4\cdot2=0,8\left(g\right)\)
Theo các PTHH: \(n_{HCl}=2n_{H_2}=0,8\left(mol\right)\) \(\Rightarrow m_{HCl}=0,8\cdot36,5=29,2\left(g\right)\)
Bảo toàn khối lượng: \(a=m_{KL}=m_{muối}+m_{H_2}-m_{HCl}=38,6\left(g\right)\)

a) gọi hóa trị của kim loại A là x , của kim loại B là y
PTHH:
2A + 2xHCl \(\rightarrow\) 2AClx + xH2 (1)
2B + 2yHCl \(\rightarrow\) 2BCly + yH2 (2)
b) nH2 = V/22,4 = 8,96/22,4 = 0,4(mol) => mH2 = 0,4 x 2 = 0,8(g)
Theo PT(1)(2) => nHCl = 2nH2 = 2 . 0,4 = 0,8(mol)
=> mHCl = 0,8 x 36,5 =29,2(g)
Theo ĐLBTKL :
mhỗn hợp 2 kim loại + mHCl = m2 muối + mH2
=> a + 29,2 = 67 + 0,8 => a =38,6(g)

a, PT: \(R+H_2SO_4\rightarrow RSO_4+H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b, Ta có: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow V_{ddH_2SO_4}=\dfrac{0,4}{2}=0,2\left(l\right)\)
Theo ĐLBT KL, có: mKL + mH2SO4 = m muối + mH2
⇒ m muối = 7,8 + 0,4.98 - 0,4.2 = 46,2 (g)
c, Gọi: nR = x (mol) → nAl = 2x (mol)
Theo PT: \(n_{H_2}=n_R+\dfrac{3}{2}n_{Al}=x+\dfrac{3}{2}.2x=0,4\left(mol\right)\Rightarrow x=0,1\left(mol\right)\)
⇒ nR = 0,1 (mol)
nAl = 0,1.2 = 0,2 (mol)
⇒ 0,1.MR + 0,2.27 = 7,8 ⇒ MR = 24 (g/mol)
Vậy: R là Mg.

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Ag}=y\left(mol\right)\end{matrix}\right.\Rightarrow27x+108y=4,2\left(1\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,1 0,05 0,15
\(\Rightarrow m_{Al}=0,1\cdot27=2,7g\)
\(\Rightarrow m_{Ag}=4,2-2,7=1,5g\)
a)\(\%m_{Al}=\dfrac{2,7}{4,2}\cdot100\%=64,28\%\)
\(\%m_{Ag}=100\%-64,28\%=35,72\%\)
b)\(m_{muối}=0,05\cdot342=17,1g\)

a) Gọi x,y lần lượt là hóa trị của kim loại A, B
Pt: 2A + 2xHCl --> 2AClx + xH2
......2B + 2yHCl --> 2BCly + yH2
b) nH2 = \(\dfrac{8,96}{22,4}=0,4\) mol
mH2 = 0,4 . 2 = 0,8 (g)
Từ pt: => nHCl =2nH2 = 2. 0,4 = 0,8 mol
=> mHCl = 0,8 . 36,5 = 29,2 (g)
Áp dụng ĐLBTKL, ta có:
mhh + mHCl = mmuối + mH2
=> mhh = mmuối + mH2 - mHCl
Hay: a = 67 + 0,8 - 29,2 = 38,6 (g)

Gọi x,y lần lượt là số mol của A,B
nH2 = \(\dfrac{8,96}{22,4}=0,4\) mol
Pt: 2A + 2xHCl --> 2AClx + xH2
.....2B + 2yHCl --> 2BCly + yH2
Theo pt ta có: nHCl = 2nH2 = 2 . 0,4 = 0,8 mol
=> mHCl = 0,8 . 36,5 = 29,2 (g)
Áp dụng ĐLBTKL, ta có:
a = mmuối khan + mH2 - mHCl = 67 + (0,4 . 2) - 29,2 = 38,6 (g)

a) Mg + 2HCl \(\rightarrow\) MgCl2 + H2
Muối tạo thành: magie clorua
b) nMg = 8,4 : 24 = 0,35 mol
Theo pt: nH2 = nMg = 0,35 mol
=> V = 0,35 . 22,4 = 7,84l
c) Pt: 2Mg + O2 \(\xrightarrow[]{t^o}\) 2MgO
nO2 = 2,24 : 22,4 = 0,1 mol
Có nFe : nO2 = \(\dfrac{0,35}{2}:\dfrac{0,1}{1}=0,175:0,1\)
Do 0,175 > 0,1 nên Mg dư
nMg = 8.4 / 24 = 0.35 (mol)
Mg + 2HCl => MgCl2 + H2
0.35....................0.35....0.35
VH2 = 0.35 * 22.4 = 7.84 (g)
mMgCl2 = 0.35 * 95 = 33.25 (g)
nO2= 2.24 / 22.4 = 0.1 (mol)
2Mg + O2 -to-> 2MgO
2...........1
0.35......0.1
LTL: 0.35/2 > 0.1
=> Mg dư
Mg không cháy hết
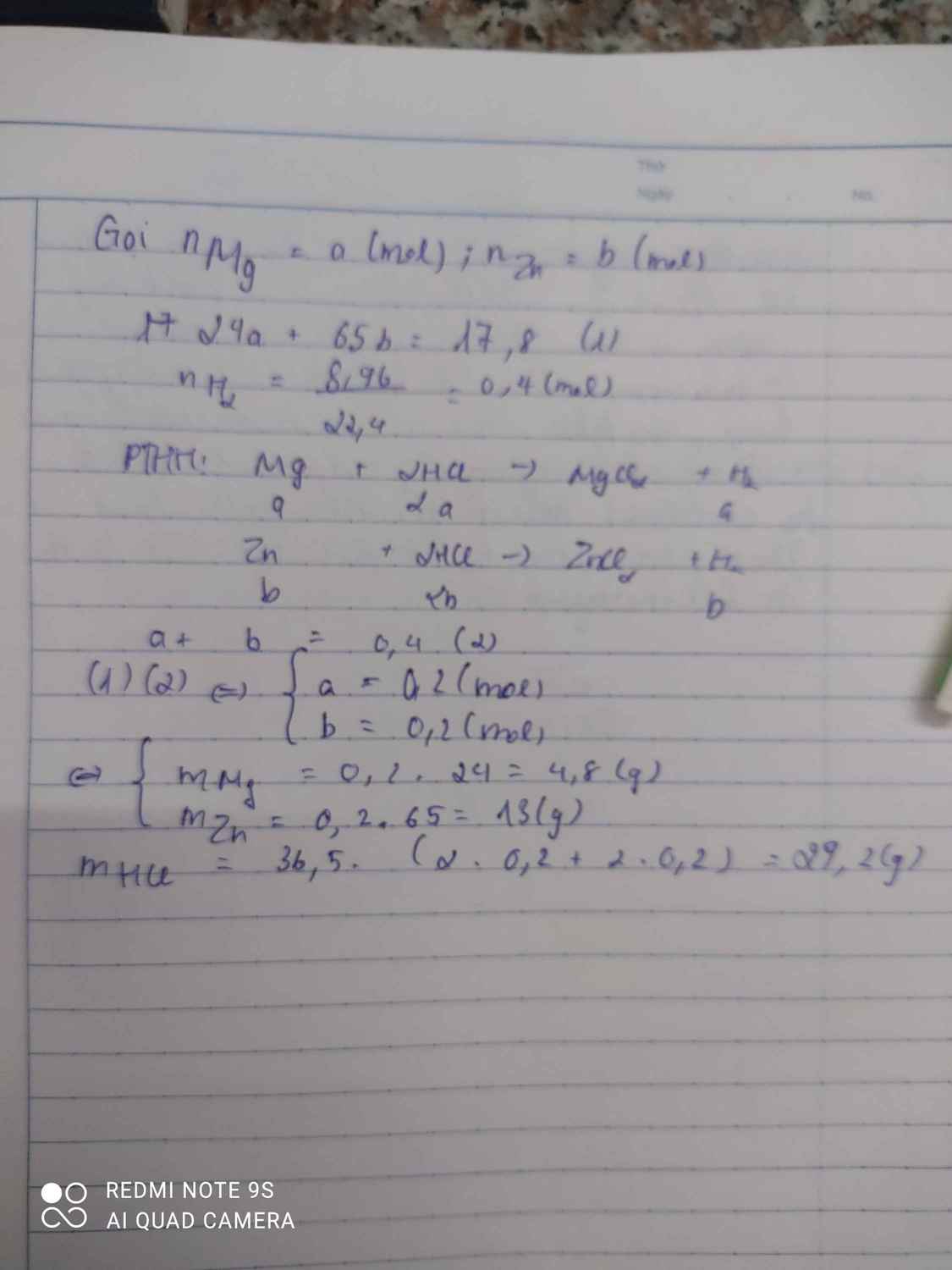
Do A và B đều tác dụng hết với dd HCl nên có thể viết được phương trình phản ứng :
2A + 2xHCl\(\rightarrow\)2 AClx +x H2;
2B+2yHCl\(\rightarrow\) 2BCly+yH2;
- Vì phản ứng xảy ra hết:
-nH2=\(\dfrac{8.96}{22.4}=0.4\left(mol\right)\) \(\Leftrightarrow\) mH2=0,8(g)
-Bảo toàn nguyên tố H: nH(H2)=nH(HCl)=2nH2=0.8(mol)
\(\Leftrightarrow\) nHCl=0.8(mol)
-mHCl=0,8.36,5=29,2(g)
- Áp dụng định luật bảo toàn khối lượng ta có:
a+mHCl=mMuối +mH2 => a=38.6(g)
Vậy ...
Gọi x, y lần lượt là hóa trị của kim loại A, B.
a. PTHH:
\(2A+2xHCl\rightarrow2ACl_x+xH_2\)
\(2B+2yHCl\rightarrow2BCl_y+yH_2\)
b. \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(\Rightarrow m_{H_2}=0,4.2=0,8\left(g\right)\)
Theo PT ta có: \(n_{HCl}=2.n_{H_2}=2.0,4=0,8\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,8.36,5=29,2\left(g\right)\)
Áp dụng ĐL BTKL ta có:
\(m_A+m_{HCl}=m_{muoi}+m_{H_2}\)
\(\Rightarrow m_A=m_{muoi}+m_{H_2}-m_{HCl}\)
\(\Rightarrow_A=67+0,8-29,2=38,6\left(g\right)\)