Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a_____2a______a_____a (mol)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
b_____3b_______b_____\(\dfrac{3}{2}\)b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}56a+27b=36,1\\a+\dfrac{3}{2}b=\dfrac{21,28}{22,4}=0,95\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,5\\b=0,3\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,5\cdot56=28\left(g\right)\\m_{Al}=8,1\left(g\right)\end{matrix}\right.\)
b+c) Theo các PTHH: \(\left\{{}\begin{matrix}n_{HCl}=2a+3b=1,9\left(mol\right)\\n_{FeCl_2}=0,5\left(mol\right)\\n_{AlCl_3}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{HCl}}=\dfrac{1,9}{0,2}=9,5\left(M\right)\\C_{M_{FeCl_2}}=\dfrac{0,5}{0,2}=2,5\left(M\right)\\C_{M_{AlCl_3}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\end{matrix}\right.\)

Vì Cu không tác dụng với HCl, nên chỉ có phản ứng của Fe.
PTHH: Fe+2HCl\(\rightarrow\)FeCl2+H2
a) nH2=0,15(mol)
Theo pt: nFe=nH2=0,15 (mol)
\(\Rightarrow\)mFe=8,4(g)
b) mCu=10-8,4=1,6(g)
c) Theo pt: nHCl=nH2=0,15(mol)
\(\Rightarrow\)VHCl=0,3(l)

\(n_{Fe} = a(mol) ; n_{Mg} = b(mol)\\ \Rightarrow 56a + 24b = 16,8 - 6,4 = 10,4(1)\\ Fe + 2HCl \to FeCl_2 + H_2\\ Mg + 2HCl \to MgCl_2 + H_2\\ n_{H_2} = a + b = \dfrac{6,72}{22,4} = 0,3(2)\)
Từ (1)(2) suy ra: a = 0,1 ; b = 0,2
Vậy :
\(\%m_{Fe} = \dfrac{0,1.56}{16,8}.100\% = 33,33\%\\ \%m_{Mg} = \dfrac{0,2.24}{16,8}.100\% = 28,57\%\\ \%m_{Cu} = 100\% - 33,33\% - 28,57\% = 38,1\%\)

PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\) (1)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\) (2)
a) Ta có: \(n_{H_2}=\dfrac{22,4}{22,4}=1\left(mol\right)=n_{Mg}\) \(\Rightarrow m_{Mg}=1\cdot24=24\left(g\right)\)
\(\Rightarrow\%m_{Mg}=\dfrac{24}{32}\cdot100\%=75\%\) \(\Rightarrow\%m_{MgO}=25\%\)
b) Theo 2 PTHH: \(\left\{{}\begin{matrix}n_{HCl\left(1\right)}=2n_{Mg}=2mol\\n_{HCl\left(2\right)}=2n_{MgO}=2\cdot\dfrac{32-24}{40}=0,4mol\end{matrix}\right.\)
\(\Rightarrow\Sigma n_{HCl}=2,4mol\) \(\Rightarrow m_{ddHCl}=\dfrac{2,4\cdot36,5}{7,3\%}=1200\left(g\right)\)
c) Theo PTHH: \(\Sigma n_{MgCl_2}=\dfrac{1}{2}\Sigma n_{HCl}=1,2mol\)
\(\Rightarrow\Sigma m_{MgCl_2}=1,2\cdot95=114\left(g\right)\)
Mặt khác: \(m_{H_2}=1\cdot2=2\left(g\right)\)
\(\Rightarrow m_{dd}=m_{hh}+m_{ddHCl}-m_{H_2}=1230\left(g\right)\)
\(\Rightarrow C\%_{MgCl_2}=\dfrac{114}{1230}\cdot100\%\approx9,27\%\)

a) \(n_{H_2}=\dfrac{6,16}{22,4}=0,275\left(mol\right)\)
Gọi \(x,y\) lần lược là số mol của Al và Fe
PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(x\) \(1,5x\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(y\) \(y\)
Ta có: \(1,5x+y=0,275\) (1)
Theo đề khối lượng của hỗn hợp Al và Fe ta có:
\(27x+56y=12,55\) (2)
Từ (1) và (2) ta có hệ:
\(\left\{{}\begin{matrix}1,5x+y=0,275\\27x+56y=12,55\end{matrix}\right.\)
Giải hệ phương trình ta tìm được:
\(\left\{{}\begin{matrix}x=0,05\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\%m_{Al}=\dfrac{0,05\cdot27\cdot100\%}{12,55}=10,7\%\)
\(\Rightarrow\%m_{Fe}=\dfrac{0,2\cdot56\cdot100\%}{12,55}=89,3\%\)
b) PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,05 0,15
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,2 0,4
\(n_{HCl}=0,4+0,15=0,55\left(mol\right)\)
\(\Rightarrow C_{MHCl}=\dfrac{0,55}{0,5}=1,1M\)

nH2=0.1(mol)
PTHH:Fe+H2SO4->FeSO4+H2
Fe2O3+3H2SO4->Fe2(SO4)3+3H2O
Theo pthh1:nFe=nH2->nFe=0.1(mol)
mFe=0.1*56=5.6(g)->%Fe=5.6:21.6*100=25.9%
%Fe2O3=100-25.9=74.1%
câu b câu c không liên quan đến đề bài bạn ơi,Chỉ có FeSO4,Fe2(SO4)3,và HCl thôi nhé,không có H2SO4 và MgSO4 đâu

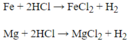
a, Gọi x,y lần lượt là số mol của Fe và Mg
PTHH: Fe + 2HCl -> FeCl2+ H2
1 2 1 1
(Mol) x->2x -> x ->x
Mg+ 2HCl-> MgCl2 + H2
1 2 1 1
(Mol) y-> 2y -> y -> y
Số mol của khí thu được sau Pứ: N=4,48/22,4= 0,2(mol)
Ta có hệ phương trình:
56x+24y=8
x+y=0,2
=>x= 0,1 mol, y= 0,1 mol( bạn giải hệ pt)
Vậy. Số gam Fe ban đầu trong hỗn hợp là: m=n.M=0,1*56=5,6(g)
=>m(Mg)= 8-5,6= 2,4(g)
b, khối lượng dd sau phản ứng:
m(ddHCl)+mFe-mFeCl2-mH2
=200+5,6-12,7-0,2
=192,7(g)
=> C% muối Fecl2 sau phản ứng là
C%= (12,7/192,7)*100≈ 6,6%
Làm tương tự, ta có: C% MgCl2≈ 73,5%
Câu b mình nghĩ là làm như vậy! Mình cũng ko chắc nhưng câu a thì chắc chắn đó!!!