Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

X + HCl \(\rightarrow\) XCl + 1/2H2 (1)
Y + 2HCl \(\rightarrow\) YCl2 + H2 (2)
Gọi x, y tương ứng là số mol của X và Y, theo pt (1) và (2) ta có: x/2 + y = nH2 = 5,6/22,4 = 0,25 mol. Suy ra: x + 2y = 0,5. Như vậy: 0,25 < x + y < 0,5
Khối lượng nguyên tử trung bình của X và Y là: M = 7,1/(x+y) Suy ra: 14,2 < M < 28,4.
Do đó chỉ có trường hợp X là Na (23) và Y là Mg (24) có khối lượng nguyên tử trung bình phù hợp với trường hợp trên.

Ta có : λo = 2300Ǻ = 2,3.10-7 (m). h= 6,625.10-34 (J.s), c = 3.108 m/s.
Emax=1,5( eV) = 1,5.1,6.10-19= 2,4.10-19(J)
Mặt khác: Theo định luật bảo toàn năng lượng và hiện tượng quang điện ta có công thức
(h.c)/ λ = (h.c)/ λo + Emax suy ra: λ=((h.c)/( (h.c)/ λo + Emax)) (1)
trong đó: λo : giới hạn quang điện của kim loại
λ: bước sóng của ánh sáng chiếu vào bề mặt kim loại để bứt electron ra khỏi bề mặt kimloại.
Emax: động năng ban đầu ( năng lượng của ánh sáng chiếu vào bề mặt kim loại).
Thay số vào (1) ta có:
λ = ((6,625.10-34.3.108)/((6,625.10-34.3.108)/(2,3.10-7) + (2,4.10-19)) = 1,8.10-7(m)
= 1800 Ǻ
Thầy xem hộ em lời giải của bài này ạ, em trình bày chưa được rõ ràng mong thầy sửa lỗi cho em ạ. em cám ơn thầy ạ!
Năng lượng cần thiết để làm bật e ra khỏi kim loại Vonfram là:
E===5,4eV
Để electron bật ra khỏi kim loại thì ánh sáng chiếu vào phải có bước sóng ngắn hơn bước sóngtấm kim loại. Mà năng lượng ánh chiếu vào kim loại có E1<E nên electron không thể bật ra ngoài

bảo toàn khối lượng ta có: 8,66+6,48+\(m_{khí}\)=28,99

Quy đổi hỗn hợp ban đầu thành Fe và O
Vì sau phản ứng còn dư kim loại => Fe chỉ bị oxi hóa lên Fe2+
Fe --> Fe2+ +2e
x...................2x
O + 2e -> O2-
y........2y
N+5 + 3e -> N+2
0,3.......0,1
Gọi x là nFe, y là nO
Ta có: 56x + 16y = 18,5 - 1,46
2x = 2y + 0,3
Giải ra: x= 0,27 mol, y = 0,12 mol
=> Khối lượng muối trong Y = 0,27 . 180 = 48,6 g
=> nHNO3 = nNO3- (trong muối) + nNO = 0,27.2 + 0,1 = 0,64 mol
=> C(HNO3) = 0,64/0,2 = 3,2 M

2Al + 2NaOH + 2H2O -> 2NaAlO2 + 3H2
0,2
=> mAl = 27.0,2 = 5,4 (gam) => %mAl = 5,4 %.
Gọi số mol của Fe và Cr trong hỗn hợp là x và y.
Fe + 2HCl -> FeCl2 + H2
x x(mol)
Cr + 2HCl -> CrCl2 + H2
y y
Ta có các phương trình : x + y = = 1,7 (1)
56x + 52y = 94,6 (2).
Giải hệ hai phương trình (1) và (2) ta được x = 1,55 ; y = 0,15.
=> mFe = 56.1,55 = 86,8 gam ; %mFe = 86,8%.
Và mCr = 52.0,15 = 7,8 (gam) ; %mCr = 7,8 %.

a) Zn + S ---> ZnS; Fe + S ---> FeS;
ZnS + H2SO4 ---> ZnSO4 + H2S; FeS + H2SO4 ---> FeSO4 + H2S
b) Gọi x, y là số mol Zn và Fe: 65x + 56y = 3,72 và x + y = 1,344/22,4 = 0,06
Giải hệ: x = 0,04; y = 0,02 ---> mZn = 65.0,04 = 2,6 g; mFe = 56.0,02 = 1,12 g.
a)Phương trình:
Zn+S→ZnS; Fe+S→FeS
ZnS+H2SO4→ZnSO4+H2S
FeS+H2SO4→FeSO4+H2S
b)Gọi m, m' là khối lượng Zn, Fe trong hỗn hợp ban đầu
m+m' = 3,72
nH2S=nZnS+nFeS=nZn+nFe=m/65+m'/56
=1,344/22,4=0,06
Bấm máy giải hệ phương trình:
m+m' = 3,72
(1/65).m+(1/56).m' = 0,06
ta được nghiệm: m = 2,6 ; m' = 1,12

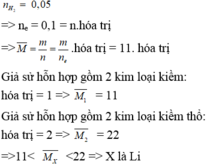
Đáp án C