Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(2Zn+O_2\underrightarrow{t^o}2ZnO\)
Ta có: \(\left\{{}\begin{matrix}n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{0,1}{1}\) \(\Rightarrow\) Oxi còn dư, Zn p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{O_2\left(dư\right)}=0,05\left(mol\right)\\n_{ZnO}=0,1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{O_2\left(dư\right)}=0,05\cdot32=1,6\left(g\right)\\m_{ZnO}=0,1\cdot81=8,1\left(g\right)\end{matrix}\right.\)

\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ n_{HCl}=\dfrac{36,5}{36,5}=1\left(mol\right)\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\a, V\text{ì}:\dfrac{0,1}{1}< \dfrac{1}{2}\Rightarrow HCl\text{dư}\\ n_{HCl\left(d\text{ư}\right)}=1-0,1.2=0,8\left(mol\right)\\ m_{HCl\left(d\text{ư}\right)}=0,8.36,5=29,2\left(g\right)\\ b,n_{ZnCl_2}=n_{Zn}=0,1\left(mol\right)\\ m_{ZnCl_2}=136.0,1=13,6\left(g\right)\)

Anh đoán là đkc chứ không phải đktc nhưng em cứ phản hồi nhé!

a, Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{2}< \dfrac{0,2}{1}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{1}{2}n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=0,05\left(mol\right)\Rightarrow m_{O_2\left(dư\right)}=0,05.32=1,6\left(g\right)\)
b, \(n_{H_2O}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{H_2O}=0,3.18=5,4\left(g\right)\)
c, PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
_______0,3_______________________0,15 (mol)
\(\Rightarrow m_{KMnO_4}=0,3.158=47,4\left(g\right)\)
Bạn tham khảo nhé!

PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\n_{HCl}=0,25\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,25}{2}\) \(\Rightarrow\) HCl còn dư, Kẽm p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,1\left(mol\right)\\n_{HCl\left(dư\right)}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=22,4\cdot0,1=2,24\left(l\right)\\m_{HCl\left(dư\right)}=0,05\cdot36,5=1,825\left(g\right)\end{matrix}\right.\)

\(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2mol\)
4P + 5O2 \(\underrightarrow{t^o}\) 2P2O5
\(\dfrac{0,1}{4}< \dfrac{0,2}{5}\) => O2 dư, Photpho đủ
\(n_{O_2}=0,2-0,04=0,16\left(mol\right)\)
\(m_{P_2O_5}=\) 0,05 . 142 = 7,1 ( g )

C9:
nP = 6,2/31 = 0,2 (mol)
nO2 = 6,4/32 = 0,2 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5
LTL: 0,2/4 > 0,2/5 => P dư
nP (p/ư) = 0,2/5 . 4 = 0,16 (mol)
nP (dư) = 0,2 - 0,16 = 0,04 (mol)
nP2O5 = 0,2/5 . 2 = 0,08 (mol)
mP2O5 = 0,08 . 142 = 11,36 (g)
C10:
Áp dụng ĐLBTKL, ta có:
mR + mO2 = mRO
=> mO2 = 21,6 - 16,8 = 4,8 (g(
=> nO2 = 4,8/32 = 0,15 (mol)
PTHH: 2R + O2 -> (t°) 2RO
nR = 0,15 . 2 = 0,3 (mol)
M(R) = 16,8/0,3 = 56 (g/mol(
=> R là Fe

a, PTHH: S + O2 -> (t°) SO2
b, nS = 6,4/32 = 0,2 (mol)
nO2 = 6,72/22,4 = 0,3 (mol)
LTL: 0,2 < 0,3 => O2 dư
nO2 (pư) = nSO2 = nS = 0,2 (mol)
mO2 (dư) = (0,3 - 0,2) . 32 = 3,2 (g)
c, mSO2 = 64 . 0,2 = 12,8 (g)
a, \(S+O_2\underrightarrow{t^o}SO_2\)
\(nS=\dfrac{6,4}{32}=0,2\left(mol\right)\)
\(nO_2=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(\dfrac{0,2}{1}< \dfrac{0,3}{1}\) => oxi dư
\(nO_{2\left(dư\right)}=0,1\left(mol\right)\)
\(mO_{2\left(dư\right)}=0,1.32=3,2\left(g\right)\)
\(nSO_2=nS=0,2\left(mol\right)\)
\(mSO_2=0,2.64=12,8\left(g\right)\)
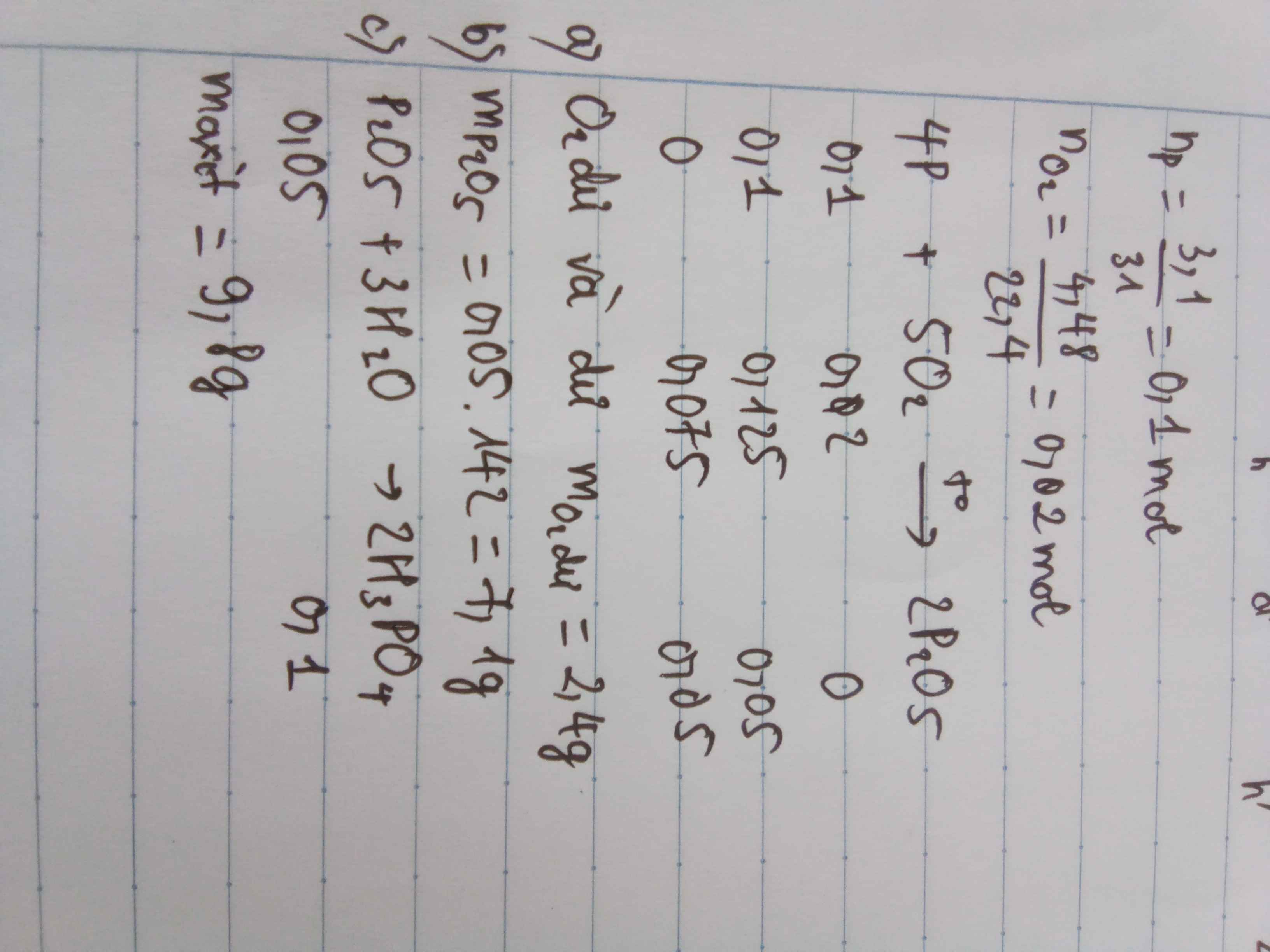
nZn = 6,5 / 65 = 0,1 (mol)
nO2 = 2,24 / 22,4 = 0,1 (mol)
2Zn + O2 --- > 2ZnO
0,1 0,05 0,1 (mol)
LTL : 0,1/2 < 0,1/1
= > O2 dư ; Zn đủ
mO2(dư) = (0,1-0,05 ) . 32 = 1,6 (g)
mZnO = 0,1 . 81 = 8,1 (g)