Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
PTHH: 2Al + 3H2SO4 ===> Al2(SO4)3 + 3H2
a)Vì Cu không phản ứng với H2SO4 loãng nên 6,72 lít khí là sản phẩm của Al tác dụng với H2SO4
=> nH2 = 6,72 / 22,4 = 0,2 (mol)
=> nAl = 0,2 (mol)
=> mAl = 0,2 x 27 = 5,4 gam
=> mCu = 10 - 5,4 = 4,6 gam
b) nH2SO4 = nH2 = 0,3 mol
=> mH2SO4 = 0,3 x 98 = 29,4 gam
=> Khối lượng dung dịch H2SO4 20% cần dùng là:
mdung dịch H2SO4 20% = \(\frac{29,4.100}{20}=147\left(gam\right)\)
nH2 = 6.72 : 22.4 = 0.3 mol
Cu không tác dụng với H2SO4
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
0.2 <- 0.3 <- 0.1 <- 0.3 ( mol )
mAl = 0.2 x 56 = 5.4 (g)
mCu = 10 - 5.4 = 4.6 (g )
mH2SO4 = 0.3 x 98 = 29.4 ( g)
mH2SO4 20% = ( 29.4 x100 ) : 20 = 147 (g)

a) 2AgNO3+CaCl2---->2AgCl+Ca(NO3)2
n AgNO3=1,7/170=0,01(mol)
n CaCl2=2,22/111=0,02(mol)
----> CaCl2 dư
Theo pthh
n AgCl=n AgNO3=0,01(mol)
m AgCl=0,01.143,5=14,35(g)
V dd sau pư=70+30=`100ml=0,1(l)
n CaCl2 dư=0,02-0,005=0,015(mol)
CM CaCl2=0,015/0,1=0,15(M)
Theo pthh
n Ca(NO3)2=1/2 n AgCl=0,005(mol)
CM Ca(NO3)2=0,005/0,1=0,05(M)
Bài 2
BaCl2+H2SO4--->BaSO4+2HCl
a) n BaCl2=400.5,2/100=20,8(g)
n BaCl2=20,8/208=0,1(mol)
m H2SO4=100.1,14.20/100=22,8(g)
n H2SO4=22,8/98=0,232(mol)
---->H2SO4 dư
Theo pthh
n BaSO4=n BaCl2=0,1(mol)
m BaSO4=0,1.233=23,3(g)
b) m dd sau pư=400+114-23,3
=490,7(g)
Theo pthh
n HCl=2n BaCl2=0,2(mol)
C%HCl=\(\frac{0,2.36,5}{490,7}.100\%=1,88\%\)
n H2SO4 dư=0,232-0,1=0,132(mol)
C% H2SO4=\(\frac{0,132.98}{490,7}.100\%=2,64\%\)
B1:
\(n_{AgNO3}=0,01\left(mol\right);n_{CaCl2}=0,2\left(mol\right)\)
PTHH:\(2AgNO3+CaCl2\rightarrow2AgCl2\downarrow+Ca\left(NO3\right)2\)
Trước :0,01................0,02..........................................................(mol)
Pứng:\(0,01\rightarrow0,005\rightarrow0,01\rightarrow0,005\)
Dư: 0............................0,015......................................................(mol)
\(m\downarrow_{AgCL}=0,01.143,5=1,435\left(g\right)\)
Trong dd sau phản ứng chứa: \(\left\{{}\begin{matrix}Ca\left(NO3\right)2:0,005\left(mol\right)\\CaCl2:0,015\left(mol\right)\end{matrix}\right.\)
\(C_{M_{Ca\left(NO3\right)2}}=\frac{0,005}{0,1}=0,05M\)
\(C_{M_{CaCl2}}=\frac{0,015}{0,1}=0,15M\)
Bài 2:\(n_{BaCl2}=\frac{400.5,2}{100.208}=0,1\left(mol\right)\)
\(D=\frac{m_{dd}}{v_{dd}};C\%=\frac{m_{ct}}{m_{dd}}.100\Rightarrow m_{H2SO4}=\frac{D.v.d^2.C\%}{100}=22,8g\)
\(\Rightarrow n_{H2SO4}=0,23\left(mol\right)\)
\(BaCl2+HSO4\rightarrow BaSO4\downarrow+2HCl\)
0,1..............0,1............0,1.................0,2.....(mol)
\(a,m_{\downarrow}=0,1.223=23,3\left(g\right)\)
\(b,m_{dd_{saupu}}=m_{BaCl2}+m_{dd_{H2SO4}}-m_{\downarrow}_{BaSO4}\)
\(=400+1,14.100-23,3=490,7\)
\(\Rightarrow C\%_{HCl}=\frac{0,2.36,5}{490,7}.100\%=1,48\%\)
\(\%H2SO4_{du}=\frac{\left(0,23-0,1\right).98}{490,7}.100=2,59\%\)

Bạn ơi d = gam / ml nha
Ta có mAgNO3 = V . D = 500 . 1,2 = 600 ( gam )
mHCl = V . D = 300 . 1,5 = 450 ( gam )
a, Gọi CM AgNO3 là C1
CM HCl là C2
Nồng độ mol của dung dịch cần tìm là C
VAgNO3 là V1
VHCl là V2

=> \(\dfrac{500}{300}\) = \(\dfrac{\left|2-C\right|}{\left|1-C\right|}\)
=> CM càn tìm = 1,375 M

a)
NaCl + AgNO3 -> NaNO3 + AgCl↓
0,1 0,1 0,1 0,1
b)
mNaCl = \(\frac{100.5,85}{100}=5,85\)=> nNaCl = 5,85 : 58,5 = 0,1 mol
mAgCl = 0,1 . 143,5 = 14,35 g
c)
mNaNO3 = 0,1 . 85 = 8,5 g
a, NaCl + AgNO3 --> NaNO3 +AgCl
1mol 1mol 1mol 1mol
0,1mol 0,1mol 0,1mol 0,1mol
b, mNaCl=100.5,85%=5,85g
nNaCl=\(\frac{5,85}{58,5}\)=0,1(mol)
mAgNO3=0,1.170=17g
mNaNO3=0,1.85=8,5g
mAgCl=0,1.143,5=14,35g

PTHH: \(NaCl+AgNO_3->NaNO_3+AgCl\) Số mol NaCl, \(AgNO_3\) tham gia: \(n_{NaCl}=0,5.2=1\left(mol\right)\) \(n_{AgNO_3}=0,6.2=1,2\left(mol\right)\) Lập tỉ lệ: \(\dfrac{1}{1}< \dfrac{1,2}{1}\) => \(AgNO_3\) dư, tính toán theo NaCl. Theo PTHH: \(n_{AgCl}=n_{NaCl}=1\left(mol\right)\) Khối lượng kết tủa AgCl thu được: \(m_{AgCl}=1.143,5=143,5\left(g\right)\)

a, nCO2= 16,8:22,4=0,75(mol) ; nNAOH=0,6.2= 1,2
ta có tỉ lệ nOH:nCO2=1,2:0,75=1,6(mol) => sản phẩm tạo 2 muối
ta có phtt:co2 +2naoh ----> na2co3+h2o
co2 +naoh----->nahco3
gọi x,y lần lượt là số mol của co2 ta có x+y=0,75
theo pthh ta có nNAOH=2x+y=1,2
=> x=0,45(mol) ; y=0,3(mol)
=> mMUỐI=mNA2CO3+mNAHCO3=0,45.106+0,3.84=72,9

a, Hiện tượng: có kết tủa trắng.
\(n_{KCl}=0,4\cdot2=0,8\left(mol\right);n_{AgNO_3}=2\cdot0,1=0,2\left(mol\right)\\ PTHH:KCl+AgNO_3\rightarrow KNO_3+AgCl\downarrow\\ ....0,2....0,2.....0,2....0,2\left(mol\right)\)
Vì \(\dfrac{n_{KCl}}{1}>\dfrac{n_{AgNO_3}}{1}\) nên sau phản ứng KCl dư, tính theo AgNO3
\(\Rightarrow m_{AgCl}=0,2\cdot143,5=28,7\left(g\right)\)
\(b,V_{dd\left(sau.p/ứ\right)}=V_{KNO_3}=V_{KCl}+V_{AgNO_3}=0,4+0,1=0,5\left(l\right)\\ \Rightarrow C_{M_{KNO_3}}=\dfrac{0,2}{0,5}=0,4M\)
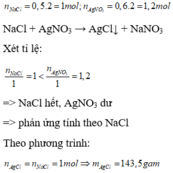
a)
Xuất hiện kết tủa màu trắng
b)
$AgNO_3 + NaCl \to AgCl + NaNO_3$
$n_{NaCl} = 0,5.2 = 1 < n_{AgNO_3} = 0,6.2 = 1,2$ nên $AgNO_3$ dư
$n_{AgCl} = n_{NaCl} = 1(mol)$
$m_{AgCl} = 1.143,5 = 143,5(gam)$
c)
$n_{NaNO_3} = n_{NaCl} = 1(mol)$
$n_{AgNO_3\ dư} = 1,2 - 1 = 0,2(mol)$
$V_{dd} = 0,5 + 0,6 = 1,1(lít)$
$C_{M_{NaNO_3}} = \dfrac{1}{1,1} = 0,91M$
$C_{M_{AgNO_3}} = \dfrac{0,2}{1,1} = 0,18M$