Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi \(\left\{{}\begin{matrix}n_{SO_2}=a\left(mol\right)\\n_{CO_2}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow a+b=\dfrac{4,48}{22,4}=0,2\) (1)
Theo đề bài: \(64a+44b=27\cdot2\cdot0,2\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
PTHH: \(SO_2+NaOH\rightarrow NaHSO_3\)
0,1______0,1 (mol)
\(CO_2+NaOH\rightarrow NaHCO_3\)
0,1______0,1 (mol)
Ta có: \(n_{NaOH}=0,2\left(mol\right)\) \(\Rightarrow V_{ddNaOH}=\dfrac{0,2}{1}=0,2\left(l\right)\)

Áp dụng sơ đồ đường chéo: SO2 CO2 M=27*2=54 64 44 10 10 1 1
=>VCO2=VSO2=2.2 lít=>nCO2=nSO2≃0.1
Vì thể tích NaOH cần dùng nhỏ nhất => tỉ lệ 1:1
NaOH+ CO2-------->NaHCO3
0.1.........0.1...................0.1
NaOH+ SO2--------->NaHSO3
0.1.........0.1...................0.1
=>nNaOH=0.2 mol
=>V=0.2/1=0.2 lít
Vậy cần dùng ít nhất 0.2 lít NaOH để hấp thụ A

Gọi số mol CO2 và SO2 là a, b (mol)
= >\(\left\{{}\begin{matrix}n_{khí}=a+b=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\\dfrac{44a+64b}{a+b}=29,5.2=59\end{matrix}\right.\) => \(\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,3\left(mol\right)\end{matrix}\right.\)
\(n_{NaOH}=1.0,4=0,4\left(mol\right)\)
PTHH: NaOH + CO2 --> NaHCO3
________0,1<----0,1------->0,1_______(mol)
NaOH + SO2 --> NaHSO3
_0,3<----0,3-------->0,3_____________(mol)
=> \(\left\{{}\begin{matrix}C_{M\left(NaHCO_3\right)}=\dfrac{0,1}{0,4}=0,25M\\C_{M\left(NaHSO_3\right)}=\dfrac{0,3}{0,4}=0,75M\end{matrix}\right.\)

PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
a, Giả sử: \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{22,4}{22,4}=1\left(mol\right)\left(1\right)\)
Ta có: \(n_{CO_2}=\dfrac{35,84}{22,4}=1,6\left(mol\right)\)
Theo PT: \(\Sigma n_{CO_2}=n_{CH_4}+2n_{C_2H_2}\)
\(\Rightarrow x+2y=1,6\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,4\left(mol\right)\\y=0,6\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,4}{1}.100\%=40\%\\\text{ }\%V_{C_2H_2}=60\%\end{matrix}\right.\)
b, Theo PT: \(\Sigma n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=2,3\left(mol\right)\)
\(\Rightarrow m_{O_2}=2,3.32=73,6\left(g\right)\)
c, PT: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
Theo PT: \(n_{Na_2CO_3}=n_{CO_2}=1,6\left(mol\right)\)
\(\Rightarrow C_{M_{Na_2CO_3}}=\dfrac{1,6}{0,8}=2M\)
Bạn tham khảo nhé!

a)
Gọi \(n_{SO_2} = n_{CO_2} = a(mol)\\ n_{CO} = b(mol)\)
Ta có :
\(M_A = \dfrac{m_{CO}+m_{CO_2} + m_{SO_2}}{n_{CO} + n_{CO_2} + n_{SO_2}}\)
⇔ \(\dfrac{28b+ 44a + 64a}{b + a + a} = 20,5.2\)
⇔ 108a + 28b = 41b + 82a
⇔ 26a = 13b
⇔ \(\dfrac{a}{b} = \dfrac{13}{26} = \dfrac{1}{2}\)
Suy ra : Nếu thể tích khí A được chia làm 4 phần thì CO chiếm 2 phần , CO2 và SO2 chiếm 1 phần
\(\%V_{CO_2} = \%V_{SO_2} = \dfrac{1}{4}.100\% = 25\%\\ \%V_{SO_2} = \dfrac{2}{4}.100\% = 50\%\)
b)
Ta có :
\(n_{CO_2} + n_{SO_2} = n_A.50\% = \dfrac{2,24}{22,4}.50\% = 0,05(mol)\)
\(2NaOH + CO_2 \to Na_2CO_3 + H_2O\\ 2NaOH + SO_2 \to Na_2SO_3 + H_2O\)
Theo PTHH :
\(n_{NaOH} = 2(n_{SO_2} + n_{CO_2}) = 0,1(mol)\\ \Rightarrow V_{NaOH} = \dfrac{0,1}{1} = 0,1(lít)\)

Đồng nhất dữ kiện các phần để tiện tính toán, bằng cách nhân khối lượng Br2 với 2. Bình H2SO4 đặc hấp thụ H2O, bình KOH đặc hấp thụ CO2. Khối lượng bình tăng chính là khối lượng khí hoặc hơi mà bình đó hấp thụ
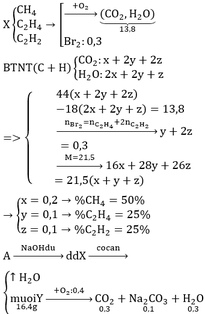
Vì bay hơi chỉ có nước, mà A tác dụng được với NaOH nên A chỉ chứa gốc phenol hoặc gốc cacboxylic (–COOH).
BTKL:
mY + mO2 = mCO2 + mNa2CO3 + mH2O => mO2 = 12,8g => nO2 = 0,4mol
BTNT O: nO(Y) + 2nO2 = 2nCO2 + 3nNa2CO3 + nH2O
=> nO(Y) = 0,4
=> nC : nH: nO: nNa = 0,4 : 0,6 : 0,4 : 0,2 = 2:3:2:1
=> C2H3O2Na => A: C2H4O2
(Vì A chứa gốc phenol (–OH) hoặc axit (–COOH) nên 1Na sẽ thế 1H).

5.
\(n_X=\dfrac{2,24}{22,4}=0,1mol\\ M_X=2,125.4=8,5g\cdot mol^{^{ }-1}\\ n_{H_2}=a;n_{C_2H_4}=b\\ a+b=0,1\\ 2a+28b=8,5.0,1=0,85\\ a=0,075;b=0,025\\ H_2+C_2H_4-^{^{ }Ni,t^{^{ }0}}->C_2H_6\\ V_{C_2H_6}=0,025.22,4=0,56L;V_{H_2dư}=22,4\left(0,075-0,025\right)=1,12L\)
6.
Thu được Y chỉ gồm hydrocarbon nên khí hydrogen phản ứng hết.
\(n_A=\dfrac{4,48}{22,4}=0,2mol\\ n_Y=\dfrac{3,36}{22,4}=0,15mol\\ \Delta n_{hh}=n_{H_2\left(pư\right)}=0,05\left(mol\right)\\ n_{C_2H_4}=0,15\left(mol\right)\\ a.\%V_{H_2}=\dfrac{0,05}{0,2}=25\%\\ \%V_{C_2H_4}=75\%\\ b.BTLK\pi:0,15=0,05+n_{Br_2}\\ n_{Br_2}=0,1mol\)