Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Coi hh gồm FeO và Fe2O3
nFeO=x,nFe2O3=y
72x + 160y = 5.36
x=0.01*3 ( bt e)
=> y=0.02
3Fe2+ + 4H+ + NO3- = 3Fe3+ + NO + 2H2O
0.02-----0.08-----0.01
=> nO2-=0.09=> nH+ pứ=0.09*2+0.01*4=0.22 => nH+ dư=0.17
=> nFe3+ = 0.03+0.02*2=0.07
3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO + 4H2O
0.03----0.08----0.02------0.03
Cu + 2Fe3+ =2Fe2+ + Cu2+
0.01--0.02------0.02
Áp dụng đl bt đt
=> nSO42- = (0.04*2 + 0.02*2 + 0.05*3)/2=0.135
=> mM' = 0.04*65 + 0.07*56 + 0.135*96 = 19.44g
=>ACoi hh gồm FeO và Fe2O3
nFeO=x,nFe2O3=y
72x + 160y = 5.36
x=0.01*3 ( bt e)
=> y=0.02
3Fe2+ + 4H+ + NO3- = 3Fe3+ + NO + 2H2O
0.02-----0.08-----0.01
=> nO2-=0.09=> nH+ pứ=0.09*2+0.01*4=0.22 => nH+ dư=0.17
=> nFe3+ = 0.03+0.02*2=0.07
3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO + 4H2O
0.03----0.08----0.02------0.03
Cu + 2Fe3+ =2Fe2+ + Cu2+
0.01--0.02------0.02
Áp dụng đl bt đt
=> nSO42- = (0.04*2 + 0.02*2 + 0.05*3)/2=0.135
=> mM' = 0.04*65 + 0.07*56 + 0.135*96 = 19.44g
=>C

A(Fe, S) ==nung==> B(Fe, S, FeS) ==HCl==> C(H2, H2S)
B(Fe, S, FeS) ==nung==> (Fe2O3, SO2)
Bằng phương pháp sơ đồ đường chéo bạn dễ dàng tính được tỉ lệ nH2/nH2S = 1/3
Mà nH2 + nH2S = V
=> nH2 = 0,25V và nH2S = 0,75V
Sau khi viết tất cả các phương trình phản ứng, bạn dễ dàng tính được những kết quả sau :
nFe (trong B) = nH2 = 0,25V mol => mFe = 14V g
nFeS (trong B) = nH2S = 0,75V mol => mFeS = 66V g
Phản ứng của B với O2 :
4FeS + 7O2 = 2Fe2O3 + 4SO2
0,75V....1,3125V mol
S + O2 = SO2
x.....x
Ta có 1,3125V + x = V'' => nS = x = V'' - 1,3125V
=> mS = 32V'' - 42V
mB = mFe + mS + mFeS = 14V + 32V'' - 42V + 66V = 38V + 32V'' g
b. nS = V'' - 1,3125V => V'' > 1,3125V => V''/V > 1,3125

Đáp án B
Sơ đồ:

« Phân tích: Trước hết, ta tính nhanh:
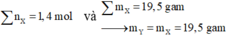
Yêu cầu tỉ khối của Y so với H2; khối lượng đã biết ® cần xác định số mol hỗn hợp Y nữa là xong.
“Tinh ý”: n Z = 0 , 85 m o l đã biết, phần còn lại của Y bị AgNO3 giữ lại đều là ankin (có 2p).
8 gam Br2 phản ứng với 0,05 mol cho biết số mol hai anken là 0,05 mol → ∑ n π t r o n g Z = 0 , 05 m o l
Gọi số mol hai ankin là x mol thì
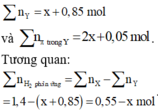
1 mol H2 phản ứng lấy 1 mol p trong X, ban đầu X có tổng số mol p là 0 , 2 × 2 + 0 , 1 × 2 + 0 , 15 = 0 , 75 .
® bảo toàn số mol p ta có ngay: 0 , 75 - 0 , 55 - x = 2 x + 0 , 05 → x = 0 , 15 m o l .
Thay ngược lại → d Y / H 2 = 19 , 5 2 × 0 , 15 + 0 , 85 = 9 , 75

Đáp án B
Ta có: n x = 0,2+0,1+0,15+0,1+0,85=1,4 mol
Gọi a là số mol H2 phản ứng, b là số mol ankin còn dư trong Y.
Ta có: n z = 0,85= 1,4 -a-b
Mặt khác cho Z vào dung dịch brom dư thấy có 0,05 mol Br2
→ n π ( Z ) = 0 , 05 m o l
Bảo toàn liên kết π: 0,2.2+0,1.2+0,15-a-2b=0,05
Giải hệ: a=0,4; b=0,15.
→ n Y = 1 , 4 - 0 , 4 = 1 m o l
Ta có: m Y = m X = 19 , 5 g a m → M - Y = 19 , 5 → d Y / H 2 = 9 , 75

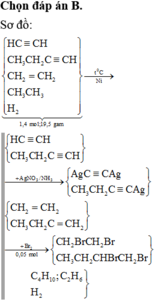


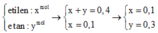
Chọn A