Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
► Bảo toàn electron: 3nAl = 2nH2 ⇒ nAl = 0,02 mol.
"vừa đủ" ⇒ X chỉ chứa AlCl3 || 0,09 mol hay 0,13 mol NaOH cho cùng 1 lượng ↓
⇒ 0,09 mol NaOH thì ↓ chưa đạt cực đại và 0,13 mol NaOH thì ↓ bị hòa tan 1 phần.
⇒ n↓ = 0,09 ÷ 3 = 0,03 mol. ||► Mặt khác, khi bị hòa tan 1 phần thì:
nOH– = 4nAl3+ – n↓ ⇒ nAl3+ = (0,03 + 0,13) ÷ 4 = 0,04 mol.
Bảo toàn nguyên tố Al: nAl2O3 = 0,01 mol ||⇒ m = 1,56(g)

Định hướng tư duy giải
→ n NH 4 + = 0 , 235 . 2 - 0 , 14 . 3 8 = 0 , 00625
=> 110,23 = 0,73943m + 96.(0,235+0,26057m/16) => m = 38,07
=> mY = 28,15 + 62.(0,00625.8 + 0,14.3 + 0,62.2) + 80.0,00625 = 134,67

Đáp án C
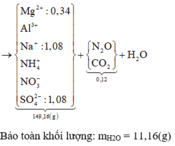
Quan sát sơ đồ quá trình
quy đổi + xử lí:
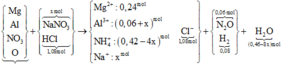
► NaOH vừa đủ xử lí "kép"
dung dịch sau phản ứng:
♦1: đọc ra chất rắn cuối cùng
là 0,24 mol MgO
→ biết ∑nMg
(vì thế mà chúng ta có xu hướng
quy đổi lại hỗn hợp X như trên sơ đồ).
♦2: Natri đi về đâu?
gọi nNaNO3 = x mol thì với
1,14 mol NaOH nữa là
∑nNa+ = 1,14 + x mol.
đi về NaCl và NaAlO2
Biết nCl = 1,08 mol nên đọc ra
nNaAlO2 = 0,06 + x mol.
Bảo toàn N có ngay và luôn
nNO3 trong X = (0,54 – 5x) mol.
có mỗi một giả thiết mX = 13,52 g
nên cần tìm nO trong X nữa là sẽ giải
và tìm được x.
♦1 Bảo toàn electron mở rộng:
∑nH+ = 10nN2O + 10nNH4+ + 2nH2 + 2nO trong X
♦2: bảo toàn H tìm nH2O rồi bảo toàn O
(ghép cụm NO3) => nO trong X
→ theo cả 2 cách đều cho biết
nO trong X = 20x – 1,94 mol.
Như phân tích trên:
giải mX = mMg + mAl + mO + mNO3
= 13,52 gam có x = 0,1 mol.
Từ đó đọc ra nO trong X = 0,06 mol
→ nAl2O3 = 0,02 mol; mà ∑nAl = 0,16 mol
→ nAl = 0,12 mol
→ Yêu cầu %mAl trong X ≈ 23,96 %.
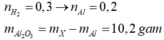
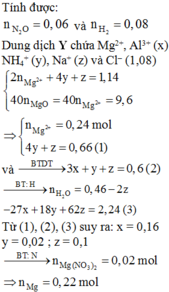
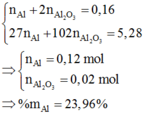
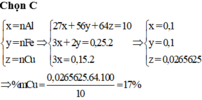


Đáp án C
nH2 = 13,44: 22,4 = 0,6 mol
- Các phản ứng:
Al2O3 + 2NaOH → 2NaAlO2 + H2O
Al + NaOH → NaAlO2 + 1,5H2
Mol: 0,4 ← 0,6
=> %mAl = 0,4.27 / 31,2 = 34,6%
=> %mAl2O3 = 100 % - %mAl = 100% - 34,6% = 65,4%