Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
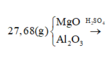
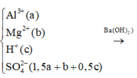
Tại thời điểm: m(kết tủa) = const → Mg(OH)2 và BaSO4.
→ n(kết tủa) = b + (1,5a + b + 0,5a) = 0,94
Tại thời điểm đó, n(Ba(OH)2) = 1,1 → n(OH-) = 2,2 → 4a + 2b + c = 2,2
Khối lượng chất rắn ban đầu: 40b + 51a = 27,68
→ a = 0,48 và b = 0,08 và c = 0,12 → x = n(SO42-) = 0,86

Đáp án D
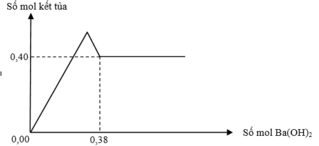
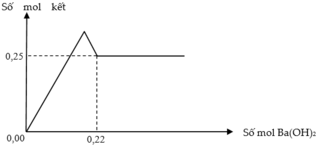
Dựa vào đồ thị:
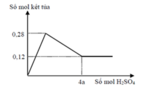
+Thấy lúc kết tủa cực đại thì lúc này kết tủa sẽ gồm BaSO4 và Al(OH)3 có tổng số mol là 0,28 mol.
+Lúc kết tủa không thay đổi thì nó chỉ gồm BaSO4 có số mol 0,12 mol.
Suy ra n(BaSO4) = 0,12 mol nên n(Al(OH)3) =0,16 mol
Lúc kết tủa Al(OH)3 vừa bị hoà tan hết thì dùng 4a mol H2SO4 lúc này SO42- đã đi và 0,12 mol BaSO4 và 0,08 mol Al2(SO4)3.
Bảo toàn S: n(H2SO4) = 4a = 0,12+ 0,08 . 3 = 0,36 nên a= 0,09
Bảo toàn nguyên tố suy ra số mol Ba và Al trong hỗn hợp ban đầu là 0,12 và 0,16 mol (về nguyên tố).
Bảo toàn e: n(O) =[2n(Ba) +3n(Al) -2n(H2)] / 2 = 0,27mol
Suy ra m= 0,12. 137 + 0,16. 27 + 0,27 . 16 = 25,08

Đáp án D
Cho hỗn hợp Na2O và Al2O3 vào 0,12 mol H2SO4 và 0,36 mol HCl thu được dung dịch X.
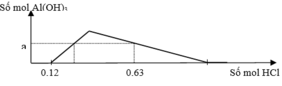
Cho Ba(OH)2 dư vào X ta thấy đồ thị như trên do vậy có các giai đoạn:
+Giai đoạn kết tủa tăng do tạo kết tủa BaSO4 và Al(OH)3.
+Kết tủa giảm do có sự hòa tan Al(OH)3.
+Kết tủa không đổi lúc này chỉ còn BaSO4.
Gọi số mol Na2O và Al2O3 lần lượt là a, b.
Kết tủa cực đại chứa BaSO4 0,12 mol và Al(OH)3
n A l ( O H ) 3 = 0 , 12 m o l => b = 0,06 mol
Suy ra: 0,28.2 + 2a - 0,12 - 0,12.2 - 0,36 = 0 => a = 0,08 mol
=> m = 11,08 gam

Đáp án A
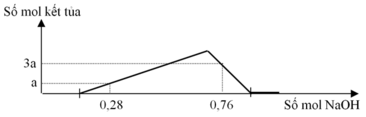
Nhìn vào đồ thì, phải mất 1 khoảng mol NaOH mới bắt đầu xuất hiện kết tủa chứng tỏ X có H2SO4 dư, và lượng mol đó tác dụng với axit.
X gồm: Al2(SO4)3 và H2SO4 dư.
Ta có: n(Al) = 0,18. BTNT (Al):
n(Al3+ trong X) = 0,18; gọi n(H+) dư = y
Tại thời điểm n(NaOH) = 0,28
→ 0,28 = y +3a
Tại thời điểm n(NaOH) = 0,76
→ 0,76 = y + 3a. 3 + (0,18 – 3a). 4
→ y = 0,16 và a = 0,04 → n(H2SO4) dư = 0,08
→ x = 0,08 + 3 n(Al2(SO4)3) = 0,08 + 3. 0,09 = 0,35

Đáp án A
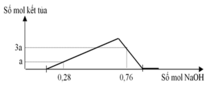
Nhìn vào đồ thì, phải mất 1 khoảng mol NaOH mới bắt đầu xuất hiện kết tủa chứng tỏ X có H2SO4 dư, và lượng mol đó tác dụng với axit.
X gồm: Al2(SO4)3 và H2SO4 dư.
Ta có: n(Al) = 0,18. BTNT (Al): n(Al3+ trong X) = 0,18; gọi n(H+) dư = y
Tại thời điểm n(NaOH) = 0,28 → 0,28 = y +3a
Tại thời điểm n(NaOH) = 0,76 → 0,76 = y + 3a. 3 + (0,18 – 3a). 4
→ y = 0,16 và a = 0,04 → n(H2SO4) dư = 0,08 → x = 0,08 + 3 n(Al2(SO4)3) = 0,08 + 3. 0,09 = 0,35

Đáp án D
Hòa tan hết Na2O và Al tỉ lệ 1:1 ta thu được dung dịch chứa Na2SO4, Al2SO4 và H2SO4 dư có thể có.
Ta có: n H 2 = 6 a → n A l = 4 a
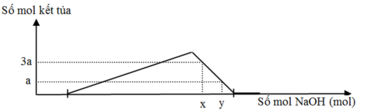
Nhận thấy lúc thêm x và y y mol NaOH đều trong giai đoạn kết tủa giảm tức hòa tan kết tủa nên lúc này tương ứng 1 mol Al(OH)3 bị hòa tan thì có 1 mol NaOH được thêm
Do vậy:
![]()
![]()
X chứa Al2(SO4)3 0,08 mol và Na2SO4 0,16 mol
→ m = 50 , 08
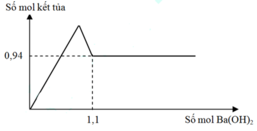
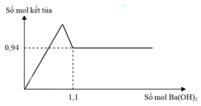
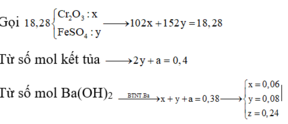
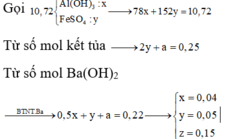


Đáp án C
Tại thời điểm: m(kết tủa) = const
→ Mg(OH)2 và BaSO4.
→ n(kết tủa) = b + (1,5a + b + 0,5a) = 0,94
Tại thời điểm đó,
n(Ba(OH)2) = 1,1 → n(OH-) = 2,2
→ 4a + 2b + c = 2,2
Khối lượng chất rắn ban đầu:
40b + 51a = 27,68
→ a = 0,48 và b = 0,08 và c = 0,12
→ x = n(SO42-) = 0,86