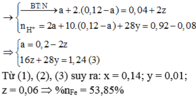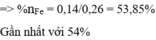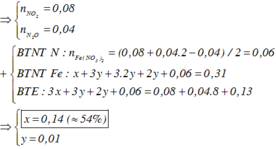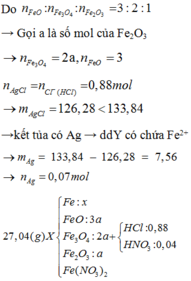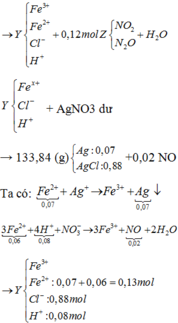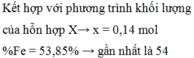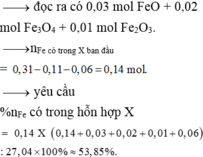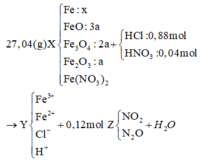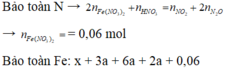Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
+ T r o n g X : n F e = x ; n F e O = 3 y ; n F e 3 O 4 = 2 y ; n F e 2 O 3 = y ; n F e ( N O 3 ) 2 = z + P Ư 1 : X d d Y + . . . P Ư 2 : Y N O + . . . ⇒ Y c h ứ a C l - : 0 , 88 m o l H + , F e 2 + , F e 3 + + n H + t r o n g Y = 4 n N O = 0 , 08 n F e 2 + t r o n g Y = 3 n N O + n A g ⇒ n H 2 O t ạ o r a ở P Ư 1 = 0 , 88 + 0 , 04 - 0 , 08 2 = 0 , 42 n F e 2 + t r o n g Y = 3 . 0 , 02 + ( 133 , 84 - 0 , 88 . 143 , 5 ) 108 = 0 , 13 + B T ~ N T c h o Y ⇒ n F e 3 + = 0 , 18 ⇒ m c á c c h ấ t tan t r o n g Y = 48 , 68 + n N O 2 + n N 2 O = 0 , 12 46 n N O 2 + 44 n N 2 O = m X + m a x i t - m c h ấ t tan t r o n g Y - m H 2 O = 5 , 44 ⇒ n N O 2 = 0 , 08 n N 2 O = 0 , 04 + B T N T N : n F e ( N O 3 ) 2 = ( 0 , 08 + 0 , 04 . 2 - 0 , 04 ) / 2 = 0 , 06 B T N T F e : x + 3 y + 3 . 2 y + 2 y + 0 , 06 = 0 , 31 B T E : 3 x + 3 y + 2 y + 0 , 06 = 0 , 08 + 0 , 04 . 8 + 0 , 13 ⇒ x = 0 , 14 ( ≈ 54 % ) y = 0 , 01

Đáp án C
Bảo toàn Cl : nHCl = nAgCl = 0,88 mol
,mkết tủa = mAgCl + mAg(nếu có) = 133,84g => nAg = 0,07 mol = nFe2+
=> dung dịch Y có Fe2+ và Fe3+ ; H+ dư ,Cl- (không có NO3-)
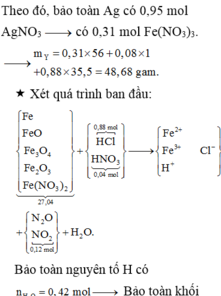
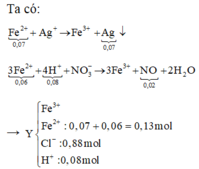
3Fe2+ + 4H+ + NO3- -> 3Fe3+ + NO + 2H2O
Fe2+ + Ag+ -> Fe3+ + Ag
=> nH+ dư = 4nNO = 0,08 mol ; nFe2+(Y) = 3nNO + nAg = 0,13 mol
Bảo toàn điện tích : 2nFe2+ + 3nFe3+ + nH+ = nCl- => nFe3+ = 0,18 mol
Gọi số mol Fe : x ; FeO : 3y ; Fe3O4 : 2y ; Fe2O3 : y ; Fe(NO3)2 : z
=> nX = x + 6y + z
=> Qui về : x mol Fe ; 5y mol FeO ; 3y mol Fe2O3 ; z mol Fe(NO3)2
=> mX = 56x + 840y + 180z = 27,04
Bảo toàn Fe : x + 11y + z = 0,13 + 0,18 = 0,31 mol
,nH+ pứ bđ = 2nH2O => nH2O = ½ (0,88 + 0,04 – 0,08) = 0,42 mol
Bảo toàn khối lượng : mX + mHCl + mHNO3 = mion muối Y + mKhí + mH2O
=> mKhí = mNO2 + mN2O = 5,44g và nNO2 + nN2O = 0,12
=> nNO2 = 0,08 ; nN2O = 0,04 mol
Bảo toàn N : 2nFe(NO3)2 + nHNO3 = 2nN2O + nNO2 => nFe(NO3)2 = z = 0,06 mol
=>x = 0,14 ; y = 0,01
=> nX = 0,26 mol
=> %nFe(X) = 53,85%
=>C

Đáp án : A
Dd Y + dd AgNO3:
3Fe2+ + 4H+ + NO3 – → 3 Fe3+ + NO + 2H2O
0,06← 0,08← 0,02 ← 0,02
Kết tủa gồm AgCl và Ag. Trong đó: n AgCl = n HCl = 0,88 mol
=> m Ag = 133,84 – 0,88. 143,5 = 7,56 gam
=> n Ag = 0,07 mol
Fe2+ + Ag+ → Fe3+ + Ag
0,07← 0,07 0,07 0,07
=> ∑ n Fe2+ (ddY) = 0,06 + 0,07 = 0,13 mol
n H+ dư (ddY) = 0,08 mol
=> dd Y gồm Fe+ ; Fe3+; H+ và Cl –
Bảo toàn điện tích trong dd có: 2 n Fe2+ + 3n Fe3+ + n H+ = n Cl –
<=> 3 n Fe3+ = 0,88 – 2. 0,13 – 0,08 = 0,54 mol
<=> n Fe3+ = 0,18 mol
Mặt khác, có ∑ n H+ bđ = 0,88 + 0,04 = 0,92 mol
=> n H+ p.ư = 2. n H2O = 0,84 mol
=> n H2O = 0,42 mol
X + HCl + HNO3 → Muối + axit dư + khí + H2O
(0,88 mol) (0,04 mol)
BTKL => m khí = 27,04 + 0,88. 36,5 + 0,04. 63 – 0,42. 18 – 0,31. 56 – 0,08 – 0,88. 35,5 = 5,44 gam
Gọi n N2O = x mol; n NO = y mol
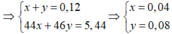
BT nguyên tố N: có n N [Fe(NO3)2] + n N(HNO3) = n N(sp khử)
=> 2. n Fe(NO3)2 + 0,04 = 0,04. 2 + 0,08 = 0,16
=> n Fe(NO3)2 = 0,06 mol
=> m Fe + m FeO + m Fe2O3 + m Fe3O4 (hhX) = 27,04 – 0,06. 180 = 16,24 gam (I)
Mặt khác, n FeO : Fe3O4 : n Fe2O3 = 3: 2: 1
=> Đặt n Fe2O3 = a => n Fe3O4 = 2a và n FeO = 3a
Đặt n Fe = b
Theo (I) => 56b + 840 a = 16,24 (1)
∑ n Fe(I) = 0,31 – 0,06 = 0,25 <=> b + 11a = 0,25 (2)
Từ (1) và (2) => a = 0,01 và b = 0,14 mol
=> % m Fe = (0,14. 56) : 27,04 = 28,99%