Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(n_{CaO}=n_{Ca\left(OH\right)_2}=\dfrac{3,36}{56}=0,06\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{1,2}{100}=0,012\left(mol\right)\)
TH1: CO2 hết, Ca(OH)2 dư
PTHH: Ca(OH)2 + CO2 -----> CaCO3 + H2O
0,012 -> 0,012 mol
=> VCO2 = 0,012 . 22,4 = 0,27 (l)
TH2: CO2 dư
PTHH: Ca(OH)2 + CO2 -> CaCO3 + H2O
0,06 ..............0,06......0,06
CO2 + CaCO3 + H2O -> Ca(HCO3)2
0,048<--(0,06 - 0,012)
=> nCO2 = 0,06 + 0,048 = 0,108 mol
=> VCO2 = 0,108 . 22,4 = 2,42 (l)

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
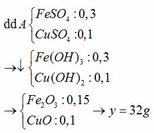

Tính toán theo PTHH :
Na + HCl → NaCl + ½ H2
Na + H2O → NaOH + ½ H2
3NaOH + AlCl3 → NaCl + Al(OH)3↓
NaOH + Al(OH)3↓→ NaAlO2 + 2 H2O ( có thể có )
n Na = 0,2 mol , n HCl = 0,25 . 0,2 = 0,05 mol , n AlCl3 = 0,4 . 0,2 = 0,08 mol
Theo PTHH : n Na = n HCl = 0,05 mol => Na dư : n Na dư = 0,2 – 0,05 = 0,15 mol
Theo PTHH : n Na = n NaOH = 0,15 mol
Theo PTHH : n NaOH = n AlCl3 . 3 ó 0,15 < 0,08 . 3 => AlCl3 dư => NaOH hết
=> n Al(OH)3 = 0,15 : 3 = 0,05 mol
=> m Al(OH)3 = 0,05 . 78 =3,9 g

Nhận xét: nAl(OH)3 = 0,05 < nAlCl3 → kết tủa chưa đạt tối đa.
TH1: kết tủa chưa bị hòa tan
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
0,025 ← 0,05
3Ba(OH)2 + 2AlCl3 → 3BaCl2 + 2Al(OH)3↓
0,075 ← 0,05
→ nBa(OH)2 = 0,1 → V = 100 ml
TH2: kết tủa bị hòa tan một phần
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
0,025 ← 0,05
3Ba(OH)2 + 2AlCl3 → 3BaCl2 + 2Al(OH)3↓
0,15 ← 0,1 → 0,1
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
0,025 ← 0,05
Dư: 0,05
→ nBa(OH)2 = 0,2 → V = 200 ml
Vậy có 2 giá trị của V là: 100 và 200

mddH2SO4 = 100 . 1,137 = 113,7
nH2SO4 = 113,7 . 20%/98 = 0,232 mol
nBaCl2 = 400 . 5,29%/208 = 0,1 mol
H2SO4 + BaCl2 —> BaSO4 + 2HCI
Bđ: 0,232 0,1
Pứ: 0,1 0, 1 0,1 0,2
Sau pứ: 0,132 0
mBaSO4 = 0,1.233 = 23,3 gam
Khối lượng dung dịch sau khi lọc bỏ kết tủa:
mddB = mddH2SO4 + mddBaCl2 - mBaSO4 = 490,4
C%HCI = 0,2.36,5/490,4 = 1,49%
C%H2SO4 dư = 0,132.98/490,4 = 2,64%

\(2Al+6HCl \rightarrow 2AlCl_3+3H_2\\ Mg+2HCl \rightarrow MgCl_2+H_2\\ n_a=Al\\ n_b=Mg\\ m_{hh}=27a+24b=7,8(1)\\ m_{muối}=133,5a+95b=36,2(2)\\ (1)(2)\\ a=0,2\\ b=0,1\\ n_{H_2}=1,5a+b=1,5.0,2+0,1=0,4mol\\ V_{H_2}=0,4.22,4=8,96l\)



\(n_{AlCl3}=\dfrac{26,7}{133,5}=0,2\left(mol\right)\)
\(n_{Al\left(OH\right)3}=\dfrac{7,8}{78}=0,1\left(mol\right)\)
Vì \(n_{Al\left(OH\right)3}< n_{AlCl3}\) nên có 2 gtr \(n_{KOH}\) thỏa mãn
PTHH : \(AlCl_3+3KOH-->Al\left(OH\right)_3+3KCl\) (1)
\(Al\left(OH\right)_3+KOH-->KAlO_2+2H_2O\) (2)
TH1 : KOH thiếu => Chỉ xảy ra pứ (1)
\(n_{KOH}=3n_{Al\left(OH\right)3}=0,3\left(mol\right)\)
=> \(C\%KOH=\dfrac{56.0,3}{400}.100\%=4,2\%=a\%\)
=> a = 4,2
TH2 : KOH dư => Xảy ra pứ (1) và (2)
Có : \(n_{KOH}=3n_{AlCl3}+n_{Al\left(OH\right)3tan}\)
\(=3n_{AlCl3}+\left(n_{Al\left(OH\right)3sinhra}-n_{Al\left(OH\right)3thuduoc}\right)\)
\(=3n_{AlCl3}+\left(n_{AlCl3}-n_{Al\left(OH\right)3thuduoc}\right)\)
\(=4n_{AlCl3}-n_{Al\left(OH\right)3thuduoc}\)
\(=4.0,2-0,1=0,7\left(mol\right)\)
=> \(C\%KOH=\dfrac{0,7.56}{400}.100\%=9,8\%=a\%\)
=> a = 9,8