Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)Gọi x,y lần lượt là số mol của Al, Fe trong hỗn hợp ban đầu (x,y>0)
Sau phản ứng hỗn hợp muối khan gồm: \(\left\{{}\begin{matrix}AlCl_3:x\left(mol\right)\\FeCl_2:y\left(mol\right)\end{matrix}\right.\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}27x+56y=13,9\\133,5x+127y=38\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,0896\\y\approx0,205\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,0896\cdot27\cdot100\%}{13,9}\approx17,4\%\\\%m_{Fe}=\dfrac{0,205\cdot56\cdot100\%}{13,9}\approx82,6\%\end{matrix}\right.\)
Theo Bảo toàn nguyên tố Cl, H ta có:\(n_{H_2}=\dfrac{n_{HCl}}{2}=\dfrac{3n_{AlCl_3}+2n_{FeCl_2}}{2}\\ =\dfrac{3\cdot0,0896+2\cdot0,205}{2}=0,3394mol\\ \Rightarrow V_{H_2}=0,3394\cdot22,4\approx7,6l\)

nH2= 0,35(mol)
a) PTHH: Mg + 2 HCl -> MgCl2 + H2
x_________2x_______x______x(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
y________2y________y_____y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}24x+56y=13,2\\x+y=0,35\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,15\end{matrix}\right.\)
b) m=m(muối khan)= mMgCl2 + mFeCl2= 95.x+127y=95.0,2+127.0,15= 38,05(g)
a)
Gọi
\(n_{Fe} = a(mol) ; n_{Mg} = b(mol)\\ \Rightarrow 56a + 24b = 13,2(1)\)
\(Mg + 2HCl \to MgCl_2 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\)
Theo PTHH : \(n_{H_2} = a + b = 0,35(mol)\)(2)
Từ (1)(2) suy ra a = 0,15 ;b = 0,2
Vậy :
\(\%m_{Fe} = \dfrac{0,15.56}{13,2}.100\% = 63,64\%\\ \Rightarrow m_{Mg} = 100\% - 63,64\% = 36,36\%\)
b)
Ta có :\(n_{HCl} = 2n_{H_2} = 0,7(mol)\)
Bảo toàn khối lượng :
\(m_{muối} = m_{kim\ loại} + m_{HCl} - m_{H_2} = 13,2 + 0,7.36,5 - 0,35.2=38,05(gam)\)

Sửa đề: đktc → đkc
a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: 24nMg + 56nFe = 13,2 (1)
\(n_{H_2}=\dfrac{8,6765}{24,79}=0,35\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}+n_{Fe}=0,35\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,2\left(mol\right)\\n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,2.24}{13,2}.100\%\approx36,36\%\\\%m_{Fe}\approx63,64\%\end{matrix}\right.\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{MgCl_2}=n_{Mg}=0,2\left(mol\right)\\n_{FeCl_2}=n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\)
⇒ m muối khan = 0,2.95 + 0,15.127 = 38,05 (g)

Đáp án D
Số mol H2 thu được là : n H 2 = 11 , 2 22 , 4 = 0 , 5 mol
Gọi M là kim loại chung cho Al và Mg với hóa trị n
Sơ dồ phản ứng :
M ⏟ 10 , 2 gam + H 2 S O 4 ( l o ã n g , d ư ) → M 2 ( S O 4 ) n ⏟ m u ố i + H 2 ↑ ⏟ 0 , 5 m o l
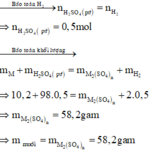

Bảo toàn nguyên tố: \(n_{H_2SO_4}=n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{H_2}=0,5\cdot2=1\left(g\right)\\m_{H_2SO_4}=0,5\cdot98=49\left(g\right)\end{matrix}\right.\)
Bảo toàn khối lượng: \(m_{muối}=m_{KL}+m_{H_2SO_4}-m_{H_2}=68,2\left(g\right)\)

\(n_{H_2}=\dfrac{0,784}{22,4}=0,035\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Zn}=b\left(mol\right)\end{matrix}\right.\)
PTHH:
Fe + H2SO4 ---> FeSO4 + H2
a------------------------------>a
Zn + H2SO4 ---> ZnSO4 + H2
b---------------------------->b
\(\Rightarrow\left\{{}\begin{matrix}56a+65b=2,14\\a+b=0,035\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,015\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\)
PTHH:
2Fe + 6H2SO4(đ, n) ---> Fe2(SO4)3 + 3SO2 + 6H2O
0,015--------------------------------------->0,0225
Zn + 2H2SO4(đ, n) ---> ZnSO4 + SO2 + 2H2O
0,02---------------------------------->0,02
=> VSO2 = (0,0225 + 0,02).22,4 = 0,952 (l)

\(a) Zn + H_2SO_4 \to ZnSO_4 + H_2\\ ZnO + H_2SO_4 \to ZnSO_4 + H_2O\\ n_{Zn} = n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)\\ \%m_{Zn} = \dfrac{0,2.65}{17,05}.100\% = 76,25\%\\ \%m_{ZnO} = 100\% -76,25\% = 23,75\%\\ b) n_{Ba(NO_3)_2}= 0,2.1,5 = 0,3(mol)\ ; n_{ZnO} = \dfrac{17,05-0,2.65}{81} = 0,05(mol)\\ n_{ZnSO_4} = n_{Zn} + n_{ZnO} = 0,25(mol)\\ ZnSO_4 + Ba(NO_3)_2 \to BaSO_4 + Zn(NO_3)_2\\ n_{ZnSO_4} < n_{Ba(NO_3)_2} \to Ba(NO_3)_2\ dư\\ \)
\(n_{BaSO_4} = n_{ZnSO_4} = 0,25(mol)\\ m_{BaSO_4} = 0,25.233 = 58,25(gam)\)
Gọi số mol Al là x; Zn là y.
\(\Rightarrow27x+65y=2,49\)
Gọi số mol Al là x; Zn là y.
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Ta có:
\(n_{H2}=\frac{3}{2}n_{Al}+n_{Zn}=1,5x+y=\frac{1,344}{22,4}=0,0\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,02\\y=0,03\end{matrix}\right.\)
\(\Rightarrow m_{Al}=0,02.27=0,54\left(g\right)\)
\(\Rightarrow\%m_{Al}=\frac{0,54}{2,49}=21,49\%\Rightarrow\%m_{Zn}=78,31\%\)
\(n_{H2SO4}=n_{H2}=0,06\left(mol\right)\)
BTKL:
\(m_{kl}+m_{H2SO4}=m_{muoi}+m_{H2}\)
\(\Rightarrow m_{muoi}=2,49+0,06.98-0,06.2=8,25\left(g\right)\)
Cho hỗn hợp trên tác dụng với H2SO4 đặc nguội thì Al bị thụ động hóa, chỉ có Zn phản ứng.
\(Zn+H_2SO_{4\left(đac\right)}\rightarrow ZnSO_4+SO_2+2H_2O\)
\(\Rightarrow n_{SO2}=n_{Zn}=0,03\left(mol\right)\)
\(\Rightarrow V_{SO2}=0,03.22,4=0,672\left(l\right)\)
a) \(n_{H2}=\frac{1,344}{22,4}=0,06\left(mol\right)\)
\(2Al+3H2SO4-->Al2\left(SO4\right)3+3H2\)
x-----------------------------------------------1,5x(mol)
\(Zn+H2SO4-->ZnSO4+H2\)
y-------------------------------------------y(mol)
Theo bài ta có hpt
\(\left\{{}\begin{matrix}27x+65y=2,49\\1,5x+y=0,06\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,02\\y=0,03\end{matrix}\right.\)
\(\%m_{Al}=\frac{0,02.27}{2,49}.100\%=21,69\%\)
\(\%m_{Zn}=100-21,69=78,31\%\)
b) \(m_{muối}=m_{Al2\left(SO4\right)3}+m_{ZnSO4}=0,02.400+0,03.161=12,83\left(g\right)\)
c)\(2Al+6H2SO4-->Al2\left(SO4\right)3+6H2O+3SO2\)
0,02----------------------------------------------------------0,03(mol)
\(Zn+2H2SO4-->ZnSO4+2H2O+SO2\)
0,03------------------------------------------------------0,03(mol)
\(\sum n_{SO2}=0,03+0,03=0,06\left(mol\right)\)
\(V_{SO2}=0,06.22,4=1,344\left(l\right)\)