


![]()
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



![]()

Đáp án C
Sơ đồ quá trình:
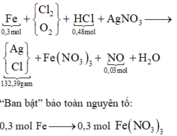
Bảo toàn nguyên tố N có 0,93 mol AgNO3 → 132,39 gam kết tủa gồm 0,93 mol Ag + 0,9 mol Cl
→ Theo bảo toàn nguyên tố Cl ta có n Cl 2 = 0,21 mol
Tiếp tục, bảo toàn H có 0,24 mol H2O sau đó bảo toàn nguyên tố O ta có n O 2 =0,09 mol
Theo đó, giá trị của V = (0,21 + 0,09) ×22,4 = 6,720 lít

Đáp án C
Cho m gam hỗn hợp rắn gồm Fe, Fe(NO3)2 vào dung dịch chứa 0,08 mol Cu(NO3)2, 0,02 mol Fe(NO3)3 và HCl thu được dung dịch X và hỗn hợp hai khí không màu, có một khí hóa nâu trong không khí là NO
Ta có: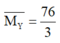 nên khí còn lại là H2 và tỉ lệ số mol NO: H2 là 5:1.
nên khí còn lại là H2 và tỉ lệ số mol NO: H2 là 5:1.
Cho AgNO3 dư vào dung dịch X thấy thoát ra 0,045 mol khí NO nên H+ dư trong X là 0,18 mol, do vậy X không chứa NO3-.
Mặt khác vì còn lại rắn không tan nên trong X chỉ chứa Fe2+ nên X chứa HCl dư và FeCl2.
Do còn H+ dư nên Fe hết ® rắn còn lại là Cu 0,08 mol
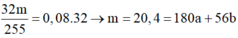
Gọi số mol Fe(NO3)2 là a mol; Fe là b mol và HCl là c mol
Bảo toàn N:![]()
![]()
Bảo toàn H:![]()
![]()
Bảo toàn nguyên tố Fe: ![]()
Giải hệ: a=0,04; b=0,6; c=1,5
Bảo toàn Cl:![]()
Bảo toàn e: ![]()
![]()
![]()

Đáp án A
![]()
Sau phản ứng còn lại 0,2m gam chất rắn.
=>kim loại dư
=> n H 2 O = 0,8 ÷ 2 = 0,4 mol; n N O = 0,8 ÷ 4 = 0,2 mol
Bảo toàn khối lượng:
m + 0,4.63 + 0,2.98 = 0,2m + 50 + 0,4.18 + 0,2.30
=> m = 23(g)
=> chọn A