Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{SO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ n_{K_2SO_3}=\dfrac{7,9}{158}=0,05\left(mol\right)\)
PTHH:
2KOH + SO2 ---> K2SO3 + H2O
0,1 0,05 0,05
\(\rightarrow n_{SO_2\left(\text{tạo muối axit}\right)}=0,15-0,05=0,1\left(mol\right)\)
KOH + SO2 ---> KHSO3
0,1 0,1
\(\rightarrow C_{M\left(KOH\right)}=\dfrac{0,1+0,1}{0,1}=2M\)

\(n_{CaO}=\dfrac{2,8}{56}=0,2\left(mol\right)\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
0,2 0,2
a. \(n_{CO_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,075 0,075
vì \(\dfrac{0,075}{1}< \dfrac{0,2}{1}\) => dd \(Ca\left(OH\right)_2\) dư sau pứ.
=> \(m_{CaCO_3}=0,075.100=7,5\left(g\right)\)
b. \(n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
Thấy: \(n_{CaCO_3}< n_{Ca\left(OH\right)_2}\)
Nên ta có 2 trường hợp.
TH 1: \(dd.Ca\left(OH\right)_2.dư\)
Có:
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,1 0,1
m muối tạo thành là m kt = 1 (g)
\(V_{CO_2}=0,1.22,4=2,24\left(l\right)\)
TH 2: khí \(CO_2\) dư
Có:
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,2 0,2 0,2
\(CO_2+CaCO_3+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
0,1 0,1 0,1
\(m_{muối}=m_{CaCO_3}+m_{Ca\left(HCO_3\right)_2}=1+0,1.162=17,2\left(g\right)\)
\(V_{CO_2}=0,3.22,4=6,72\left(l\right)\)

\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(n_{CaO}=n_{Ca\left(OH\right)_2}=\dfrac{3,36}{56}=0,06\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{1,2}{100}=0,012\left(mol\right)\)
TH1: CO2 hết, Ca(OH)2 dư
PTHH: Ca(OH)2 + CO2 -----> CaCO3 + H2O
0,012 -> 0,012 mol
=> VCO2 = 0,012 . 22,4 = 0,27 (l)
TH2: CO2 dư
PTHH: Ca(OH)2 + CO2 -> CaCO3 + H2O
0,06 ..............0,06......0,06
CO2 + CaCO3 + H2O -> Ca(HCO3)2
0,048<--(0,06 - 0,012)
=> nCO2 = 0,06 + 0,048 = 0,108 mol
=> VCO2 = 0,108 . 22,4 = 2,42 (l)

ý a là biết a=0,06 rồi biết b=6,975 à em? Mà a,b ở đâu vậy em?

Gọi $n_{NaHSO_3} = a(mol) ; n_{Na_2SO_3} = b(mol)$
$\Rightarrow 104a + 126b = 23(1)$
$NaOH + SO_2 \to NaHSO_3$
$2NaOH + SO_2 \to Na_2SO_3 + H_2O$
$n_{SO_2} = a + b = \dfrac{4,48}{22,4} = 0,2(2)$
Từ (1)(2) suy ra a = b = 0,1
$n_{NaOH} = a + 2b = 0,3(mol)$
$m = 0,3.40 = 12(gam)$

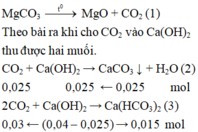
C a H C O 3 2 + 2 N a O H d ư → C a C O 3 ↓ + N a 2 C O 3 + 2 H 2 O ( 4 ) 0 , 015 → 0 , 015 m o l
Đáp án A

Sửa đề : 500 ml dung dịch Ca(OH)2 0,1M . Nếu là 0,01M thì đề sai
\(n_{Ca\left(OH\right)_2}=0,5.0,1=0,05\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{2}{100}=0,02\left(mol\right)\)
Bảo toàn nguyên tố Ca : \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}+n_{Ca\left(HCO_3\right)_2}\)
=> \(n_{Ca\left(HCO_3\right)_2}=0,05-0,02=0,03\left(mol\right)\)
Bảo toàn nguyên tố C :
=> \(n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}=0,02+0,03.2=0,08\left(mol\right)\)
=> \(V_{CO_2}=0,08.22,4=1,792\left(l\right)\)

nCO2 = 6,72 / 22,4 = 0,3 mol
Giả sử pứ tạo 2 muối \(\begin{cases}Na2CO3:xmol\\NaHCO3:ymol\end{cases}\)
CO2 + 2NaOH ===> Na2CO3 + H2O
x 2x x (mol)
CO2 + NaOH ===> NaHCO3
y y y (mol)
Theo đề bài và theo PTHH, ta có:
\(\begin{cases}x+y=0,3\\106x+84y=29,6\end{cases}\)
===> x = 0,2 mol, y = 0,1 mol
Vì x, y đều có nghiệm xác đunhj nên giả thiết trên là đúng.
=> nNaOH = 2 x 0,2 + 0,1 = 0,5 mol
=> V = 0,5 / 2 = 0,25 lít = 250 ml
Bìa này còn nhiều cách giải lắm, bạn tự tìm hiểu nha!!!![]()
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{NaOH}=0,1a\left(mol\right)\)
Xét TH1: Tạo muối trung hoà
\(n_{Na_2CO_3}=\dfrac{9,5}{106}=\dfrac{19}{212}\left(mol\right)\)
PTHH: 2NaOH + CO2 ---> Na2CO3 + H2O
0,1--------->0,1
So sánh: \(0,1\ne0,\dfrac{19}{212}\rightarrow\) Loại TH1
Xét TH2: Tạo muối axit
\(n_{NaHCO_3}=\dfrac{9,5}{84}=\dfrac{19}{168}\left(mol\right)\)
PTHH: NaOH + CO2 ---> NaHCO3
0,1-------->0,1
So sánh: \(0,1\ne\dfrac{19}{168}\rightarrow\) Loại TH2
Xét TH3: Tạo cả hai muối
Gọi \(\left\{{}\begin{matrix}n_{Na_2CO_3}=x\left(mol\right)\\n_{NaHCO_3}=y\left(mol\right)\end{matrix}\right.\)
PTHH:
2NaOH + CO2 ---> Na2CO3 + H2O
2x x x
NaOH + CO2 ---> NaHCO3
y y y
Hệ pt \(\left\{{}\begin{matrix}x+y=0,1\\106x+84y=9,5\end{matrix}\right.\Leftrightarrow x=y=0,05\left(mol\right)\)
\(\rightarrow C_{M\left(NaOH\right)}=\dfrac{0,05.2+0,05}{0,1}=1,5M\)