Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C.
(a) Sai, Độ dẫn điện của Al kém hơn Cu.
(c) Sai, Cho dung dịch Ba(OH)2 dư vào dung dịch Al2(SO4)3, sau phản ứng thu được kết tủa BaSO4.
(d) Sai, Các kim loại kiềm thổ khử nước ở nhiệt độ thường (trừ Be).

Chọn C.
(a) Sai, Độ dẫn điện của Al kém hơn Cu.
(c) Sai, Cho dung dịch Ba(OH)2 dư vào dung dịch Al2(SO4)3, sau phản ứng thu được kết tủa BaSO4.
(d) Sai, Các kim loại kiềm thổ khử nước ở nhiệt độ thường (trừ Be).

Chọn C
Y tác dụng với NaOH dư Þ Al nếu có sẽ bị tan hết Þ 2 oxit kim loại trong T là Fe2O3 và CuO.

Chọn A.
(a) Đúng, Hai kết tủa thu được là AgCl và Ag.
(b) Đúng, Cu tác dụng với dung dịch chứa H+, NO3–.
(c) Sai, Hỗn hợp Cu, Fe3O4 không tan trong nước.
(d) Sai, Cu + 2FeCl3 ® CuCl2 + 2FeCl2 (và FeCl3 còn dư) Þ Sau pư thu được 3 muối.
(e) Đúng, Al + OH- + H2O ® AlO2– + 3/2H2 (ứng với 2 mol Al hoà tan hết 2 mol NaOH).
(f) Sai, Kết tủa thu được là BaSO4 (không có Al(OH)3 vì bị tan trong kiềm dư).
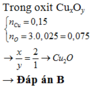


Đáp án : A
Gọi CT oxit là : R2O
Giả sử có x mol Al và y mol R2O
, nHCl = 0,65 mol ; nAl(OH)3 = 0,05mol
Nếu Al dư => Trong dung dịch chỉ có 2y mol RAlO2
Do nHCl > nAl(OH)3 => kết tủa tan 1 phần
=> nH+= 4nAlO2 – 3nAl(OH)3 => nAlO2 = 2y = 0,2 => y = 0,1 mol
=> nH2 = 0,3 mol và nAl pứ = 0,2 mol
=> mtăng = mR2O + mAl pứ - mH2
=> mR2O = 9,4g và nR2O = 0,1 mol
=> M oxit = 94 => R = 39 (Kali)
TH : Al hết sẽ không thỏa mãn