Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

dùng bảo toàn nguyên tố nha cậu
xong tính khối lượng muối = khối lượng kim loại+ khối lượng gốc axit
1.
nh+ =0,8 *2 =1,6 suy ra nhcl =ncl- =1,6 suy ra m = 12 +1,6 * 35,5 =68,8
2.
nh+ =1,4 * 10-3
gọi nhcl = 2x nh2so4 = x
áp dụng định luận bảo toàn nguyên tố ta có: 2x+x = 1,4*10-3 suy ra x=0,005
suy ra m = 18,2 + 0,005 *2 *35,5 +0,005*96 = 19,035
CHÚC BẠN THÀNH CÔNG

nHNO3pu= 0,87 mol
Đặt số mol N2 là x mol; số mol N2O là y mol
→x+y=0,06
mhỗn hợp= 28x+44y= 0,06.20,667.2=2,48 gam
Giải hệ trên được x=0,01 ; y= 0,05
2NO3-+ 8e+ 10H+ → N2O + 5H2O (1)
0,4 0,5 ← 0,05 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (2)
0,12← 0,01
Theo PT (1), (2): nH+= 0,5+0,12= 0,62 mol= nHNO3
Mà đề cho nHNO3pu= 0,87 mol
→Có phản ứng tiếp :
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (3)
0,2 0,25 0,025 mol
nH+ pứ 3= 0,87- 0,62= 0,25 mol
bảo toàn nguyên tố H: nH (HNO3)= nH(NH4NO3)+ nH(H2O)
→0,87= 0,025.4+ 2.nH2O→ nH2O=0,385 mol
Áp dụng định luật bảo toàn khối lượng:
mkim loại+ mHNO3= m +mkhí+ mH2O
↔ 9,55+ 0,87.63=m+2,48 + 0,385.18 → m=54,95 gam
Đáp án A

Đáp án D
Hỗn hợp gồm: Mg ( a mol) ; Cu(NO3)2 ( 0,25 mol)
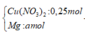
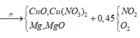
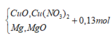
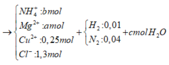
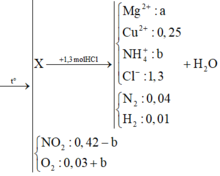
Vì H2 sinh ra nên không còn NO3− trong muối
Bảo toàn điện tích trong dung dịch → 2a + b + 0,25 .2 = 1,3 → 2a + b = 0,8 (1)
Bảo toàn mol H: 1,3 = 4b + 0,01 . 2 + 2c → 4b + 2c = 1,28 (2)
Bảo toàn O:
→ a = 0,39 ; b = 0,02 , c = 0,6
Vậymmuoi = 24.0,39 + 18.0,02 + 64.0,25 + 35,5.1,3 = 71,87 g
→ a = 0,39 ; b = 0,02 , c = 0,6
Vậy mmuoi = 24.0,39 + 18.0,02 + 64.0,25 + 35,5.1,3 = 71,87 gam

Giả sử số mol Mg là x\(\Rightarrow n_{Al}=1,25x\)(mol)
\(\Rightarrow24x+27\cdot1,25x=23,1\Rightarrow x=0,4\)
Gọi số mol của N2O và H2 là a và b(mol).
Ta có: \(\left\{{}\begin{matrix}a+b=\dfrac{6,72}{22,4}=0,3\\44a+2b=11,5\cdot2\cdot0,3\end{matrix}\right.\)\(\Rightarrow\left\{{}\begin{matrix}a=0,15mol\\b=0,15mol\end{matrix}\right.\)
BTe ta thấy: \(2n_{Mg}+3n_{Al}>8n_{N_2O}+2n_{H_2\Rightarrow}\)dd chứa \(NH^+_4\)
\(\Rightarrow8n_{NH^+_4}=2n_{Mg}+3n_{Al}-8n_{N_2O}-2n_{H_2}\Rightarrow n_{NH^+_4}=0,0625mol\)
Do sinh khí H2 nên toàn bộ lượng NO-3 bị chuyển hóa thành N2O và NH+4.
\(\Rightarrow n_{NaNO_3}=0,15\cdot2+0,0625=0,3625mol\left(BTN\right)\)
\(n_{HSO^-_4}=2n_{H_2}+10n_{N_2O}+10n_{NH^+_4}=2,425mol\)
Dung dịch X chứa:
\(Mg^{2+}:0,4mol\)
\(Al^{3+}:0,5mol\)
\(Na^+:0,3625mol\) \(\Rightarrow m=255,3625\left(g\right)\)
\(SO^{2-}_4:2,425mol\)
\(NH^+_4:0,0625mol\)

Đáp án D
nD = 0,45 => nO(D) = 0,9 mol
nY = 0,05 mol
Đặt nN2 = x => nH2 = 0,05 – x
=> 28x + 2(0,05 – x) = 0,05.11,4.2 = 1,14
=> x = 0,04 mol
=> nN2 = 0,04 mol và nH2 = 0,01 mol
Trong Y chứa khí H2 chứng tỏ NO3- hết
Hỗn hợp muối clorua gồm : a mol MgCl2 ; 0,25 mol CuCl2 ; NH4Cl
Bảo toàn Clo : nNH4Cl = 1,3 – 2a – 0,5 = 0,8 – 2a
Bảo toàn H : nH2 = ½ (nHCl + 4nNH4Cl – 2nH2) = 4a – 0,96
Bảo toàn O : nO (Cu(NO3)2) = nO(D) + nO(H2O) => 0,25.6 = 0,9 + 4a – 0,96
=> a = 0,39 mol
=> m = 0,39.95 + 0,25.135 + (0,8 – 2.0,39). 53,5 = 71,87g
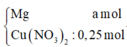
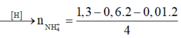
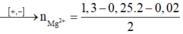

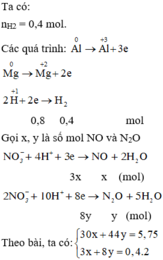

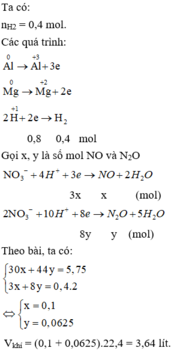
nh + =1,4 . 10-3
Gọi nhcl = 2x nh2so4 = x
Áp dụng định luật bảo toàn nguyên tố ta có:2x + x =1,4 .103 => x= 0,005
=> m = 18,2 + 0,005 . 2 . 35,5 + 0,005 . 96 = 19,035
camon ạ :33