Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Gọi n N O = a n N O 2 = b
Có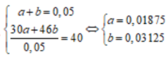
Vậy
m m u ố i = m k i m l o ạ i + m N O 3 -
=1 1,35+62.0,0875 = 6,775 (gam)

Gọi \(n_{NO} = a ; n_{NO_2} = b\)
Ta có :
\(a + b = \dfrac{896}{1000.22,4} = 0,04\\ 30a + 46b = 0,04.42\)
Suy ra a = 0,01 ; b = 0,03
Giả sử không có muối amoni tạo thành.
\(n_{NO_3^-} = n_{e\ trao\ đổi} = 3n_{NO} + n_{NO_2} = 0,06(mol)\)
\(m_{muối} = m_{kim\ loại} + m_{NO_3^-} = 1,35 + 0,06.62 = 5,07(gam)\)

Đặt x, y, z lần lượt là số mol Cu, Mg, Al.
Quá trình nhường e :
Cu → Cu 2 + + 2e
x → x → 2x
Mg → Mg 2 + + 2e
y → y → 2y
Al → Al 3 + + 3e
z → z → 3z
Quá trình thu e :
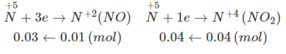
Ta có : 2x + 2y + 3z = 0,03 + 0,04 = 0,07 và 0,07 cũng chính là số mol NO 3 - tạo muối.
Khối lượng muối nitrat là : 1,35 + 62 × 0,07 = 5,69 (gam).

1) Gọi x, y là số mol Mg và Zn có trong hh kim loại:
m(hh KL) = m(Mg) + m(Zn) = 24x + 65y = 8,9g [1]
Số mol các sản phẩm khử tạo thành:
n(SO2) = 1,12/22,4 = 0,05mol; n(S) = 1,6/32 = 0,05mol
Quá trình oxy hóa:
Mg → Mg+2 + 2e
x x 2x
Zn → Zn+2 + 2e
y y 2y
Số mol e nhường: n(e nhường) = 2x + 2y mol
Quá trình khử:
2e + S+6 → S+4
0,1 0,05
6e + S+6 → S
0,3 0,05
số mol e nhận: n(e nhận) = 0,1 + 0,3 = 0,4mol
Theo ĐL bảo toàn e: n(e nhường) = n(e nhận) → 2x + 2y = 0,5mol [2]
Giải hệ PT [1], [2] ta được: x = 0,1mol và y = 0,1mol
Khối lượng mỗi muối thu được:
m(MgSO4) = 120.0,1 = 12g
m(ZnSO4) = 161.0,1 = 16,1g

\(n_k=0,6mol\)
\(d_k=d_{H_2}=26\Rightarrow d_k=52\)
Áp dụng sơ đồ đường chéo tính được là: \(n_{SO_2}=0,2mol;n_{NO_2}=0,4mol\)
Bảo toàn e: \(5^{+6}+2e\rightarrow S^{+4}\)
mol: \(0,4\rightarrow0,2\)
\(N^{+5}+1e\rightarrow N^{+4}\)
mol: \(0,4\rightarrow0,4\)
\(m_{\text{muối}}=m_{kl}+m_{SO_4^{2^-}}+m_{NO_3^-}=55,8g\)

Gọi nZn = x , nCu = y (mol)
=> 65x+64y = 12,9 (1)
nkhí = \(\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
dk/H2 = 19 => Mkhí = 38
NO 30 8 1
38
NO2 46 8 1
=> \(\dfrac{nNO}{nNO_2}=1:1\)
=> nNO = 0,1(mol) , nNO2 = 0,1 (mol)
Zn => Zn+2 + 2e x 2x | N+5 + 3e => N+2 0,3 0,1 |
Cu => Cu+2 + 2e y 2y | N+5 + 1e => N+4 0,1 0,1 |
=> 2x + 2y = 0,4 (mol) (2)
Từ 1 + 2 => x = 0,1, y = 0,1 (mol)
=> mCu = 6,4g
mZn = 6,5g

nSO2 = \(\dfrac{2,8}{22,4}\)=0,125 mol
S+6 + 2e → S+4
0,25<-----0,125
=> Số mol e do 3,35 gam hỗn hợp kim loại nhường là 0,25 mol.
Xét phản ứng với Clo
Kim loại + Cl2 → Muối clorua
Có 3,35 gam kim loại phản ứng nên số mol e kim loại nhường cũng là 0,25 mol
Cl20 + 2e → 2Cl-1
0,25 --> 0,25
=> nCl-1 trong muối clorua = 0,25 mol
<=> mCl-1 = 0,25.35,5 = 8,875 gam.
mMuối = mKim loại + mCl-1 = 3,35 + 8,875 = 12,225 gam.
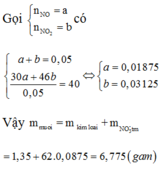

nNO = a; nNO2 = b.
Ta có: a+b = 0,0530a + 46b = 0,05.42,8 = 2,14
\(\Rightarrow\) a= 0,01; b=0,04
mMuối= mKL + mNO3= 1,35 + 62( 0,01.3+0,04) = 5,69 gam
Ta dễ dàng tính được nNO = 0,01 mol; nNO2 = 0,04 mol
m muối = mKL + 62( 3nNO + nNO2)
= 1,35 + 62( 3. 0,01 + 0,04)
= 5,69 (g)