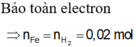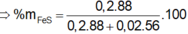Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n O = 10.24%/16 = 0,15(mol)
Quy đổi X gồm n Fe = a(mol) ; n S = b(mol) ; n O = 0,15(mol)
=> 56a + 32b + 0,15.16 = 10(1)
n SO2 = 1,68/22,4 = 0,075(mol)
Bảo toàn electron :
3a + 6b = 0,15.2 + 0,075.2(2)
Từ (1)(2) suy ra a = 0,13 ; b = 0,01
Gọi n O2 = n O3 = x(mol)
Bảo toàn electron :
4n O2 + 6n O3 + 2n O = 3n Fe + 4n S
<=> 4x + 6x + 0,15.2 = 0,13.3 + 0,01.4
<=> x = 0,013
=> V = (0,013 + 0,013).22,4 = 0,5824 lít

thu được dung dịch Y chứa một chất tan và khí NO ấy. mình ghi thiếu

Đáp án B
nSO2 = 1,7 (mol)
Chất rắn Z là Fe2O3, nFe2O3 = 0,4 (mol)
2Febđ → Fe2O3
0,8 ← 0,4 (mol)
Ta có: mX = 1,7 ×64 – 48=60,8 (gam)
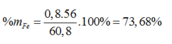

a, Gọi \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Zn}=b\left(mol\right)\end{matrix}\right.\left(đk:a,b>0\right)\)
\(n_{H_2}=\dfrac{7,28}{22,4}=0,35\left(mol\right)\)
PTHH:
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
a--------------------------------------->1,5a
Zn + H2SO4 ---> ZnSO4 + H2
b------------------------------>b
Theo bài ra, ta có hệ: \(\left\{{}\begin{matrix}27a+65b=10,55\\1,5a+b=0,35\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=0,15\left(mol\right)\\b=0,1\left(mol\right)\end{matrix}\right.\left(TM\right)\)
\(\rightarrow\left\{{}\begin{matrix}m_{Al}=0,15.27=4,05\left(g\right)\\m_{Fe}=0,1.56=5,6\left(g\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{4,05}{10,55}.100\%=38,4\%\\\%m_{Zn}=100\%-38,4\%=61,6\%\end{matrix}\right.\)
b, PTHH:
\(Zn+2H_2SO_{4\left(đặc,nguội\right)}\rightarrow ZnSO_4+SO_2\uparrow+2H_2O\)
0,1------------------------------>0,1----->0,1
\(2Al+3ZnSO_4\rightarrow Al_2\left(SO_4\right)_3+3Zn\downarrow\)
\(\dfrac{1}{15}\)<---0,1---------->\(\dfrac{1}{30}\)---------->0,1
\(Zn+2H_2SO_{4\left(đặc,nguội\right)}\rightarrow ZnSO_4+SO_2\uparrow+2H_2O\)
0,1----------------------------->0,1-------->0,1
\(\rightarrow\left\{{}\begin{matrix}V=\left(0,1+0,1\right).22,4=4,48\left(l\right)\\x=\dfrac{1}{30}.342+0,1.161=27,5\left(g\right)\end{matrix}\right.\)
\(a.Đặt:\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Zn}=y\left(mol\right)\end{matrix}\right.\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ \Rightarrow\left\{{}\begin{matrix}27x+65y=10,55\left(g\right)\\\dfrac{3}{2}x+y=\dfrac{7,28}{22,4}=0,325\left(mol\right)\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,15\\y=0,1\end{matrix}\right.\\ \%m_{Al}=\dfrac{0,15.27}{10,55}.100=38,39\%;\%m_{Zn}=61,61\%\\ b.X+H_2SO_4đặc,nguội\Rightarrow ChỉcóZnphảnứng\\ Zn\rightarrow Zn^{2+}+2e\\ S^{+6}+2e\rightarrow S^{+4}\\ Bảotoàne:n_{Zn}.2=n_{SO_2}.2\\ \Rightarrow n_{SO_2}=0,1\left(mol\right)\\ \Rightarrow V_{SO_2}=0,1.22,4=2,24\left(l\right)\\ n_{ZnSO_4}=n_{Zn}=0,1\left(mol\right)\\ \Rightarrow m_{ZnSO_4}=161.0,1=16,1\left(g\right)\)
Lưu ý: Al bị thụ động với H2SO4 dặc nguội

a) n Fe = a(mol) ; n Cu = b(mol)
=> 56a + 64b = 4,8(1)
n SO2 = 2,24/22,4 = 0,1(mol)
Bảo toàn e :
3n Fe + 2n Cu = 2n SO2
<=> 3a + 2b = 0,2(2)
Từ (1)(2) suy ra a = b = 0,04
%m Fe = 0,04.56/4,8 .100% = 46,67%
%m Cu = 100% -46,67% = 53,33%
b)
n KOH = 0,15
Ta có :
1 < n KOH / n SO2 = 0,15/0,1 = 1,5 < 2 nên muối sinh ra là Na2SO3(x mol) và NaHSO3(y mol)
2NaOH + SO2 $\to$ Na2SO3 + H2O
NaOH + SO2 $\to$ NaHSO3
Theo PTHH :
n SO2 = a + b = 0,1
n NaOH = 2a + b = 0,15
Suy ra a= 0,05 ; b = 0,05
m muối = 0,05.126 + 0,05.104 = 11,5 gam
Bài 2 :
- Gọi số mol Fe và Cu lần lượt là a, b mol
Ta có : mhh = mFe + mCu = 56a + 64b = 4,8
Bte : 3a + 2b = 0,2
=> a = b =0,04mol
a, Ta có : mFe =n.M = 2,24g ( 46,7% )
=> %Cu = 53,3%
b, Ta thấy sau phản ứng thu được K+, SO3-2 xmol, HSO3- y mol
BtS : x + y = 0,1
BTĐT : 2x + y = 0,15
=> x =y = 0,05 mol
=> mM = mK2SO3 + mKHSO3 = 13,9g

`2Fe + 6H_2 SO_[4(đ,n)] -> Fe_2(SO_4)_3 + 6H_2 O + 3SO_2 \uparrow`
`0,1` `0,15` `(mol)`
`2Ag + 2H_2 SO_[4(đ,n)] -> Ag_2 SO_4 + 2H_2 O + SO_2 \uparrow`
`0,2` `0,1` `(mol)`
`n_[SO_2]=[5,6]/[22,4]=0,25(mol)`
Gọi `n_[Fe]=x` ; `n_[Ag]=y`
`=>` $\left[\begin{matrix} 56x+108y=27,2\\ \dfrac{3}{2}x+\dfrac{1}{2}y=0,25\end{matrix}\right.$
`<=>` $\left[\begin{matrix} x=0,1\\ y=0,2\end{matrix}\right.$
`a)%m_[Fe]=[0,1.56]/[27,2] .100~~20,59%`
`=>%m_[Ag]~~100-20,59~~79,41%`
`b)n_[SO_2]=0,15+0,1=0,25(mol)`
`n_[NaOH]=0,5.0,8=0,4(mol)`
Ta có:`T=[0,4]/[0,25]=1,6 ->` Tạo muối `Na_2 SO_3` và `NaHSO_3`
`SO_2 + 2NaOH -> Na_2 SO_3 + H_2 O`
`SO_2 + NaOH -> NaHSO_3`
Gọi `n_[Na_2 SO_3]=x ; n_[NaHSO_3]=y`
`=>` $\left[\begin{matrix} x+y=0,25\\ 2x+y=0,4\end{matrix}\right.$
`<=>` $\left[\begin{matrix} x=0,15\\ y=0,1\end{matrix}\right.$
`=>C_[M_[Na_2 SO_3]]=[0,15]/[0,5]=0,3(M)`
`=>C_[M_[NaHSO_3]]=[0,1]/[0,5]=0,2(M)`
Lần sau chú ý dùng dấu \(\left\{{}\begin{matrix}\\\end{matrix}\right.\) ha, dấu \(\left[{}\begin{matrix}\\\end{matrix}\right.\) có ý nghĩa là xảy ra một trong các trường hợp còn dấu \(\left\{{}\begin{matrix}\\\end{matrix}\right.\) có ý nghĩa là đồng thời xảy ra