Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích: Đáp án A
nAg = 0,03 mol. Andehit no đơn chức mạch hở và không chứa HCHO nên
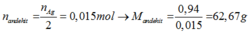
Vậy 2 andehit là C2H5CHOvà C3H7CHO

Đáp án C
TH1: X có HCHO a mol, nên anđehit còn lại là CH3CHO b mol.
BTNT cho H nên n(H2O)=a+2b=0,16(1)
Sơ đồ phản ứng tráng bạc :
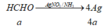
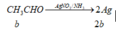
n(Ag)=4a+2b= 0,12(2) TH này không TM vì nghiệm âm
TH2: X không chứa HCHO, gọi CT chung của hai anđehit là
Sơ đồ phản ứng tráng bạc:
![]()
BTNT cho H ta có n(H2O) = 0,06.![]() hai anđehit là CH3CHO x mol và C2H5OH y mol.
hai anđehit là CH3CHO x mol và C2H5OH y mol.
x+y=0,06 (3) BTNT cho H ta có n(H2O)=2x+3y=0,16
Giải hệ ta có :x=0,02 và y=0,04 suy ra m(C2H5CHO)=58.0,04=2,32 gam

Ta có: n↓=0,8(mol)
TH1: Không có HCHO , khi đó: nX=0,4(mol)→ loại
TH2: 2 anđehit là HCHO và CH3CHO
\(\left\{{}\begin{matrix}30n_{HCHO}+44_{nCH_3CHO}=8,9\\4n_{HCHO}+2n_{CH_3CHO}=0,8\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{HCHO}=0,15\\n_{CH_3CHO}=0,1\end{matrix}\right.\)

Đáp án C
+) Cách 1: thử các đáp án bằng cách lập hệ 2 phương trình với ẩn là số mol của mỗi anđehit
Ví dụ: Xét đáp án A:
G ọ i n H C H O = x ( m o l ) ; n C H 3 C H O = y ( m o l ) ⇒ 30 x + 44 y = 1 , 02 4 x + 2 y = n A g = 0 , 04
Khi giải hệ ta sẽ thấy sẽ có nghiệm âm do đó không thỏa mãn.
Tương tự như trên ta thử các đáp án còn lại nếu thu được 2 nghiệm x và y đều lớn hơn 0 thì đó là đáp án đúng.
Cách này không cần suy nghĩ nhiều và ta có máy tính để giải hệ nên trong trường hợp thiếu thời gian ta nên làm theo cách này.
+) Cách 2: Ta xét 2 trường hợp.
- TH1: X và Y là CH3CHO (do kế tỉếp nhau)
Ta giải hệ và tìm ra số mol của từng chất. Tương tự như ví dụ trên ta thấy không thỏa mãn.
- TH2 : X và Y đều không phải HCHO
⇒ n a n d e h i t = 1 2 n A g = 0 , 02 ( m o l ) ⇒ M ¯ a n d e h i t = 1 , 02 0 , 02 = 52
=> anđehit là CH3CHO và C2H5CHO
Nhận xét: Đây là bài toán không khó nhưng ta phải chú ý xét trường hợp nếu một trong hai chất là HCHO.

Đáp án C
0,5 mol X cho ra 0,4 mol Ag nên trong X có 1 este là HCOOR
HCOOR + AgNO3 → 2Ag ||⇒ nHCOOR = 0,4 ÷ 2 = 0,2 mol.
Mặt khác khi thủy phân X trong KOH cho hỗn hợp hai muối của 2 axit đồng đẳng kế tiếp nên este còn lại là CH3COOR
⇒ nCH3COOR1 = 0,5 – 0,2 = 0,3 mol.
Gọi nHCOOR = nCH3COOR1.2a = 3a.
HCOOR + KOH → HCOONa + ROH.
CH3COOR1 + KOH → CH3COOK + R1OH.
Bảo toàn khối lượng: mX + mKOH = mMuối + mAncol
14,08 + (0,2a+0,3a)×56 = 0,2a.MHCONa + 0,3a.MCH3COONa + 8,256
⇒ a = 0,32 mol ||⇒ nAncol = (0,3+0,2)×0,32 = 0,16 mol
⇒ MAncol = 8,256÷0,16 = 51,6 (Vì 46 < 51,6 < 60).
⇒ 2 ancol đó là C2H5OH và C3H7OH

Giải thích: Đáp án B
Trường hợp 1: Có HCHO loại
Trường hợp 2: Không có HCHO
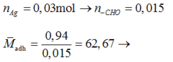
CTPT của hai anđehit là C3H6Ovà C4H8O

Đáp án B
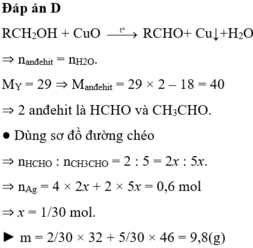
► Xét 1 phần ⇒ mhỗn hợp anđehit = 20,8 ÷ 2 = 10,4(g).
GIẢ SỬ không chứa HCHO ⇒ nhỗn hợp = nAg ÷ 2 = 0,5 mol.
⇒ Mtrung bình hỗn hợp = 10,4 ÷ 0,5 = 20,8 ⇒ loại
⇒ hỗn hợp gồm HCHO và CH3CHO với số mol là 0,2 và 0,1.
► X gồm 0,2 mol CH3OH (Y) và 0,1 mol C2H5OH (Z).
Đặt hiệu suất tạo ete của Z = x ⇒ nZ phản ứng = 0,1x mol.
nY phản ứng = 0,2 × 0,5 = 0,1 mol 2 ancol → 1 ete + 1H2O.
⇒ nH2O = nancol phản ứng ÷ 2 = (0,05 + 0,05x) mol.
Bảo toàn khối lượng: 32.0,1 + 46.0,1x = 4,52 + 18.(0,05 + 0,05x)
⇒ x = 0,6 = 60%
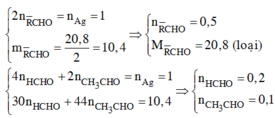
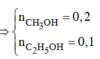
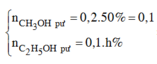
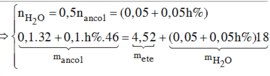
\(n_{Ag}=\dfrac{4,32}{108}=0,04\left(mol\right)\)
TH1: Hỗn hợp không có HCHO.
⇒ nCnH2nO = 0,02 (mol)
\(\Rightarrow M_{C_nH_{2n}O}=\dfrac{1,02}{0,02}=51\left(g/mol\right)\)
⇒ n = 2,5
Mà: 2 aldehyde là đồng đẳng kế tiếp.
→ C2H4O và C3H6O.
CTCT: CH3CHO và CH3CH2CHO
TH2: Hỗn hợp có HCHO.
Mà: 2 aldehyde đồng đẳng kế tiếp
→ HCHO và CH3CHO
\(\Rightarrow\left\{{}\begin{matrix}30n_{HCHO}+44n_{CH_3CHO}=1,02\\4n_{HCHO}+2n_{CH_3CHO}=0,04\end{matrix}\right.\) → số mol âm (vô lý) → loại.
TK:
Để giải bài toán này, ta cần xác định công thức cấu tạo của hai aldehyde dựa trên lượng Ag tạo thành khi phản ứng với dung dịch AgNO3/NH3.
1. Tính số mol Ag tạo thành từ 4.32g Ag:
\[ n_{Ag} = \frac{4.32 \text{ g}}{107.87 \text{ g/mol}} \approx 0.04 \text{ mol} \]
2. Theo phản ứng, mỗi mol aldehyde tạo ra một mol Ag:
\[ \text{số mol aldehyde} = 0.04 \text{ mol} \]
3. Vì aldehyde no có công thức chung là \(C_nH_{2n}O\), ta cần tìm \(n\) để biết công thức cấu tạo chính xác.
4. Xác định khối lượng mol của aldehyde từ lượng hỗn hợp:
a. Khối lượng mol của hỗn hợp aldehyde:
\[ m_{\text{hỗn hợp}} = 1.02 \text{ g} \]
\[ n_{\text{hỗn hợp}} = \frac{1.02 \text{ g}}{M_{\text{hỗn hợp}}} \]
Trong đó, \(M_{\text{hỗn hợp}}\) là khối lượng mol trung bình của aldehyde trong hỗn hợp. Vì hai aldehyde có cùng lượng mol, nên:
\[ M_{\text{hỗn hợp}} = \frac{1}{2} M_{\text{aldehyde}} \]
b. Ta cần tìm \(M_{\text{aldehyde}}\). Ta biết rằng:
\[ M_{\text{aldehyde}} = n_{\text{aldehyde}} \times (12 + 1 + 16) \]
Từ số mol của aldehyde đã tính ở bước 2, ta tính được \(M_{\text{aldehyde}}\).
c. Từ \(M_{\text{aldehyde}}\), ta tính được \(M_{\text{hỗn hợp}}\).
5. Từ \(M_{\text{hỗn hợp}}\), ta tính được \(n_{\text{hỗn hợp}}\).
6. Xác định \(n\) từ \(n_{\text{hỗn hợp}}\). Nếu \(n_{\text{hỗn hợp}}\) là số nguyên, đó chính là \(n\). Nếu không, ta cần kiểm tra các giá trị gần nhất để xác định \(n\).
7. Từ \(n\), ta biết được công thức cấu tạo của hai aldehyde.