Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$n_{Al_2O_3} = \dfrac{2,55}{102} = 0,025(mol) \Rightarrow n_{Al(OH)_3} = 0,025.2 = 0,05(mol)$
$n_{AlCl_3} = 0,1(mol)$
TH1 : $AlCl_3$ dư
$n_{NaOH} = 3n_{Al(OH)_3} = 0,05.3 = 0,15(mol) \Rightarrow C_{M_{NaOH}} = \dfrac{0,15}{0,2} = 0,75M$
TH2 : Kết tủa bị hòa tan một phần
$n_{NaOH} = 4n_{AlCl_3} - n_{Al(OH)_3} = 0,1.4 - 0,05 = 0,35(mol)$
$\Rightarrow C_{M_{NaOH}} = \dfrac{0,35}{0,2} = 1,75M$

Giải:
nAlCl3 = 0,1.1 = 0,1 (mol); nAl2O3 = = 0,025 (mol)
Có hai trường hợp:
a)NaOH thiếu.
AlCl3 + 3NaOH → Al(OH)3 ↓ + 3NaCl (1)
0,05.3 0,05 (mol)
2Al(OH)3 Al2O3 + 3H2O (2)
0,05 0,025 (mol)
=>CM (NaOH) = = 0,75 (M).
b) NaOH dư một phần.
AlCl3 + 3NaOH → Al(OH)3 ↓ + 3NaCl (1)
0,1 0,3 0,1 (mol)
Al(OH)3 + NaOH → NaAlO2 + 2H2O (2)
0,05 0,05 (mol)
2Al(OH)3 Al2O3 + 3H2O (3)
0,05 0,025 (mol)
=> nNaOH = 0,3 + 0,05 = 0,35 (mol); CM (NaOH) = = 1,75 (M).

Đặt a, b, c là số mol Al203, CuO , FeO mA = 102a + 80b + 72c = 20,3 m rắn = 102a + 64b + 56c = 17,1 nHCl = 6a + 2b + 2c = 0,7 -> a = 0,05 ; b = c = 0,1 Trong B chứa nCO2 = b + c = 0,2 nCaCO3 = 0,1 -> nCa(HCO3)2 = 0,05 -> nCa(OH)2 = 0,15 -> Vdd =105 ml

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

Cho m gam hỗn hợp X gồm ( Fe , FeO , Fe2O3 ) có tỷ lệ khối lượng tương ứng là 7:18:40 .Hỗn hợp X tan vừa hết trong 500 ml H2SO4 loãng 0,68 M thu được dung dịch B và thoát ra V lít khí H2 ( đktc). Cho dung dịch B tác dụng NaOH dư lọc kết tủa nung khô trong không khí thu được 22,4 gam chất rắn. Giá trị của V là ?
A. 0,448
B. 0,896
C. 2,24
D. 1,12

nCa2+ = nCaCO3 = nCaO = 0 . 28 56 = 0 . 005 ⇒ [Ca2+] = 0 , 005 0 , 1 = 0 , 5 M ⇒ Chọn A.

+ Tính được những gì có thể tính được
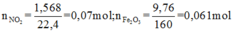
+ Với bài toán gồm nhiều giai đoạn liên tiếp nhau như thế này ta nên tóm tắt lại bài toán:
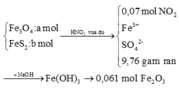
Bây giờ ta phải thiết lập được mối quan hệ giữa a và b với hi vọng là tìm được a và b rồi sau đó áp dụng các định luật bảo toàn như khối lượng, nguyên tố, electron ....
+ Bảo toàn nguyên tố Fe: 3a + b = nFe = 2.0,061 = 0,122
+ Bảo toàn sốmol electron trao đổi: a + 15b = 0,07.1 ( Chú ý FeS2→Fe3+ + 2S+6 + 15e)
Giải được a = 0,04; b = 0,002.
+ Tiếp tục sử dụng bảo toàn nguyên tố S:
![]()
+ Vì phản ứng xảy ra hoàn toàn và vừa đủ nên sau khi phản ứng với dung dịch NaOH ta chỉ thu được 2 muối là Na2SO4 và NaNO3.
Áp dụng định luật bảo toàn nguyên tố Na:
![]()
+ Cuối cùng dựa vào sơ đồ tóm tắt, ta sẽ dùng bảo toàn nguyên tố N
![]()
=>![]()
Đáp án D
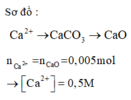
 với các chất sau:
với các chất sau:
Số mol AlCl3 là nAlCl3 = 0,1. 1 = 0,1 (mol)
Số mol Al2O3 là nAl2O3 =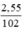 = 0,025 (mol)
= 0,025 (mol)
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl (1)
0,1(mol) 0,1(mol)
2Al(OH)3 + 2NaOH → 2NaAlO2 + 3H2O (2)
0,05(mol)
2 Al(OH)3 -to→ Al2O3 + 3H2O (3)
0,05(mol) 0,025(mol)
Theo pt(3) ta thấy nAl(OH)3 = 2. nAl2O3 = 2. 0,025 = 0,05 (mol)
Như vậy đã có: 0,1 - 0,05 = 0,05 (mol) Al(OH)3 đã bị hòa tan ở pt (2)
Từ (1) và (2) số mol NaOH = 3.0,1 + 0,05 = 0,35 (mol)
Nồng độ mol/l C(M(NaOH)) =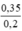 = 1,75M
= 1,75M