Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi \(\left\{{}\begin{matrix}n_{Cu}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{matrix}\right.\left(đk:a,b>0\right)\)
PTHH:
\(Cu+2H_2SO_{4\left(đặc,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\)
a------------------------------->a
\(2Fe+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
b----------------------------------->0,5b
\(2NaOH+CuSO_4\rightarrow Cu\left(OH\right)_2\downarrow+Na_2SO_4\)
a---------->a
\(6NaOH+Fe_2\left(SO_4\right)_3\rightarrow2Fe\left(OH\right)_3\downarrow+3Na_2SO_4\)
0,5b----------->a
Theo bài ra, ta có hệ: \(\left\{{}\begin{matrix}160a+400.0,5b=71,2\\98a+107b=40,2\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=0,17\left(mol\right)\\b=0,22\left(mol\right)\end{matrix}\right.\left(TM\right)\)
\(\rightarrow m=0,17.64+0,22.56=23,2\left(g\right)\)

cÂU 2.
\(n_Z=\dfrac{6,72}{22,4}=0,3mol\)
\(\left\{{}\begin{matrix}n_{CaCO_3}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\Rightarrow100x+56y=25,6\left(1\right)\)
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\Rightarrow x+y=n_Z=0,3\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\%m_{CaCO_3}=\dfrac{0,2\cdot100}{25,6}\cdot100\%=78,125\%\)
\(\%m_{Fe}=100\%-78,125\%=21,875\%\)
\(m_{muối}=m_{CaCl_2}+m_{FeCl_2}=0,2\cdot111+0,1\cdot127=34,9g\)

Đáp án C
Quy đổi hỗn hợp về Fe (x mol); Cu (y mol) và S (z mol)
Bảo toàn S có
nS = n↓ = 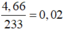 (mol)
(mol)
mX = 2,72 gam → 56x + 64y + 0,02.32 = 2,72 → 56x + 64y = 2,08 (1)
Do Y có thể hòa tan được Cu, bảo toàn electron có:
3.nFe + 2.nCu + 6.nS = 3.0,07 → 3x + 2y = 0,09 (2)
Từ (1) và (2) có: x = 0,02 và y = 0,015.
Dung dịch Y gồm: Fe3+: 0,02 mol; Cu2+: 0,015 mol; SO42- = 0,02 mol; NO3- = (0,5 – 0,07 = 0,43 mol) và có thể có H+
Bảo toàn điện tích → nH+ = 0,38 mol
Cho Cu vào Y có phản ứng:
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
0,1425 ← 0,38 0,43 mol
Cu + 2Fe3+ → Cu2+ + 2Fe2+
0,01 ← 0,02 mol
m = (0,01 + 0,1425).64 = 9,76 gam.

PTHH: Fe + 2HCl --> FeCl2 + H2
FeS + 2HCl --> FeCl2 + H2S
=> \(n_{Fe}+n_{FeS}=n_{H_2}+n_{H_2S}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Và 56.nFe + 88.nFeS = 18,8
=> \(\left\{{}\begin{matrix}n_{Fe}=0,1\left(mol\right)\\n_{FeS}=0,15\left(mol\right)\end{matrix}\right.\)
Bảo toàn S: nCaSO3 = 0,15 (mol)
=> m = 0,15.120 = 18 (g)
=> B
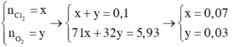
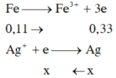
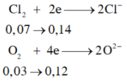
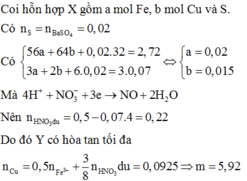

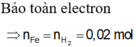
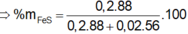
8) nNO=0,04, nO=0,14=> ne=0,4, nFe=0,16 => H+ hết => nH+=nHNO3+2nH2SO4=2nO2+4nNO=> nHNO3=0,32
mọi người giải giúp với ạ, viết phương trình từng câu và giải theo cách nhanh nhất ( kiểu trắc nghiệm ) [ nếu có đầy đủ càng tốt ] e xin cảm ơn trước