Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chào em!
Nguyên tử có 3 loại hạt cơ bản:
+ Vỏ nguyên tử có các hạt electron sắp xếp thành nhiều lớp (e), những hạt này mang điện tích âm.
+ Hạt nhân nguyên tử có các hạt proton(p) mang điện tích dương và các hạt notron (n) không mang điện tích.
Nguyên tử trung hoà về điện: P=E=Z
Sửa đề: Tổng số hạt mang điện tích gấp đôi số hạt không mang điện tích
\(a,2P=2N\Leftrightarrow P=N=E\\ Mà:P+N+E=36\\ \Leftrightarrow3P=36\Leftrightarrow P=E=N=Z=12\)
\(b,m=0,16605.10^{-23}.A=0,16605.10^{-23}.\left(P+N\right)\\ =0,16605.10^{-23}.\left(12+12\right)=3,9852.10^{-23}\left(g\right)\)
\(c,Cấu.hình.e\left(Z=12\right):1s^22s^22p^63s^2\\ Số.lớp.e:3\\ Số.e.lớp.ngoài.cùng:2\)

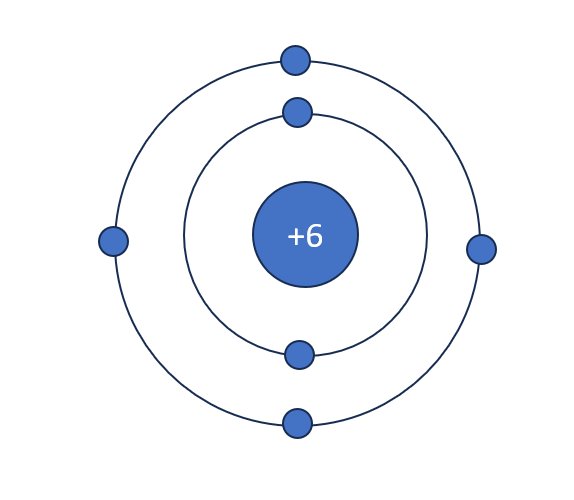
\(a.p+e+n=2p+n=18\\ n=\dfrac{1}{3}\left(2p+n\right)\Leftrightarrow\dfrac{2n}{3}=\dfrac{2p}{3}\Rightarrow n=p\Rightarrow p=\dfrac{18}{3}=6\\ X:C\left(carbon\right)\\ b.\)

Ta có: P + N + E = 48
Mà: P = E (do nguyên tử trung hòa về điện)
⇒ 2P + N = 48 (1)
Theo đề, số hạt mang điện gấp 2 lần số hạt không mang điện.
⇒ 2P = 2N (2)
Từ (1) và (2) ⇒ P = E = N = 16
⇒ MX = 16 + 16 = 32 (amu)

`#3107.101107`
Tổng số hạt `p, n, e` có trong nguyên tố X là `116`
`\Rightarrow p + n + e = 116`
Mà trong nguyên tử, số `p = e`
`\Rightarrow 2p + n = 116`
Vì số hạt mang điện nhiều hơn số hạt không mang điện `24` hạt
`\Rightarrow 2p - n = 24`
`\Rightarrow n = 2p - 24`
Ta có:
`2p + n = 116`
`\Rightarrow 2p + 2p - 24 = 116`
`\Rightarrow 4p = 116 + 24`
`\Rightarrow 4p = 140`
`\Rightarrow p = 140 \div 4`
`\Rightarrow p = 35`
`\Rightarrow p = e = 35`
Số hạt n có trong nguyên tử nguyên tố X là:
`35 . 2 - 24 = 46`
Vậy, số `p, n, e` trong nguyên tử nguyên tố X lần lượt là `35; 46; 35.`
- Tổng số hạt trong nguyên tử nguyên tố X là 116.
⇒ P + N + E = 116
Mà: P = E (Do nguyên tử trung hòa về điện.)
⇒ 2P + N = 116 (1)
- Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 24 hạt.
⇒ 2P - N = 24 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P=E=35\\N=46\end{matrix}\right.\)

Sửa đề : số hạt không mang điện nhiều hơn số hạt mang điện là 2
a. VÌ nguyên tử cấu tạo bởi 3 loại hạt proton , electron , neutron
Mà số p = số e
Lại có
\(\Rightarrow\left\{{}\begin{matrix}2P+N=58\\2P-N=-2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=E=14\\N=30\end{matrix}\right.\)
b. \(m_{NT}=14.1+30.1+14.0,00055=44,0077\left(amu\right)\)

Gọi số proton , notron , electron của nguyên tử M lần lượt là p , n , e ( p,n,e ϵ N*)
Ta có :
n - p = 1 => n = p+1 (*)
Do trong nguyên tử M số hạt mang điện lớn hơn số hạt không mang điện là 10 hạt
=> (p+e) - n = 10
=> 2p - n = 10 (vì nguyên tử trung hòa về điện)
kết hợp (*) ta được
2p - (p+1) = 10
=> 2p - p - 1 =10
=> p = 11
=> e = 11 (hạt)
=> M là nguyên tố Natri

Hạt nhân nguyên tử của nguyên tố A có 24 hạt:
\(2P+N=24\)
Số hạt không mang điện là 12:
\(N=12\)
=> \(2P+12=24\Rightarrow P=\dfrac{24-12}{2}=6\)
=> A là nguyên tố Cacbon.
Cấu hình e: \(1s^22s^22p^2\)
Vị trí: ô số 6 trong bảng tuần hoàn, chu kì 2, nhóm IVA
Tính chất cơ bản của A: tính phi kim xu hướng nhận e, không màu, không mùi, khả năng dẫn điện và nhiệt kém.