Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B.
n C = 1,2 : 12 = 0,1mol; n O 2 = 1,68 : 22,4 = 0,075 mol
C + O 2 ⟶ CO 2
0,075 0,075 0,075 (mol)
C dư ⇒ V CO 2 = 0,075.22,4 = 1,68 lít

2/\(Si+O_2\rightarrow SiO_2\)
\(2NaOH+SiO_2\rightarrow H_2O+Na_2SiO_3\)
\(H_2O+Na_2SiO_3+CO_2\rightarrow Na_2CO_3+H_2SiO_3\)
\(H_2SiO_3\rightarrow H_2O+SiO_2\)
\(2C+SiO_2\rightarrow2CO+Si\)
Bài 2:
- Si + O2 → SiO2
- SiO2 + NaOH → Na2SiO3 + H2O
- Na2SiO3 + CO2 → SiO2 + Na2CO3
- 2SiO2 + 2C → 2CO +Si

a.
3CO + Fe2O3 ---to---> 2Fe + 3CO2
CO + PbO ---to---> Pb + CO2
b.
2CO + O2 ---to---> 2CO2
CO + CuO ---to---> Cu + CO2
c.
CO2 + 2NaOH → Na2CO3 + H2O
CO2 + Ca(OH)2 → CaCO3 + H2O

\(CaCO_3 \rightarrow ^{t^o} CaO + CO_2\)
\(n_{CaCO_3}= \dfrac{20}{100}= 0,2 mol\)
Theo PTHH:
\(n_{CO_2}=n_{CaO}=n_{CaCO_3}= 0,2 mol\)
\(\Rightarrow m_{CaO}= 0,2 . 56=11,2 g\)
\(V_{CO_2}= 0,2 . 22,4=4,48 l\)
b)\(2NaOH + CO_2 \rightarrow Na_2CO_3 + H_2O\)
\(Na_2CO_3 + CO_2 + H_2O \rightarrow 2 NaHCO_3\)
\(m_{NaOH}= 12 . 50\)%= 6 g
\(n_{NaOH}=\dfrac{6}{40}= 0,15 mol\)\(\Rightarrow n_{nhóm OH}= 0,15 . 1= 0,15 mol\)
Ta có tỉ lệ T:
\(T=\dfrac{n_{nhóm OH}}{n_{CO_2}}= \dfrac{0,15}{0,2}=0,75<1\)
Do T=0,75<1 nên muối tạo thành là muối axit NaHCO3
natri hiđrocacbonat
\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
PTHH:\(CaCO_3\rightarrow CaO+CO_2\)
0,2 0.2 0,2 (mol)
\(V_{CO_2}=n.22,4=0,2.22,4=4,48\left(l\right)\)
\(m_{CaO}=0,2.56=11,2\left(g\right)\)
b.\(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
thu được muối natri cacbonat

\(n_{hh}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(n_{CH_4}=a\left(mol\right),n_{H_2}=b\left(mol\right)\)
\(\Rightarrow a+b=0.5\left(1\right)\)
\(n_{H_2O}=2a+b=\dfrac{12.6}{18}=0.7\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.2,b=0.3\)
\(n_{CO_2}=n_{CH_4}=0.2\left(mol\right)\)
\(V=0.2\cdot22.4=4.48\left(l\right)\)
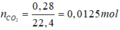
\(n_C=\frac{1,2}{12}=0,1\left(mol\right)\)
\(n_{O2}=\frac{1,68}{22,4}=0,075\left(mol\right)\)
________\(C+O_2\underrightarrow{t^o}CO_2\)
Ban đầu: 0,1_0,075
Phản ứng: 0,075________(mol)
Dư: 0,025
Lập tỉ lệ: \(\frac{0,1}{1}>\frac{0,075}{1}\)
\(V_{CO2}=0,075.22,4=1,68\left(l\right)\)
Chúc bạn học tốt