Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1. nH2=3.36/22.4=0.15mol
PT: Fe+ 2HCl ---> FeCl2 + H2
0.15 0.3 0.15
a)mFe=0.15*56=8.4g
b)CMddHCl = 0.3/0.5=0.6M
2. nCO=15.68/22.4=0.7 mol
Đặt x,y lần lượt là số mol của CuO,Fe2O3 :
PT: CuO+ CO ---> Cu + CO2
x x
Fe2O3 + 3CO --> Fe + 3CO2
y 3x
Theo pthh,ta lập được hệ pt:
80x + 160y=40(1)
x + 3x = 0.7 (2)
giải hệ pt trên,ta được :x =0.1, y=0.2
Thế x,y vào PTHH:
CuO+ CO ---> Cu + CO2
0.1 0.1
Fe2O3 + 3CO --> Fe + 3CO2
0.2 0.6
mCuO=0.1*80=8g => %CuO=(8/40)*100=20%
=>%Fe2O3= 100 - 20=80%
b) Để tách Cu ra khỏi hỗn hợp Fe,Cu.Dùng nam châm để hút sắt ra khỏi hỗn hợp (sắt có tính từ),còn lại là đồng.
Chúc em học tốt !!@

M(Y)=19x2=38(đvC) =>nNO=nNO2=0,0175(mol)
BTe:3x=4nO2+0,0175.3+0,0175.1
=>nO2=(3x-0,07)/4
BTKL: mFe+mO2=m(A) <=> 56x+(3x-0,07).32/4=5,04
<=> x=0,07 (mol )

1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl

BÀI NÀY THÌ PHẦN TRĂM SAI 99,99%, VÌ VẬY NẾU SAI XIN ANH RAINBOW GIẢI LẠI .
\(n_E=\dfrac{2,24}{22,4}=0,1mol\)
\(n_{\downarrow}=n_{CaCO_3}=\dfrac{4}{100}=0,04mol\)
Dẫn khí oxi đi qua cacbon nung nóng xảy ra hai phương trình hoá học :
\(2C+O_2\underrightarrow{t^o}2CO\)
x mol \(\rightarrow\) x mol \(\)
\(C+O_2\underrightarrow{t^o}CO_2\)
y mol \(\rightarrow\) y mol
Hỗn hợp E gồm \(CO\left(x\right);CO_2\left(y\right);O_2du\left(z\right)\)
Ta có :
\(n_E=n_x+n_y+n_z=0,1\)
\(d_{\dfrac{E}{H_2}}=\dfrac{M_E}{M_{H_2}}=18\rightarrow\dfrac{M_E}{2}=18\Rightarrow M_E=36g\)
\(m_E=M_E.n_E=36.0,1=3,6g\rightarrow28x+44y+32z=3,6\)
Dẫn E qua nước vôi trong dư , chỉ có \(CO_2\) bị hấp thụ :
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow\)
y mol \(\rightarrow\) y mol
\(\rightarrow y=0,04mol\)
Ta có :
\(\left\{{}\begin{matrix}x+y+z=0,1\\28x+44y+32z=3,6\\y=0,04\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}x=0,02\\y=0,04\\z=0,04\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,02}{0,1}.100=20\%.\\\%V_{CO_2}=\dfrac{0,04}{0,1}.100=40\%.\\\%V_{O_2}=\dfrac{0,04}{0,1}.100=40\%.\end{matrix}\right.\)
Vậy ............

Chọn B
Phản ứng khử oxit của CO có thể hiểu là:
![]()
Trước là 44,8 g oxit sau thu được 40g chất rắn.
Vậy lượng chất rắn sau phản ứng bị giảm.
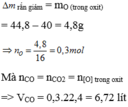

Câu 1: Đặt CÔng thức FexOy
FexOy+yCO\(\rightarrow\)xFe+yCO2
CO2 bị Ca(OH)2 hấp thụ nên m=\(m_{CO_2}\)
Fe+2HCl\(\rightarrow\)FeCl2+H2
\(n_{Fe}=n_{H_2}=0,1mol\)
Theo PTHH 1 ta có: noxit\(=\dfrac{1}{x}.n_{Fe}=\dfrac{0,1}{x}mol\)
MOxit\(=\dfrac{m}{n}=\dfrac{8}{\dfrac{0,1}{x}}=80x\)
Hay 56x+16y=80x suy ra 24x=16y hay 3x=2y\(\Leftrightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Fe2O3
\(n_{CO_2}=\dfrac{y}{x}n_{Fe}=\dfrac{3}{2}.0,1=0,15mol\)
m=0,15.44=6,6g
Cu+2AgNO3\(\rightarrow\)Cu(NO3)2+2Ag
-Gọi số mol Cu là x theo PTHH số mol Ag là 2x
- Độ tăng khối lượng=108.2x-64x=7,6
152x=7,6 hay x=0,05mol
\(n_{AgNO_3}=2n_{Cu}=2.0,05=0,1mol\)
\(m_{AgNO_3}=0,1.170=17g\)
\(m_{AgNO_3}=0,1.170=17g\)
\(m_{ddAgNO_3}=v.D=400.1,05=420g\)
\(C\%=\dfrac{17.100}{420}\approx4,05\%\)
mdd=420-7,6=412,4g
\(n_{Cu\left(NO_3\right)_2}=n_{Cu}=0,05mol\)
\(m_{Cu\left(NO_3\right)_2}=0,05.188=9,4g\)
\(C\%=\dfrac{9,4.100}{412,4}\approx2,3\%\)
BÀI GÌ MÀ KHÓ THẾ LÀM SAI 90% RỒI .
\(n_{CO}=\dfrac{2,24}{22,4}=0,1mol\)
\(n_{Fe}=\dfrac{3,36}{56}=0,06mol\)
Hỗn hợp khí gồm :CO (a) và \(CO_2\left(b\right)\) . Ta có : a + b = 0,1 mol.(1)
\(d_{\dfrac{hh}{H_2}}=\dfrac{\overline{M_{hh}}}{M_{H_2}}=20,4.\rightarrow\overline{M_{hh}}=20,4.2=40,8\left(g\right)\rightarrow\dfrac{m_{hh}}{n_{hh}}=40,8\rightarrow\dfrac{28a+44b}{a+b}=40,8\rightarrow28a+44b=40,8\left(a+b\right)=40,8.0,1=4,08\left(2\right)\)
Từ (1) và (2) ta có hệ phương trình :
\(\left\{{}\begin{matrix}a+b=0,1\\28a+44b=4,08\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}a=0,02\\b=0,08\end{matrix}\right.\)
Gọi công thức của Sắt là \(Fe_xO_y\) . Phương trình hoá học khử oxit sắt bằng khí \(CO_2\) .
\(Fe_xO_y+yCO\underrightarrow{t^o}xFe+yCO_2.\)
c \(\rightarrow\) cx \(\rightarrow\) cy
\(\rightarrow\) cx =0,06 , cy = 0,08 .
Ta có : \(\dfrac{x}{y}=\dfrac{cx}{cy}=\dfrac{0,06}{0,08}=\dfrac{3}{4}\rightarrow x=3;y=4\)
Vậy oxit sắt cần tìm là \(Fe_3O_4.\)
sai đâu đúng hết mà