Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

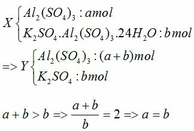
Vì dung dịch sau phản ứng chỉ chứa một chất tan => Z chỉ chứa KAlO2 hoặc K2SO4.
Khi cho từ từ Ba(OH)2 vào Y thì có thể xảy ra các phản ứng:
Al2(SO4)3 + 3Ba(OH)2 → 2Al(OH)3 + 3BaSO4(1)
2b → 6b 4b 6b (mol)
K2SO4 + Ba(OH)2 → 2KOH + BaSO4 (2)
b → b 2b b (mol)
Al(OH)3 + KOH → KAlO2 + 2H2O (3)
2b →2b 2b (mol)
· Trường hợp 1: Chất tan trong Z là K2SO4 → vừa đủ phản ứng (1)
Theo đề => a= b = 0,02 mol
nBaSO4 = nBa(OH)2 = 6b = 0,12mol
nAl(OH)3 = 4b = 0,08mol
m1= 948 . 0,02 + 342 . 0,02 = 25,8 gam
m2 = 0,08 . 78 + 0,12 . 233 = 34,2 gam
V = 0,12/2 = 0,06 lít = 60ml
· Trường hợp 2: Chất tan trong Z là KAlO2 →xảy ra cả (1,2,3)
nKAlO2 = 0,02mol
=> 2b = 0,02 => a = b =0,01
nBaSO4 = nBa(OH)2 = 7b = 0,07
nAl(OH)3 = 4b – 2b = 0,02
=> m1= 948.0,01 + 342.0,01 = 12,9 gam
m2 = 0,02.78 + 0,07.233 = 17,87 gam
V = 0,07/2 = 0,035 lít = 35ml

PTHH: \(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\) (1)
\(HCl+NaOH\rightarrow NaCl+H_2O\) (2)
\(AlCl_3+3NaOH\rightarrow3NaCl+Al\left(OH\right)_3\downarrow\) (3)
Ta có: \(\left\{{}\begin{matrix}n_{Al_2O_3}=\dfrac{6,12}{102}=0,06\left(mol\right)\\\Sigma n_{HCl}=0,2\cdot2=0,4\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,06}{1}< \dfrac{0,4}{6}\) \(\Rightarrow\) HCl còn dư, Al2O3 p/ứ hết
Vì bazơ mạnh sẽ p/ứ với axit mạnh trước nên sẽ xảy ra p/ứ (2) và (3)
Lại có: \(n_{Al\left(OH\right)_3}=\dfrac{7,8}{78}=0,1\left(mol\right)=n_{AlCl_3\left(3\right)}\)
Theo PTHH (1): \(n_{AlCl_3\left(1\right)}=0,12\left(mol\right)\)
\(\Rightarrow\) AlCl3 còn dư nên tính theo Al(OH)3 \(\Rightarrow n_{NaOH\left(3\right)}=0,3\left(mol\right)\)
Mặt khác: \(n_{HCl\left(dư\right)}=n_{HCl\left(2\right)}=0,04\left(mol\right)=n_{NaOH\left(2\right)}\)
\(\Rightarrow\Sigma n_{NaOH}=0,34\left(mol\right)\) \(\Rightarrow V_{NaOH}=\dfrac{0,34}{2}=0,17\left(l\right)=170\left(ml\right)\)

a) 2HCl + Ca(OH)2 = CaCl2 + 2H2O
0.2 0.1 0.1 (mol)
b) nCaCl2=11.1:111 = 0.1 (mol)
=>VHCl= 0.2:0.5= 0.4 (l)
=>VCa(OH)2=0.1:2=0.05(l)
c) CM CaCl2=0.1: (0.4+0.05)=0.22M
mình chỉ làm thử thôi nhaa![]()

PTHH bạn tự viết nha.
Từ (1) và (2)->nCl- trong 50ml dd A=nAgCl=4.305:143.5=0.03mol
->500ml dd A có 0.03x500:50=0.3 mol Cl-
đặt nNaCl=amol;nKCl=bmol
Ta có hệ: 58.5a+74.5b=19.15
a+b=0.3
->a=0.2mol;b=0.1mol
->CM NaCl=0.2:0.5=0.4M
CM KCl=0.1:0.5=0.2M

nCO2 = 6,72 / 22,4 = 0,3 mol
Giả sử pứ tạo 2 muối \(\begin{cases}Na2CO3:xmol\\NaHCO3:ymol\end{cases}\)
CO2 + 2NaOH ===> Na2CO3 + H2O
x 2x x (mol)
CO2 + NaOH ===> NaHCO3
y y y (mol)
Theo đề bài và theo PTHH, ta có:
\(\begin{cases}x+y=0,3\\106x+84y=29,6\end{cases}\)
===> x = 0,2 mol, y = 0,1 mol
Vì x, y đều có nghiệm xác đunhj nên giả thiết trên là đúng.
=> nNaOH = 2 x 0,2 + 0,1 = 0,5 mol
=> V = 0,5 / 2 = 0,25 lít = 250 ml
Bìa này còn nhiều cách giải lắm, bạn tự tìm hiểu nha!!!![]()

\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(n_{HCl}=\dfrac{73\cdot36.5\%}{36.5}=0.73\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(1.............2\)
\(0.1.........0.73\)
\(LTL:\dfrac{0.1}{1}< \dfrac{0.73}{2}\rightarrow HCldư\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(m_{ZnCl_2}=0.1\cdot136=13.6\left(g\right)\)
\(m_{\text{dung dịch sau phản ứng}}=6.5+73-0.1\cdot2=79.3\left(g\right)\)
\(C\%_{ZnCl_2}=\dfrac{13.6}{79.3}\cdot100\%=17.15\%\)
\(C\%_{HCl\left(dư\right)}=\dfrac{\left(0.73-0.2\right)\cdot36.5}{79.3}\cdot100\%=25.4\%\)
---Chúc em học tốt------
lần sau bạn nhớ cho them NTK nha cho dễ nhìn mà tính

Gọi x, y lần lượt là số mol của NaCl và KCl
Theo đề bài ta có pt:
58,5x + 74,5y=13,3
x + y = 10 x nAgCl = 10 x (2,87 : 143,5) = 0,2
Giải hệ ta được x = y = 0,1
m NaCl = 58,5 x 0,1 = 5,85 (g) ===> m KCl = 13,3 - 5,85 = 7,45 (g)
C% NaCl = (5,85 : 500) x 100% = 1,17%
C% KCl = (7,45 :500) x 100% = 1,49%
Chúc bạn học tốt!!!
Bt1: Làm bay hơi 200ml nước từ ddNaCL 2M người ta thu được dd NaCL 5M. Tính Vdd NaCL 2M ban đầu.
---
Gọi x là số mol NaCl. (x>0)
=> \(\frac{x}{2}-0,2=\frac{x}{5}\\ \rightarrow x=\frac{2}{3}\)
=> nNaCl= 2/3 (mol)
=> VddNaCl(ban đầu)= nNaCl/CMddNaCl(bđ)= (2/3)/2= 1/3 (l)
Bt2: Hoà tan 36,24 gam muối kép (NH4)2SO4.Al2(SO4)3.24H2O vào 163,76 gam nước. Tính C% và Cm của dd thu được.
---
\(n_{\left(NH_4\right)_2SO_4.Al_2\left(SO_4\right)_3.24H_2O}=\frac{36,24}{906}=0,04\left(mol\right)\)
mdd= m(muối kép)+ mH2O= 36,24+163,76=200(g)
\(m_{\left(NH_4\right)_2SO_4}=0,04.132=5,28\left(g\right)\\ n_{Al_2\left(SO_4\right)_3}=342.0,04=13,68\left(g\right)\\ \rightarrow C\%dd\left(NH_4\right)_2SO_4=\frac{5,28}{200}.100=2,64\%\\ C\%ddAl_2\left(SO_4\right)_3=\frac{13,68}{200}.100=6,84\%\)
Câu 1 phải là 0,3 chứ