Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn D.
Khí quyển có p0 = 105 Pa, ở nhiệt độ T0 = 0 + 273 = 273 K.
Áp suất của khí trong cốc ở 100 oC là:
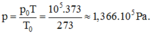
Gọi p1 là áp suất của nắp đậy lên bình ta có:
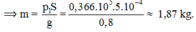
p = p1 + p0 ⟹ p1 = p – p0 = 0,366.105 N/m2

Chọn D.
Khí quyển có p 0 = 10 5 Pa, ở nhiệt độ T 0 = 0 + 273 = 273 K.
Áp suất của khí trong cốc ở 100 o C là:
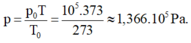
Gọi p1 là áp suất của nắp đậy lên bình ta có:
p = p 1 + p 0 ⇒ p 1 = p - p 0 = 0 , 366 . 105 N / m 2
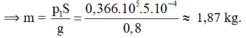

Chọn A.
Gọi thể tích và áp suất của bọt khí ở đáy hồ và mặt hồ lần lượt là p 1 , V 1 và p 2 , V 2 , ta có:
p 2 = p 0 , p 1 = p 0 + h/13,6 (cmHg)
Áp dụng định luật Bôi-lơ – Ma-ri-ốt: p 1 V 1 = p 2 V 2
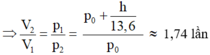

Chọn A.
Gọi thể tích và áp suất của bọt khí ở đáy hồ và mặt hồ lần lượt là p1, V1 và p2, V2, ta có:
p2 = p0, p1 = p0 + h/13,6 (cmHg)
Áp dụng định luật Bôi-lơ – Ma-ri-ốt: p1V1 = p2V2
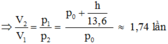

Chọn A.
Ở điều kiện tiêu chuẩn (1 atm, 0 oC), khối lượng riêng của ôxi là: ρ0 = m/V0.
Ở điều kiện 150 atm, 0 oC, khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = ρ0.V0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p0V0 = pV (2)
Từ (1) và (2) suy ra:
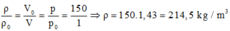
Và m = ρ.V = 214,5.15-3 ≈ 3,23 kg.

Chọn A.

Ở điều kiện tiêu chuẩn (1 atm, 0 o C ), khối lượng riêng của ôxi là: p 0 = m / V 0
Ở điều kiện 150 atm, 0 o C , khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = p 0 . V 0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p 0 . V 0 = pV (2)
Từ (1) và (2) suy ra:
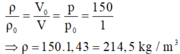
Và m = ρ . V = 214,5.15.10 − 3 ≈ 3,22 k g
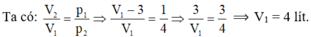
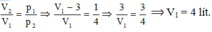
Chọn A.
Xét lượng khí ở hai trạng thái.
Trạng thái 1: T1 = 273 K; p1 = 1,02.105 Pa; V1 = m/1,29.
Trạng thái 2: p2 = 4.105 Pa; T2 = 473 K; V2 = m/ρ .
Áp dụng phương trình trạng thái: