
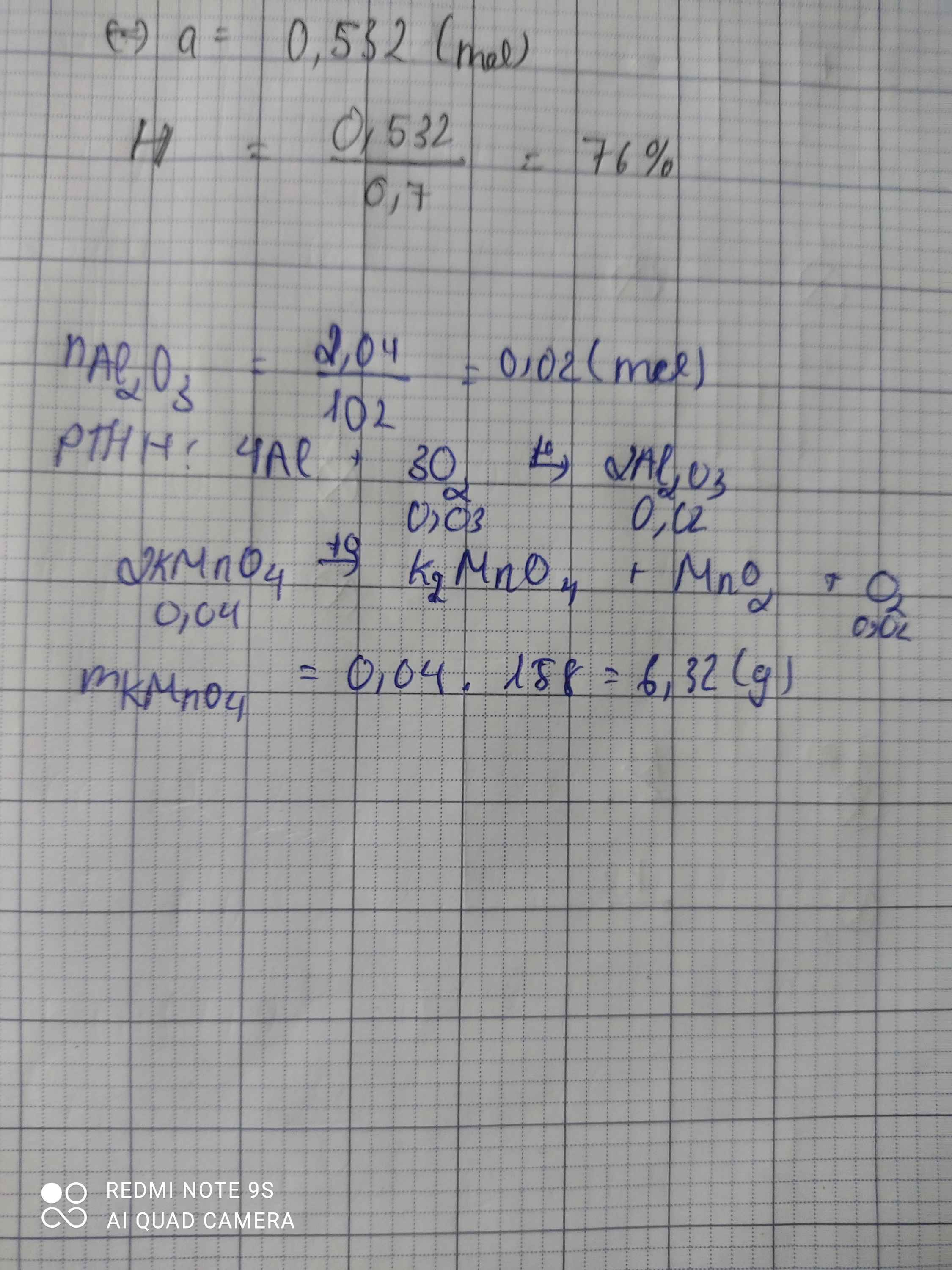
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

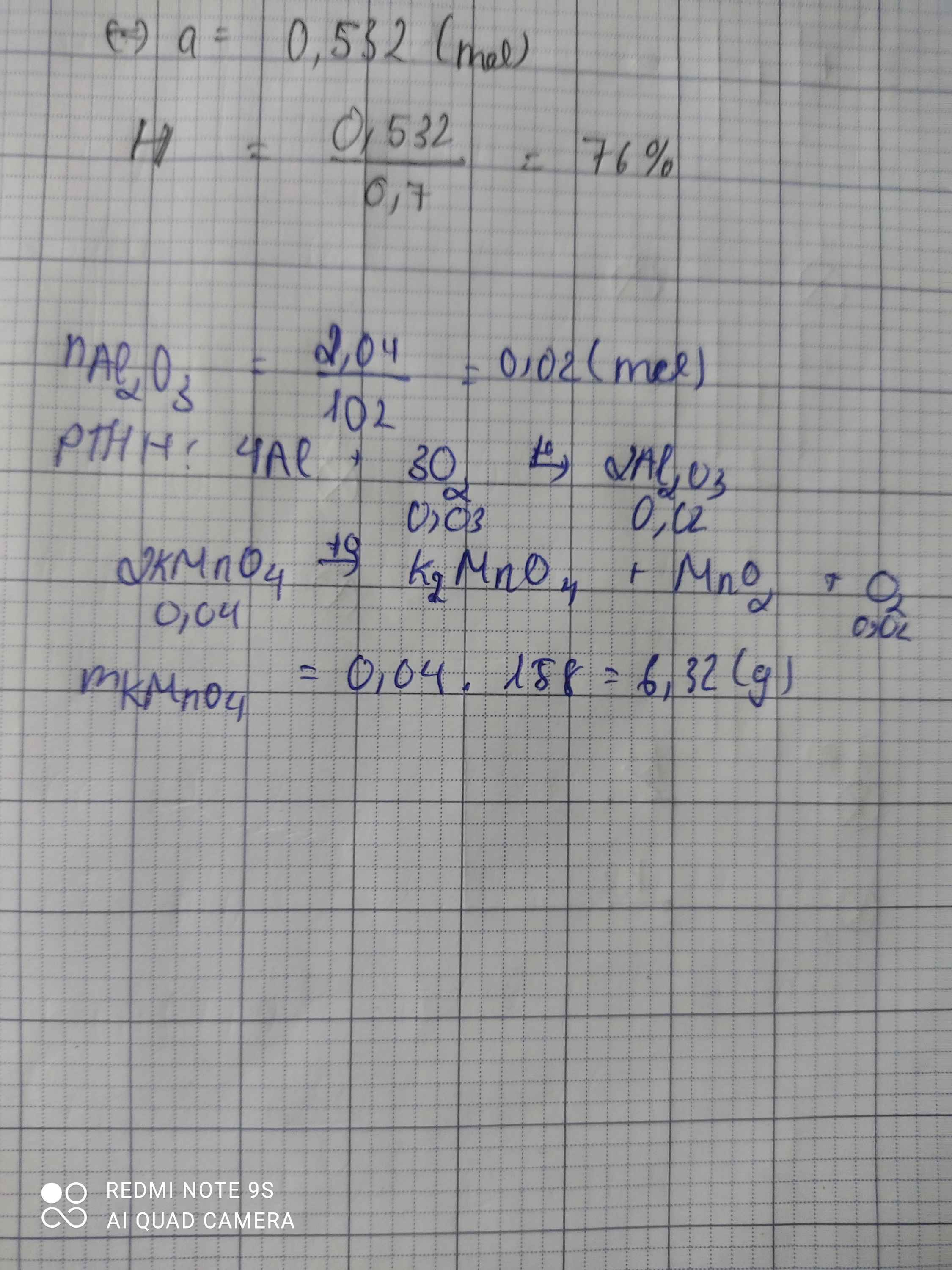

a) 2KMnO4--------->K2MnO4+MnO2+O2
b) n KMnO4=15,8/158=0,1(mol)
Theo pthh
n O2=1/2n KMnO4=0,05(mol)
V O2=0,05.22,4=1,12(l)
c) 3O2+4Al---->2Al2O3
Theo pthh
n Al2O3=2/3n O2=0,03333(mol)
m Al2O3=0,033333.102=3,4(g)

Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
a, PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
_____0,05__0,1____________0,05 (mol)
b, mFe = 0,05.56 = 2,8 (g)
c, mHCl = 0,1.36,5 = 3,65 (g)
\(\Rightarrow m_{ddHCl}=\dfrac{3,65}{10\%}=36,5\left(g\right)\)
Bạn tham khảo nhé!

Ta có: \(n_{H_2SO_4}=\dfrac{58,8}{98}=0,6\left(mol\right)\)
\(PTHH:2Al+3H_2SO_4--->Al_2\left(SO_4\right)_3+3H_2\uparrow\)
0,4 <--- 0,6 -----------> 0,2 --> 0,6
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,4.27=10,8\left(g\right)\\m_{Al_2\left(SO_4\right)_3}=0,2.342=68,4\left(g\right)\\V_{H_2}=0,6.22,4=13,44\left(lít\right)\end{matrix}\right.\)

a) 4Al + 3O2 --to--> 2Al2O3
b) \(n_{O_2}=\dfrac{19,2}{32}=0,6\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,8<-0,6---------->0,4
=> mAl = 0,8.27 = 21,6(g)
c) mAl2O3 = 0,4.102 = 40,8(g)

a) pt
1) Zn + 2HCl -> ZnCl2 + H2
2) H2 + CuO -> Cu + H2O
b) ta có mZn = 6,5 g
=> nZn = 0,1 mol
pt 1)
1) Zn + 2HCl -> ZnCl2 + H2
..0,1mol..0,1mol..0,1mol.....0,1mol
theo pt 1) ta có nZn = nH2 = 0,1mol
pt 2)
2) H2 + CuO -> Cu + H2O
...0,1mol...0,1mol...0,1mol..0,1mol
theo pt 2) ta có nH2 = nCu = 0,1mol
=> mCu = 0,1 . 64 = 6,4 g
1. PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\) (1)
\(H_2+CuO\rightarrow Cu+H_2O\) (2)
2. \(n_{Zn}=\dfrac{6,5}{65}=0.1mol\)
Từ phương trình (1) : \(n_{H_2}=n_{Zn}=0.1mol\)
Vì lượng \(H_2\) ở cả hai phương trình bằng nhau nên cùng bằng 0,1 mol.
Từ phương trình (2) :\(n_{Cu}=n_{H_2}=0,1mol\)
\(\rightarrow m_{Cu}=0,1.64=6,4g\)

a.4Al + 3O2 -> 2Al2O3
0.8 0.6 0.4
\(nO2=\dfrac{19.2}{32}=0.6mol\)
b.mAl = \(0.8\times27=21.6g\)
c.mAl2O3 = \(0.4\times102=40.8g\)

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{Cu}=\dfrac{40}{80}=0,5\left(mol\right)\)
PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\left(1\right)\)
Xét tỉ lệ: \(\dfrac{0,5}{1}>\dfrac{0,1}{1}\) => CuO dư, tính theo H2
Theo PT \(\left(1\right):n_{Cu}=n_{H_2}=0,1\left(mol\right)\)
\(\rightarrow m_{Cu}=0,1.64=6,4\left(g\right)\)

a)
MgCO3 --to--> MgO + CO2
CaCO3 --to--> CaO + CO2
b) Khối lượng rắn sau pư giảm do có khí CO2 thoát ra
c) \(m_{giảm}=m_{CO_2}=8,8\left(g\right)\)
=> \(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\)
Gọi số mol CaCO3, MgCO3 là a, b (mol)
=> \(\left\{{}\begin{matrix}a+b=0,2\\100a+84b=18,4\end{matrix}\right.\)
=> a = 0,1 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}m_{CaCO_3}=0,1.100=10\left(g\right)\\m_{MgCO_3}=0,1.84=8,4\left(g\right)\end{matrix}\right.\)

\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Zn + 2HCl ---> FeCl2 + H2
0,3<---------------0,3<----0,3
=> \(\left\{{}\begin{matrix}m=0,3.65=19,5\left(g\right)\\m_{muối}=0,3.136=40,8\left(g\right)\\V_{ddHCl}:thiếu.C_M\end{matrix}\right.\)
\(n_{Fe_2O_3}=\dfrac{32}{160}=0,2\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
LTL: \(0,2>\dfrac{0,3}{3}\) => Fe2O3 dư
Theo pthh: nFe2O3 (pư) = \(\dfrac{1}{3}n_{H_2}=\dfrac{1}{3}.0,3=0,1\left(mol\right)\)
nFe = \(\dfrac{2}{3}n_{H_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\)
=> mchất rắn = 0,1.160 + 0,2.56 = 27,2 (g)