Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
Phản ứng phân hủy
b) \(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
PTHH: 2KNO3 --to--> 2KNO2 + O2
0,15<--------------------0,075
=> \(m_{KNO_3\left(PTHH\right)}=0,15.101=15,15\left(g\right)\)
=> mKNO3 (thực tế) = \(\dfrac{15,15.100}{85}=17,824\left(g\right)\)
c) \(n_{KNO_3\left(pư\right)}=\dfrac{10,1.80\%}{101}=0,08\left(mol\right)\)
=> nO2 = 0,04 (mol)
=> VO2 = 0,04.22,4 = 0,896(l)

Bài 1.
\(n_{Mg}=\dfrac{2,4}{24}=0,1mol\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
Đây là phản ứng hóa hợp vì chất sản phẩm được tạo từ 2 chất ban đầu.
\(n_{O_2}=2n_{Mg}=0,2mol\)
\(V=0,2\cdot22,4=4,48\left(l\right)\)
Bài 2.
\(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
\(n_{O_2}=\dfrac{1,68}{22,4}=0,075mol\)
\(n_{KNO_3}=2n_{O_2}=0,15mol\)\(\Rightarrow m_{KNO_3}=0,15\cdot101=15,15g\)

2KClO3-to\xt->2KCl+3O2
0,1------------------0,1
n KClO3=\(\dfrac{12,25}{122,5}\)=0,1 mol
=>m KCl=0,1.74,5=7,45g
H=\(\dfrac{6,8}{7,45}.100\)=91,275%
b)
2KClO3-to\xt->2KCl+3O2
0,2-------------------------0,3 mol
n O2=\(\dfrac{6,72}{22,4}\)=0,3 mol
H=85%
=>m KClO3=0,2.122,5.\(\dfrac{100}{85}\)=28,82g
c)
2KClO3-to\xt->2KCl+3O2
0,2------------------------0,3
n KClO3=\(\dfrac{24,5}{122,5}\)=0,2 mol
H=80%
=>m O2=0,3.32.\(\dfrac{80}{100}\)=10,4g

a) PTHH:
2KNO3→2KNO2 + O2
b)\(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)Theo PTHH ta có:
nKNO3=2nO2=0,15(mol)
mKNO3 ban đầu=0,15.101=15,15(g)
mKNO3 thực tế=15,15.\(\dfrac{85}{100}\)=12,8775(g)

\(PTHH:2KNO_3\overset{t^0}{\rightarrow}2KNO_2+O_2\)
\(a,n_{O_2}=\frac{11,2}{32}=0,35mol\)
\(\Rightarrow n_{KNO_3}=\frac{0,35}{80}.101=44,1875g\)
\(b,n_{KNO_3}=\frac{40,4}{101}=0,4mol\)
\(\Rightarrow m_{O_2}=0,4.32.85\%=10,88g\)

\(n_{O_2}=\dfrac{0,64}{32}=0,02mol\\ 2KNO_3\xrightarrow[]{t^0}2KNO_2+O_2\\ n_{KNO_3\left(lí.thuyết\right)}=0,02.2=0,04mol\\ n_{KNO_3\left(thực.tế\right)}=0,04:80\%=0,05mol\\ m_{KNO_3\left(cần\right)}=0,05.101=5,05g\\ \Rightarrow B\)

\(PTHH:2KClO_3\underrightarrow{t^o}2KCl+3O_2\left(1\right)\\ PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\left(2\right)\)
\(Gọi.số.mol.của.O_2.là:a\)
\(Theo.PTHH\left(1\right):n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2}{3}.a=\dfrac{2a}{3}\\ m=m_{KClO_3}=n.M=\dfrac{2a}{3}.122,5=\dfrac{245a}{3}\left(g\right)\)
\(Theo.PTHH\left(2\right):n_{KMnO_4}=2.n_{O_2}=2.a=2a\\ x=m_{KMnO_4}=n.M=2a.158=316a\left(g\right)\)
\(Tỉ.lệ:m:x:\dfrac{m}{x}=\dfrac{\dfrac{245a}{3}}{316a}=\dfrac{245}{948}\)

a) \(2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\)
b)
\(n_{KClO_3} = \dfrac{36,75}{122,5} = 0,3(mol)\)
Theo PTHH :
\(n_{KCl} = n_{KClO_3} = 0,3(mol)\\ \Rightarrow m_{KCl} = 0,3.74,5 = 22,35(gam)\\ \Rightarrow m_{O_2} = m_{KClO_3} - m_{KCl} = 14,4(gam)\)
c)
Bảo toàn khối lượng :
\(m_{O_2} = 25 - 15,4 = 9,6(gam)\\ \Rightarrow n_{O_2} = \dfrac{9,6}{32} = 0,3(mol)\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = 0,2(mol)\\ \Rightarrow m_{KClO_3} = 0,2.122,5 = 24,5(gam)\\ \%m_{tạp\ chất}= \dfrac{25-24,5}{25}.100\% = 2\%\)
\(a.\)
\(2KClO_3\underrightarrow{t^0}2KCl+3O_2\)
\(b.\)
\(n_{KClO_3}=\dfrac{36.75}{122.5}=0.3\left(mol\right)\)
\(\Rightarrow n_{O_2}=\dfrac{3}{2}n_{KClO_3}=\dfrac{3}{2}\cdot0.3=0.45\left(mol\right)\)
\(m_{O_2}=0.45\cdot32=14.4\left(g\right)\)
\(m_{KCl}=0.3\cdot74.5=22.35\left(g\right)\)
\(c.\)
\(2KClO_3\underrightarrow{t^0}2KCl+3O_2\)
\(a.............a\)
\(m_{Cr}=m_{KCl}+m_{tc}=25-122.5a+74.5a=15.4\left(g\right)\)
\(\Rightarrow a=0.2\)
\(m_{O_2}=\dfrac{3}{2}\cdot0.2\cdot32=9.6\left(g\right)\)
\(m_{KClO_3}=0.2\cdot122.5=24.5\left(g\right)\)
\(m_{tc}=25-24.5=0.5\left(g\right)\)
\(\%m_{Tc}=\dfrac{0.5}{25}\cdot100\%-2\%\)

2KClO3 ---> 2KCl +3O2
nKClo3 = 24,5/122,5 = 0,2 mol
nKCl = nKClo3 =0,2 mol
m Kcl = 0,2 x 74,5 = 14,9g
no2 = 0,2x3:2 = 0,3mol
Vo2 = n.22,4 = 6,72 lít
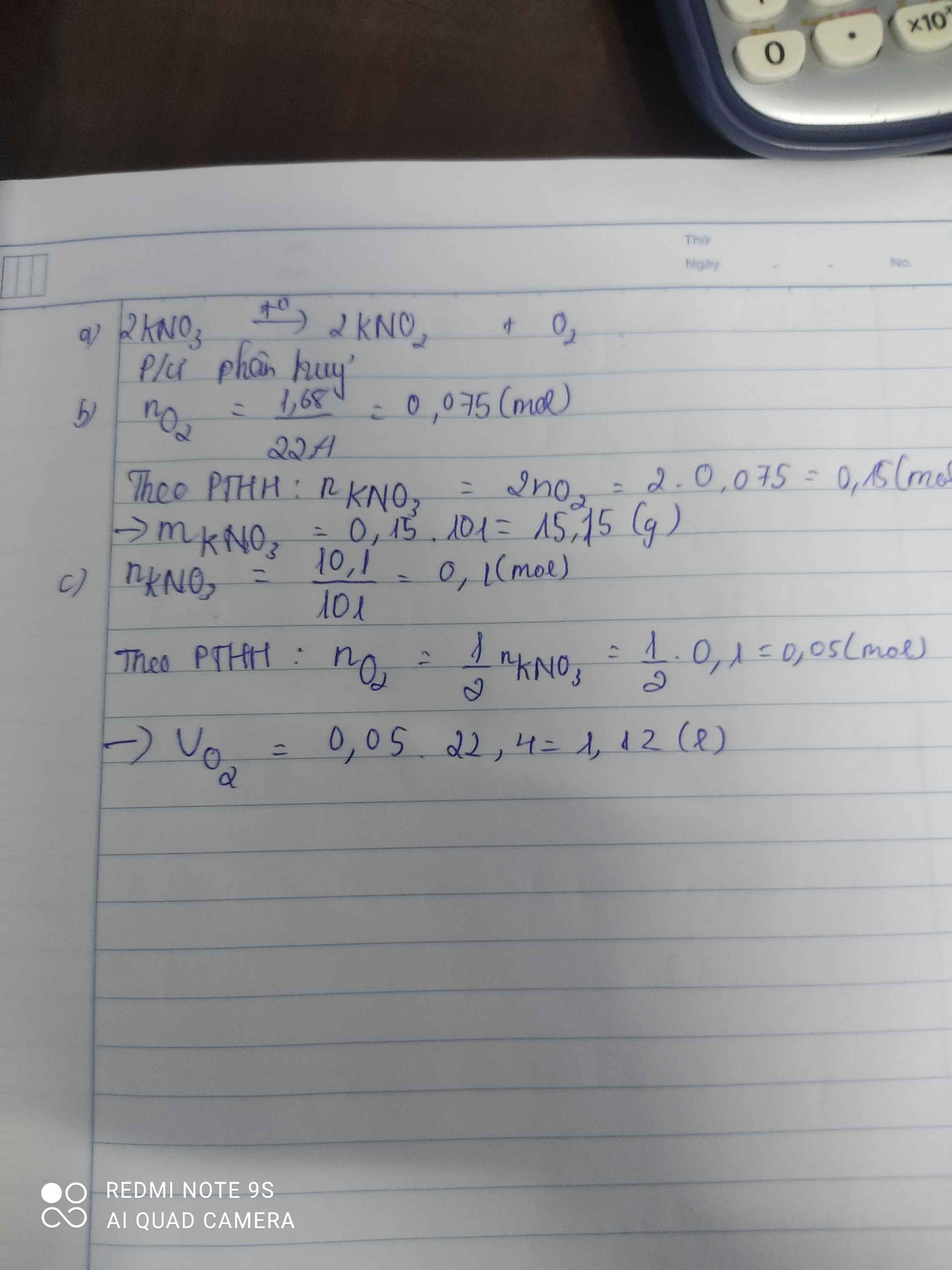


1. 2KNO3 ------> 2KNO2 + O2
2. nKNO3 = \({ 5,05{} \over 39 + 14 + 16 . 3}\) = 0,05 (mol )
PTHH: 2KNO3 ---------> 2KNO2 + O2
0,05 0,05 0,025 (mol)
=> mO2 = 0,025 . 32 = 0,8 (g)
3. nKNO2 = \({ 3,4 {} \over 39+14+16.2}\) = 0,04 (mol)
nO2 = \( {0,64{} \over 32}\) = 0,02 (mol)
PTHH: 2KNO3 ---------> 2KNO2 + O2
0,04 0,04 0,02 (mol)
=> mKNO3 = 0,04 . 101 = 4,04 (g)
*HỌC TỐT*
Em ơi, mấy cái bên dưới chị ra kết quả đúng nhưng phép tính sai bởi vì chị ko bt ấn ó. Có j em tham khảo tạm nha