Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nhh = 5.6/22.4 = 0.25(mol)
nAg2C2 = nC2H2 = 24/240 = 0.1 (mol)
nBr2 = 0.3 (mol)
=> nC2H4 = 0.3 - 0.1*2 = 0.1 (mol)
nCH4 = 0.25 - 0.1 - 0.1 = 0.05 (mol)
mCH4 = 0.05*16 = 0.8 (g)
mC2H2 = 0.1*26 = 2.6 (g)
mC2H4 = 0.1*28 = 2.8 (g)
mhh = 0.8 + 2.6 + 2.8 = 6.2 (g)
%CH4 = 0.8/6.2 * 100% = 12.9%
%C2H4 = 2.8/ 6.2 * 100% = 45.16%
%C2H2 = 41.94%

Đáp án C
C2H2 và C2H4 cho qua dd AgNO3 chỉ có C2H2 phản ứng => khí đi ra là khí C2H4
BTNT C: nC2H2 = nAg2C2 = 28,8: 240 = 0,12 (mol)
nC2H4 = 2,912 : 22,4 = 0,13 (mol)
%m C2H2 = (mC2H2 : mhh khí).100% = [ 0,12. 26 : (0,12.26 + 0,13.28)].100% = 46,15%

\(C_2H_2+AgNO_3+NH_3->C_2Ag_2+NH_4NO_3\\ CH_2=CH-CH_3+Br_2->CH_2Br-CHBr-CH_3\\ n_{C_2Ag_2}=0,325mol=n_{C_2H_2}\\ m_{C_2H_2}=8,45g\\ n_{Br_2}=n_{C_3H_6}=\dfrac{32}{160}=0,2mol\\ m_{C_3H_6}=8,4g\\ m_{CH_4}=20-8,45-8,4=3,15g\\ n_{CH_4}=0,196875mol\\ n_{hh}=n_{CH_4}+n_{C_2H_2}+n_{C_3H_6}=0,721875mol\\ \%V_{C_3H_6}=\dfrac{0,2}{n_{hh}}.100\%=27,71\%\\ \%V_{C_2H_2}=\dfrac{0,325}{n_{hh}}.100\%=45,02\%\\ \%V_{CH_{_34}}=27,27\%\)

\(C_2H_2 + 2AgNO_3 + 2NH_3 \to Ag_2C_2 + 2NH_4NO_3\\ n_{C_2H_2} = n_{Ag_2C_2} = \dfrac{7,2}{240} = 0,03(mol)\\ \Rightarrow V_{C_2H_2} = 0,03.22,4 = 0,672(lít)\\ C_2H_4 + Br_2 \to C_2H_4Br_2\\ n_{C_2H_4} = \dfrac{1,68}{28} = 0,06(mol)\\ \Rightarrow V_{C_2H_4} = 0,06.22,4 = 1,344(lít)\\ \Rightarrow V_{CH_4} = 4,032-0,672-1,344 = 2,016(lít)\)

Đáp án : A
Ta có nX=0,18 mol mà trong X chỉ có C2H2 tác dụng với AgNO3 trong NH3=>n C2H2=n kết tủa =0,03 mol.
Lại có trong X co C2H4 tác dụng với dd Br2 =>nC2H4=m ( khối lượng bình 2
tăng )=1,68:28=0,06mol
=>nCH4 = NX - nC2H4 - nC2H2 = 0,18 - 0,06 - 0,03 = 0,09 mol
=> 0,672 lít; 1,344 lít; 2,016 lít.

Đáp án : A
Ta có nX=0,18 mol mà trong X chỉ có C2H2 tác dụng với AgNO3 trong NH3=>n C2H2=n kết tủa =0,03 mol.
Lại có trong X co C2H4 tác dụng với dd Br2 =>nC2H4=m ( khối lượng bình 2
tăng )=1,68:28=0,06mol
=>nCH4 = NX - nC2H4 - nC2H2 = 0,18 - 0,06 - 0,03 = 0,09 mol
=> 0,672 lít; 1,344 lít; 2,016 lít.


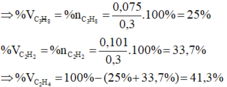
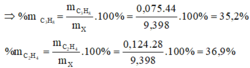
Bài 1 :
\(m_1\downarrow=m_{Ag2C2}\)
\(\Rightarrow n_{axetilen}=n_{Ag2C2}=0,1\left(mol\right)\)
\(m_{2\left(tang\right)}=m_{etilen}\)
\(\Rightarrow n_{etilen}=0,2\left(mol\right)\)
\(n_{hh}=0,6\left(mol\right)\)
\(\Rightarrow n_{metan}=0,6-0,1-0,2=0,3\left(mol\right)\)
\(\%_{CH4}=\frac{0,3.16.100}{0,3.16+0,1.26+0,2.28}=36,92\%\)
\(\%C_2H_2=\frac{0,1.26.100}{0,3.16+0,1.26+0,2.28}=20\%\)
\(\%C_{2H4}=43,08\%\)
Bài 2 :
\(n_{Br2}=0,5\left(mol\right)\)
Gọi x là nC2H2, y là nC2H4
PTHH:\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\) ( do là ankin có 2 lk pi nên td với 2 phân tử Br2)
_______x _____2x_____________________
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
y ______y____________________
Giải hệ PT:
\(\left\{{}\begin{matrix}26x+28y=11\\2x+y=0,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,3\end{matrix}\right.\)
\(m_{C2H2}=0,1.\left(12.2+2\right)=2,6\left(g\right)\)
\(m_{C2H4}=0,3.\left(12.2+4\right)=8,4\left(g\right)\)