Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1:
a, \(C_nH_{2n}+Br_2\rightarrow C_nH_{2n}Br_2\)
\(C_nH_{2n}+\dfrac{3n}{2}O_2\underrightarrow{t^o}nCO_2+nH_2O\)
\(C_3H_8+5O_2\underrightarrow{t^o}3CO_2+4H_2O\)
b, Gọi: \(\left\{{}\begin{matrix}n_{C_nH_{2n}}=x\left(mol\right)\\n_{C_3H_8}=y\left(mol\right)\end{matrix}\right.\) \(\Rightarrow x+y=\dfrac{15,68}{22,4}=0,7\left(1\right)\)
Có: \(n_{CO_2}=n.n_{C_nH_{2n}}+3n_{C_3H_8}=nx+3y=\dfrac{40,32}{22,4}=1,8\left(2\right)\)
Mà: m bình tăng = 16,8 (g) = mCnH2n = 14nx (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}nx=1,2\\x=0,5\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
⇒ n = 1,2:0,5 = 2,4
Mà: 2 anken đồng đẳng kế tiếp.
→ C2H4 và C3H6.
Có: \(\left\{{}\begin{matrix}28n_{C_2H_4}+42n_{C_3H_6}=16,8\\n_{C_2H_4}+n_{C_3H_6}=0,7-0,2\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_4}=0,3\left(mol\right)\\n_{C_3H_6}=0,2\left(mol\right)\end{matrix}\right.\)
%n cũng là %V ở cùng điều kiện nhiệt độ, áp suất.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,3}{0,7}.100\%\approx42,86\%\\\%V_{C_3H_6}=\%V_{C_3H_8}=\dfrac{0,2}{0,7}.100\%\approx28,57\%\end{matrix}\right.\)
Bài 2:
a, \(n_{CO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(n_{H_2O}=\dfrac{6,48}{18}=0,36\left(mol\right)\)
\(\Rightarrow n_X=0,6-0,35=0,24\left(mol\right)\)
\(\Rightarrow\overline{C}=\dfrac{0,6}{0,24}=2,5\)
Mà: 2 ankin hơn kém nhau 2 C và số C nhỏ nhất có thể có là 2.
→ C2H2 và C4H6.
CTCT: C2H2: \(CH\equiv CH\)
C4H6: \(CH\equiv C-CH_2-CH_3\) hoặc \(CH_3-C\equiv C-CH_3\)
b, BTNT C, có: \(2n_{C_2H_2}+4n_{C_4H_6}=n_{CO_2}=0,6\left(1\right)\)
BTNT H, có: \(2n_{C_2H_2}+6n_{C_4H_6}=2n_{H_2O}=0,36.2\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_2}=0,18\left(mol\right)\\n_{C_4H_6}=0,06\left(mol\right)\end{matrix}\right.\)
C2H2 luôn pư với AgNO3/NH3.
Ta có: \(n_{Ag_2C_2}=n_{C_2H_2}=0,18\left(mol\right)\Rightarrow m_{Ag_2C_2}=0,18.240=43,2\left(g\right)=m_{\downarrow}\)
→ C4H6 không pư.
Vậy: CTCT đúng của 2 chất là: \(CH\equiv CH\) và \(CH_3-C\equiv C-CH_3\)

Đặt lượng C x H y là a mol, lượng C x + 1 H y + 2 là b mol.
Ta có : a + b = 0,05 (1)
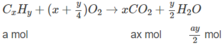
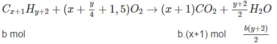
Số mol C O 2 : ax + b(x + 1) = 0,170 (2)
Số mol
H
2
O
: 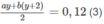
Từ (2) ta có (a + b)x + b = 0,170 ;
b = 0,170 - 0,0500x
b là số mol của một trong hai chất nên 0 < b < 0,0500.
Do đó 0 < 0,170 - 0,0500x < 0,0500 ⇒ 2,40 < x < 3,40 ⇒ x
= 3.
⇒ b = 0,1700 - 0,0500.3 = 0,0200 ⇒ a = 0,0500 - 0,0200 =


Ta có: \(n_{O_2\left(banđau\right)}=\dfrac{62}{32}=2\left(mol\right)\)
\(n_{CO_2}=n_{CaCO_3}=\dfrac{100}{100}=1\left(mol\right)\)
Khí thoát ra khỏi bình là O2 dư.
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{pV}{RT}=\dfrac{0,4.11,2}{0,082.273}=0,2\left(mol\right)\)
\(\Rightarrow n_{O_2\left(pư\right)}=2-0,2=1,8\left(mol\right)\)
BTNT O, có: \(2n_{O_2\left(pư\right)}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=2.1,8-2.1=1,6\left(mol\right)\)
Vì đốt cháy 2 hiđrocacbon thu được nH2O > nCO2 nên A và B là ankan.
⇒ nankan = 1,6 - 1 = 0,6 (mol)
Gọi CTPT chung của A và B là \(C_{\overline{n}}H_{2\overline{n}+2}\)
\(\Rightarrow\overline{n}=\dfrac{1}{0,6}=1,667\)
Vậy: A và B là CH4 và C2H6.
Bạn tham khảo nhé!

\(n_{CO_2}=\dfrac{48,4}{44}=1,1\left(mol\right)\\ n_{H_2O}=\dfrac{29,7}{18}=1,65\left(mol\right)\\ Vì:n_{H_2O}>n_{CO_2}\Rightarrow hhZ:hh.ankan\\ CTTQ:C_aH_{2a+2}\\ Ta.có:1< \dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{1,65}{1,1}=1,5< 2\\ \Rightarrow hh.Z:50\%V_{CH_4},50\%V_{C_2H_6}\\ \Rightarrow\%m_{\dfrac{CH_4}{hhZ}}=\dfrac{16}{16+28}.100\approx36,364\%\\ \Rightarrow\%m_{\dfrac{C_2H_6}{hhZ}}\approx63,636\%\)

Đáp án C
nX =0,4 mol
Khối lượng bình 1 đựng P2O5 tăng là số lượng của H2O.
Khối lượng bình đựng KOH rắn tăng chính là khối lượng của CO2
Khi đốt cháy 1 anken ta luôn có: ![]()
![]()
![]()
![]() anken là C3H6 và C4H8
anken là C3H6 và C4H8
Gọi phần trăm thể tích về thể tích của C3H6 là x% thì phần trăm thể tích về thể tích của C4H8 là
(100 -x) %
Ta có:
![]()
![]()

$n_{H_2O} = \dfrac{5,22}{18} = 0,29(mol)$
$2KOH + CO_2 \to K_2CO_3 + H_2O$
$n_{CO_2} = \dfrac{9,24}{44} = 0,21(mol)$
Ta có :
$n_{ancol} = n_{H_2O} - n_{CO_2} = 0,29 - 0,21 = 0,08(mol)$
Gọi CT hai ancol là $C_nH_{2n+1}OH$
Suy ra $n = n_{CO_2} : n_{ancol} = 0,21 : 0,08 = 2,625$
Vậy hai ancol là $C_2H5OH(a\ mol) ; C_3H_7OH(b\ mol)$
Ta có :
a + b = 0,08
$n_{CO_2} = 2a + 3b = 0,21$
Suy ra a = 0,03 ; b = 0,05
Suy ra : m = 0,03.46 + 0,05.60 = 4,38(gam)
\(CT:C_{\overline{n}}H_{2\overline{n}+2}O\)
\(m_{\text{bình 1 tăng}}=m_{H_2O}=5.22\left(g\right)\)
\(\Rightarrow n_{H_2O}=\dfrac{5.22}{18}=0.29\left(mol\right)\)
\(m_{\text{bình 2 tăng}}=m_{CO_2}=5.22\left(g\right)\)
\(\Rightarrow n_{CO_2}=\dfrac{9.24}{44}=0.21\left(mol\right)\)
\(TC:\)
\(\dfrac{\overline{n}}{2\overline{n}+2}=\dfrac{0.21}{0.29\cdot2}\)
\(\Leftrightarrow n=2.625\)
\(CTPT:C_2H_5OH.C_3H_7OH\)
\(n_{ancol}=n_{H_2O}-n_{CO_2}=0.29-0.21=0.08\left(mol\right)\)
\(\Rightarrow n_{O\left(ancol\right)}=0.08\left(mol\right)\)
\(m_{hh}=m_C+m_H+m_O=0.21\cdot12+0.29\cdot2+0.08\cdot16=4.38\left(g\right)\)

a) \(n_{O_2}=\dfrac{21,056}{22,4}=0,94\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{52}{100}=0,52\left(mol\right)\)
BTNT C: \(n_C=n_{CO_2}=n_{CaCO_3}=0,52\left(mol\right)\)
BTNT O: \(n_{H_2O}=2n_{O_2}-2n_{CO_2}=0,84\left(mol\right)\)
\(\Rightarrow n_{ankan}=n_{H_2O}-n_{CO_2}=0,32\left(mol\right)\)
\(\Rightarrow\text{Số }\overline{C}_{\text{trung bình}}=\dfrac{n_C}{n_{ankan}}=\dfrac{0,52}{0,32}=1,625\)
Vì 2 ankan liên tiếp nhau trong dãy đồng đẳng nên 2 ankan là CH4 (metan) và C2H6 (etan)
b) BTNT H: \(n_H=2n_{H_2O}=1,68\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_6}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_C=n_{CH_4}+2n_{C_2H_6}=a+2b=0,52\\n_H=4n_{CH_4}+6n_{C_2H_6}=4a+6b=1,68\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,12\\b=0,2\end{matrix}\right.\left(TM\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,12.16}{0,12.16+0,2.30}.100\%=24,24\%\\\%m_{C_2H_6}=100\%-24,24\%=75,76\%\end{matrix}\right.\)
c)
\(CH_4+Cl_2\xrightarrow[]{askt}CH_3Cl\left(\text{metyl clorua}\right)+HCl\\ C_2H_6+Cl_2\xrightarrow[]{askt}C_2H_5Cl\left(\text{etyl clorua}\right)+HCl\)



bài 1
Đốt cháy hoàn toàn V lít (đktc) hỗn hợp 2 hidrocacbon là đồng đẳng liên tiếp nhau, sản phẩm cháy thu được có tỉ lệ thể tích CO2 và H2O là 12 : 23. Tìm CTPT và % thể tích của mỗi hidrocacbon
Ta có nCO2nCO2 < nH2OnH2O ---> hỗn hợp gồm hai hidrocacbon no, mạch hở
Cx¯H2x¯+2
ta có : x¯/12=x¯+1/23---> x¯=1,1
hỗn hợp gồm: CH4, C2H6
Tính % thì dùng sơ đồ đường chéo
C1------------------0,9
---------1,1----------
C2------------------0.1
CH4: 90%
C2H6: 10%
bài 2
Đốt cháy hoàn toàn 29,2g hỗn hợp 2 ankan A và B. Sản phẩm sinh ra cho vào dung dịch Ba(OH) 2 thấy khối
lượng bình tăng thêm 134,8g.
a. Tính khối lượng CO2 và H2O tạo thành khi đốt 2 ankan.
b. Nếu A, B là đồng đẳng kế tiếp, tìm CTPT A,B.
a) Gọi a,b lần lượt là số mol CO2, H2O
=> 44a + 18b = 134,8 (1)
Ta có : nC = nCO2 = a mol; nH = 2nH2O = 2b mol
=> 12a + 2b = 29,2 (2)
(1),(2) => a = 2; => mCO2 = 88g
b = 2,6 => m H2O = 46,8g
b,m oxi phản ứng là 134,8 - 29,2 = 105,6
số mol của oxi là : 105,6/32 =3,3 mol
gọi cong thức chung của 2 ankan là CnH2n+2 +(3n+1)/2 O2 => nCO2 + (n+1) H2O
số mol của CnH2n+2 = 3,3 chia cho (3n+1)/2 =6,6/(3n+1)
=> (14n +2) x 6,6/(3n+1) =29,2
=> n =3,3
=> C3H8 và C4H10
Bài 3 :
Theo đề bài ta có : nH2O = 10,8/18 = 0,6 (mol) ; nCO2 = 15,4/44 = 0,35 (mol) ;nhh=0,25(mol)
ta thấy : nH2O > nCO2 => 2 hidroccacbon là ankan
=> số \(\overset{_-}{C}\) = 0,35/0,25 = 1,4 => 2 ankan là CH4(x) và C2H6(y)
Theo BTNT C có : x + 2y = 0,35 ;(1)
Thep BTNT H có : 2x + 3y = 0,6 ;(2)
từ (1) và (2) => x = 0,15;y=0,1 => %VCH4 = (0,15/0,25).100=60%;%VC2H6=40%