Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cô @Cẩm Vân Nguyễn Thị, đề có vài chỗ sai em đã sửa lại. Mong cô giúp đỡ.
Đề này sai số liệu hay sai thông tin?
Đề yêu cầu là: Tính khối lượng m và B.
Và B nghĩa là như thế nào?

1/ nNaCl=5,85/58,5=0,1 mol.
nAgNO3=34/170=0,2 mol.
PTPU: NaCl+AgNO3=>AgCl+NaNO3
vì NaCl và AgNO3 phan ung theo ti le 1:1 (nAgNO3 p.u=nNaCl=0,1 mol)
=>AgNO3 du
nAgNO3 du= 0,2-0,1=0,1 mol.
Ta tinh luong san pham theo chat p.u het la NaCl
sau p.u co: AgNO3 du:0,1 mol; AgCl ket tua va NaCl: nAgCl=nNaNO3=nNaCl=0,1 mol.V(dd)=300+200=500ml=0,5 ()l
=>khoi lg ket tua: mAgCl=0,1.143,5=14,35 g
C(M)AgNO3=C(M)NaNO3=n/V=0,1/0,5=0,2 M

Câu 1:
Khối lượng CaO: 
Số mol CaO:
Pt:
 số mol Ca (OH)2
số mol Ca (OH)2
Vậy khối lượng Ca(OH)2tạo thành: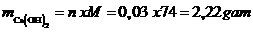
Vậy mct = 2,22 gam
 Mà
Mà 
Vậy nồng độ phần trăm Ca(OH)2: 
Câu 2:
+ Khối lượng riêng  khối lượng dd H2SO4 là
khối lượng dd H2SO4 là 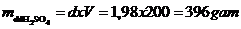
+ 
Số mol CuO: 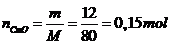
 Pt:
Pt: 

 Khối lượng
Khối lượng 
Vậy khối lượng chất tan: mct = 24 gam
Mà 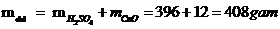
Vậy nồng độ phần trăm: 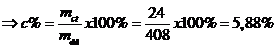

Cô @Cẩm Vân Nguyễn Thị ơi. Giúp em bài này với. Bài này có vài chỗ em không hiểu được.

1.
2Cu +O2 -to-> 2CuO
vì khi cho A vào dd H2SO4 đặc nóng có khí C => A :Cu dư,CuO,Ag
CuO +H2SO4đặc nóng --> CuSO4+H2O
Cu +2HSO4đặc nóng --> CuSO4 +SO2 +2H2O
dd B:CuSO4
khí C:SO2
2KOH +SO2 --> K2SO3+H2O
KOH +SO2-->KHSO3
dd D:K2SO3,KHSO3
BaCl2+K2SO3 --> BaSO3 +2KCl
2NaOH +2KHSO3 --> Na2SO3 +K2SO3 +2H2O
sai rồi Cu không dư , ag phản ứng với H2SO4 đặc nóng
2Ag + 2H2SO4 đặc = Ag2SO4 + SO2 +2 H2O
nSO3 = \(\frac{1,2}{80}\) = 0,015 (mol)
SO3 + H2O \(\rightarrow\) H2SO4
0,015 -----------> 0,015 (mol)
a) C%(H2SO4) = \(\frac{0,015.98}{100}\) . 100% = 1,47%
b) nMgO = \(\frac{5}{40}\) = 0,125 (mol)
PT: MgO + H2SO4 \(\rightarrow\) MgSO4 + H2O
bđ 0,125 .... 0,015 (mol)
pư 0,015\(\leftarrow\) 0,015 \(\rightarrow\) 0,015 (mol)
spư 0,1125 .... 0 .............. 0,015 (mol)
Sau pư, MgO dư
mMgO = 0,1125 . 40 = 4,5 (g)
c) m dd spư = 5 + 100 - 4,5 = 100,5 (g)
C% (MgSO4)= \(\frac{0,015.120}{100,5}\) . 100% = 1,8%
thanks bạn nha