Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3. Khối lượng mol của hợp chất đó là :
2.28 = 56 (g/mol)
mC = \(\frac{56.85,7}{100}\approx48\left(g\right)\)
mH = 56 - 48 = 8 (g)
nC = \(\frac{48}{12}=4\left(mol\right)\)
nH = \(\frac{8}{1}=8\left(mol\right)\)
Vậy công thức hóa học là C4H8.

Chọn A
Công thức oxit ứng với hóa trị cao nhất của R là R 2 O 5
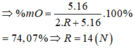
Dạ cho em hỏi là 74,07 phần trăm suy ra như thế nào vậy ạ? Em cảm ơn.

1/Đặt Z, N lần lượt là số hạt p, n có trong nguyên tử M
ta có hệ phương trình
\(\begin{cases}2Z+N=79+3\\2Z-N=19+3\end{cases}\)\(\Rightarrow\begin{cases}Z=26\\N=30\end{cases}\)
a. Cấu hình electron nguyên tử của M là: 1s22s22p63s23p63d64s2
M ở ô thứ 26, chu kì 4 nhóm VIIIB trong bảng tuần hoàn.
b. Cấu hình electron của ion Fe2+ là: 1s22s22p63s23p63d6
Cấu hình electron của ion Fe3+ là: 1s22s22p63s23p63d5
2.
Vì R tạo được hợp chất khí với H nên R là phi kim.
Giả sử R thuộc nhóm x (x\(\ge\)4).
Theo giả thiết
công thức của R với H là RH8-x \(\Rightarrow\)a=\(\frac{R}{R+8-x}.100\)
công thức oxit cao nhất của R là R2Ox
\(\Rightarrow\) b=\(\frac{2R}{2R+16x}.100\) \(\Leftrightarrow\) b= \(\frac{R}{R+8x}.100\)
suy ra \(\frac{a}{b}=\frac{R+8x}{R+8-x}=\frac{11}{4}\)\(\Leftrightarrow R=\frac{43x-88}{7}\)
Xét bảng
x R 4 5 6 7 12 có C 18,14 loại 24,28 loại 30,42 loại
a/ Vậy R là C
b/
Công thức của R với H là CH4
Công thức electron C : H : H : H : H ; Công thức cấu tạo C - H - - - H H H
Oxti cao nhất của R là CO2
Công thức electron O:: C ::O; Công thức cấu tạo O=C=O
c.
Trong hợp chất CH4 có \(\Delta\chi=\chi_C-\chi_H\)=2,55-0,22=0,35<0,4 nên liên kết giữa C-H là liên kết cộng hóa trị không cực
Trong hợp chất CO2 có 0, \(\Delta\chi=\chi_O-\chi_C\) =3,44-2,55=0,89
\(\Rightarrow\) 0,4<\(\Delta\chi=0,89\)<1,7 nên liên kết giữa C=O là liên kết cộng hóa trị phân cực

Gọi CTHH là \(Na_xS_yO_z\)
\(x:y:z=\dfrac{\%Na}{23}:\dfrac{\%S}{32}:\dfrac{\%O}{16}=\dfrac{32,4}{23}:\dfrac{22,54}{32}:\dfrac{45,1}{16}=1,41:0,74:2,82=2:1:4\)Vậy CTĐGN(công thức đơn giản nhất) là \(Na_2SO_4\)
Lại có: \(M_X=142đvC\)\(\Rightarrow\left(Na_2SO_4\right)_n=142\Rightarrow n=1\)
Vậy CTHH là \(Na_2SO_4\)

a) Vì 2 nguyên tố có tổng số proton là 32
=> 2 nguyên tố thuộc chu kì nhỏ
Gọi 2 nguyên tố cần tìm trong A là X, Y
Vì hợp chất A tạo bởi 3 nguyên tử của 2 nguyên tố thuộc cùng 1 nhóm, ở 2 chu kì liên tiếp => CT của A : XY2
Ta có : \(\left\{{}\begin{matrix}Z_X+2Z_Y=32\\\left|Z_X-Z_Y\right|=8\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}Z_X=16\left(S\right)\\Z_Y=8\left(O\right)\end{matrix}\right.\)
=> CTPT của hợp chất : SO2
CT cấu tạo :
SO2 là liên kết cộng hóa trị có cực
b) Lưu huỳnh đioxit (SO2) mang đầy đủ tính chất hóa học của một oxit axit.
Tính chất hóa học của SO2:
- Tác dụng với nước tạo thành dung dịch axit.
Ví dụ: SO2 + H2O → H2SO3
- Tác dụng với dung dịch bazơ tạo thành muối và nước.
Ví dụ: SO2 + 2NaOH → Na2SO3 + H2O
- Tác dụng với oxit bazơ tạo thành muối.
Ví dụ: SO2 + Na2O → Na2SO3

a)
Do R thuộc nhóm VA
=> CTHH của R và H là: RH3
Có \(\dfrac{3}{M_R+3}.100\%=17,64\%=>M_R=14\left(g/mol\right)\)
=> R là N
b) Do CTHH của R và H là RH3
=> oxit cao nhất của R là R2O5
Có: \(\dfrac{16.5}{2.M_R+16.5}.100\%=74,07\%=>M_R=14\left(g/mol\right)\)
=> R là N


1. Gọi CTHH là R2(SO4)3
\(2MR+96.3=400\Rightarrow M_R=56\left(\frac{g}{mol}\right)\)
Vậy R là Sắt (Fe)
2. Gọi CTHH là MgxSyOz
\(x:y:z=\frac{20}{24}:\frac{26,7}{32}:\frac{53,3}{16}=1:1:4\)
Vậy CTHH là MgSO4
3. Gọi CTHH là HxOy
\(x:16y=1:8\Leftrightarrow x:y=1:2\)
Vậy CTHH là H2O