Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a/300ml=0,3l;
200ml=0,2l;
nHCl=0,3*1=0,3(mol)
nNaOH =0,2*0,5=0,1(mol)
PTHH NaOH + HCl =>NaCl + H2O
theo PT 1 mol 1mol 58,5 (g)
theo đề 0,1 mol 0,3 mol x(g)
xét tỉ lệ \(\dfrac{0,1}{1}< \dfrac{0,3}{1}\) => NaOH hết và HCl dư mọi tính toán phụ thuộc vào chất hết NaOH
mNaOH = x = (0,1*58,5)/1=5,85 (g)
b/muồn phản ứng trên xảy ra hoàn toàn thì phải thêm vào dung dịch NaOH 0,5M vì nNaOH < nHCl
=> nNaOH thêm vào là 0,2 mol=> thể tích của dung dịch NaOH 0,5M thêm vào là : V=0,2/0,5=0,4 l
c/Trong trường hợp phản ứng xảy ra hoàn toàn thì khối lượng muối tạo thành là : mNaCl = (0,3*58,5)/1=17,55(g)

\(a)n_{NaOH}=0,5.0,2=0,1mol\\ n_{H_2SO_4}=0,3.1=0,3mol\\2 NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ \Rightarrow\dfrac{0,1}{2}< \dfrac{0,3}{1}\Rightarrow H_2SO_4.dư\\ 2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,1 0,05 0,05 0,1
\(C_M\) \(_{Na_2SO_4}=\dfrac{0,05}{0,2+0,3}=0,1M\)
\(C_M\) \(_{H_2SO_4}=\dfrac{0,3-0,05}{0,2+0,3}=0,5M\)
b) Vì H2SO4 dư nên quỳ tím hoá đỏ.

nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
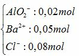 + V ml HCl 1M→ Al(OH)3: 0,01 (mol)
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)

1. Cho 200g dung dịch NaOH 20% tác dụng vừa hết với 100g dung dịch HCl. Tính:
a) Nồng độ muối thu được sau phản ứng?
b) Tính nồng độ axit HCl. Biết phản ứng xảy ra hoàn toàn?
---
a) mNaOH=20%.200=40(g) -> nNaOH=40/40=0,1(mol)
PTHH: NaOH + HCl -> NaCl + H2O
Ta có: nNaCl=nHCl=nNaOH=1(mol)
=> mNaCl=1.58,5=58,5(g)
mddNaCl=mddNaOH + mddHCl= 200+100=300(g)
=>C%ddNaCl= (58,5/300).100=19,5%
b) mHCl=0,1. 36,5=36,5(g)
=> C%ddHCl=(36,5/100).100=36,5%
2. Hòa tan hoàn toàn 11,2g sắt cần vừa đủ V(l) dung dịch HCl 0,2M sau phản ứng thu được dung dịch A và X (lít) H2(đktc).
a) Tìm V?
b) Tìm X?
c) Tính CM của muối thu được trong dung dịch A?
---
a) nFe=0,2(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
0,2_____0,4______0,2___0,2(mol)
a) V=VddHCl= nHCl/CMddHCl= 0,4/0,2=2(l)
b) V(H2,đktc)=0,2.22,4=4,48(l)
c) Vddmuoi=VddHCl=2(l)
CMddFeCl2= (0,2/2)=0,1(M)
Chúc em học tốt!

\(a,2NaOH+MgSO_4\rightarrow Mg\left(OH\right)_2+Na_2SO_4\\ n_{NaOH}=0,5.1=0,5\left(mol\right)\\ b,n_{Mg\left(OH\right)_2}=\dfrac{0,5}{2}=0,25\left(mol\right)=n_{Na_2SO_4}\\ m_{kt}=m_{Mg\left(OH\right)_2}=58.0,25=14,5\left(g\right)\\ c,V_{ddX}=V_{ddNaOH}+V_{ddMgSO_4}=0,5+0,5=1\left(l\right)\\ C_{MddNa_2SO_4}=\dfrac{0,25}{1}=0,25\left(M\right)\)

\(n_{NaOH}=0,5.0,02=0,01\left(mol\right)\)
\(n_{HCl}=1.0,3=0,3\left(mol\right)\)
\(Pt:NaOH+HCl\rightarrow NaCl+H_2O\)
0,01 mol 0,3mol\(\rightarrow0,01mol\)
Lập tỉ số: nNaOH : nHCl = 0,01 < 0,3
\(\Rightarrow\) NaOH hết; HCl dư
\(m_{NaCl}=0,01.58,5=0,585\left(g\right)\)
\(n_{HCl\left(dư\right)}=0,3-0,01=0,29\left(mol\right)\)
\(C_{M_{HCl\left(Dư\right)}}=\dfrac{0,29}{0,3}=1M\)
Theo đề bài ta có :
nNaOH=0,5.0,02=0,01 mol
nHCl=1.0,3=0,3 mol
Ta có PTHH :
2NaOH + 2HCl -> 2NaCl + 2H2O
0,01mol....0,01mol....0,01mol
Ta có tỉ lệ :
nNaOH=\(\dfrac{0,01}{2}mol< nHCl=\dfrac{0,3}{2}mol\)
=> nHCl dư ( tính theo nNaOH )
a) mNaCl=0,01.58,5=0,585 g
b) Nồng độ mol của chất tan dung dịch sau p/ư là :
CMNaCl = 0,01/0,02=0,5(M)
c) Muốn p/ư xẩy ra hoàn toàn thì cần phải thêm số ml dd NaOH 0,5M là :
VddNaOH=\(\dfrac{0,01}{0,5}=0,02\left(l\right)=20\left(ml\right)\)
Vậy .....