Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

. Do trộn 100g với 100g mà lượng dung dịch thu được < 200g thì muối sunfat kim loại là muối axit.( do sự thất thoát khí )
pt : 2MHSO4 + 2NaHCO3 = M2SO4 + Na2SO4 + 2CO2 + 2H2O
Sự thoát khí CO2 làm giảm khối lượng ( số mol CO2 = số mol NaHCO3 0,05mol)
gọi số mol của MHSO4 là x ta có:
(M + 97) x = 13,2 => x = 13,2/ (M + 97)
Theo phương trình sự tạo kết tủa với BaCl2 là muối sunfat:
MNaSO4 + BaCl2 = BaSO4 + MCl + NaCl
=> Với 0,1 < x < 0,1 + 0,02 thì 13< M < 35 thoả mãn Na = 23 Vậy công thức sunfat là NaHSO4

a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
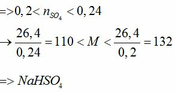
b)
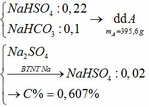
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O


BTKL: mD + mNaHCO3 = mCO2 + mE
mD + 179,88 = 44.0,2 + 492 => mD = 320,92
BTKL: mMg + mddHCl = mH2 + mD
=> 24 . 0,4 + mddHCl = 2 . 0,4 + 320,92 => mddHCl = 312,12
=> C%HCl = 11,69%

bài 1
a. -hòa tan 3 kl trên vào dd NaOH dư
+tan => Al
2NaOH +2 Al + 2H2O => 2NaAlO2 + 3H2
+ko tan => Fe,Cu
- hòa tan 2 kim loại trên trong HCl dư
+tan => Fe
Fe + 2HCl=> FeCl2 + H2
+ko tan => Cu
b.
hòa tan hh trên vào NaOH dư
+tan => Al
+ko tan => Fe,Ag
-hòa tan 2 KL còn lại trong HCl
+tan=> Fe
+ko tan=> Ag
câu C
hòa tan các KL trên vào nước
+tan, có khí thoát ra => Na
Na + H2O =>. NaOH + 1/2H2
+ko tan => Al,Fe,Cu
hòa tan 3 kl còn lại trong NaOH dư
+tan => Al
+ko tan => Fe,Cu
hòa tan 2 kl còn lại vào HCl dư
+tan => Fe
+ko tan =.> Cu
câu d
hòa tan hh trên trong NaOh dư
+tan ,có khí => Al
NaOh + Al + H2o => NaAlO2 + 3/2H2
+tan => Al2O3
2NaOh + Al2o3 => 2NaAlO2 + H2O
+ko tan => Mg

Câu 1:
PTHH: 2Al + 3H2SO4 ===> Al2(SO4)3 + 3H2
a)Vì Cu không phản ứng với H2SO4 loãng nên 6,72 lít khí là sản phẩm của Al tác dụng với H2SO4
=> nH2 = 6,72 / 22,4 = 0,2 (mol)
=> nAl = 0,2 (mol)
=> mAl = 0,2 x 27 = 5,4 gam
=> mCu = 10 - 5,4 = 4,6 gam
b) nH2SO4 = nH2 = 0,3 mol
=> mH2SO4 = 0,3 x 98 = 29,4 gam
=> Khối lượng dung dịch H2SO4 20% cần dùng là:
mdung dịch H2SO4 20% = \(\frac{29,4.100}{20}=147\left(gam\right)\)
nH2 = 6.72 : 22.4 = 0.3 mol
Cu không tác dụng với H2SO4
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
0.2 <- 0.3 <- 0.1 <- 0.3 ( mol )
mAl = 0.2 x 56 = 5.4 (g)
mCu = 10 - 5.4 = 4.6 (g )
mH2SO4 = 0.3 x 98 = 29.4 ( g)
mH2SO4 20% = ( 29.4 x100 ) : 20 = 147 (g)

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

nH2=\(\frac{6,72}{22,4}=0,3\)mol
PTHH
M+2HCl--> MCl2+H2
0,3mol<---------------0,3mol
=>MM=\(\frac{19,5}{0,3}=64\)
=> km loại là kẽm (Zn)
b) nNaOH=0,2.1=0,2 mol
PTHH
NaOH+HCl-->NaCl + H2O
0,2 mol--> 0,2 mol
---> thể tích HCl 1M đã dùng là V=\(\frac{0,2+0,3}{1}=0,5\)lít
=> CM(ZnCl2)=\(\frac{0,3}{0,5}=0,6M\)



trần hữu tuyển
Bài 1:muối Sunfat của KL kiềm làm sao mà tác dụng dc với NaHCO3