Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 24:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:A+2HCl\rightarrow ACl_2+H_2\uparrow\)
Theo pthh: nA = nH2 = 0,15 (mol)
=> MA = \(\dfrac{3,6}{0,15}=24\left(\dfrac{g}{mol}\right)\)
=> A là Mg
Bài 25:
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\\ PTHH:2A+6HCl\rightarrow2ACl_3+3H_2\uparrow\\ Mol:0,3\leftarrow0,9\leftarrow0,3\leftarrow0,45\\ \rightarrow\left\{{}\begin{matrix}M_A=\dfrac{8,1}{0,3}=27\left(\dfrac{g}{mol}\right)\Rightarrow A:Al\\m_{HCl}=0,9.36,5=32,85\left(g\right)\end{matrix}\right.\)
Bài 24.
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_A=\dfrac{3,6}{M_A}\) mol
\(A+2HCl\rightarrow ACl_2+H_2\)
0,15 0,15 ( mol )
\(\Rightarrow\dfrac{3,6}{M_A}=0,15mol\)
\(\Leftrightarrow M_A=24\) ( g/mol )
=> A là Magie ( Mg )
Bài 25.
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45mol\)
\(n_A=\dfrac{8,1}{M_A}\) mol
\(2A+6HCl\rightarrow2ACl_3+3H_2\)
0,3 0,45 ( mol )
\(\Rightarrow\dfrac{8,1}{M_A}=0,3\)
\(\Leftrightarrow M_A=27\) g/mol
=> A là nhôm ( Al )

Gọi hóa trị của kim loại R là x (x > 0)
n H2 = 2,912/22,4 = 0,13 (mol)
PTPƯ: 2R + 2xH2O -> 2R(OH)x + xH2
Theo ptpư: n R = 2/x n H2 = 2/x . 0,13 = 0,26/x (mol)
M R = m R/n R = 5,98/(0,26/x) = 23x
Với x=1 -> R = 23 (Na)

Gọi nFe=a(mol);nM=b(mol)⇒56a+Mb=9,6(1)
Fe+2HCl→FeCl2+H2
M+2HCl→MCl2+H2
nH2=a+b=0,2⇒a=0,2−b
Ta có :
56a+Mb=9,656a+Mb=9,6
⇔56(0,2−b)+Mb=9,6
⇔Mb−56b=−1,6
⇔b(56−M)=1,6
⇔b=1,656−M
Mà 0<b<0,20<b<0,2
Suy ra : 0<1,656−M<0,20<1,656−M<0,2
⇔M<48(1)
M+2HCl→MCl2+H2
nM=nH2<5,622,4=0,25
⇒MM>4,60,25=18,4
+) Nếu M=24(Mg)
Ta có :
56a+24b=9,656a+24b=9,6
a+b=0,2a+b=0,2
Suy ra a = 0,15 ; b = 0,05
mFe=0,15.56=8,4(gam)
mMg=0,05.24=1,2(gam)
+) Nếu M=40(Ca)
56a+40b=9,656a+40b=9,6
a+b=0,2
Suy ra a = b = 0,1
mCa=0,1.40=4(gam)
mFe=0,1.56=5,6(gam)

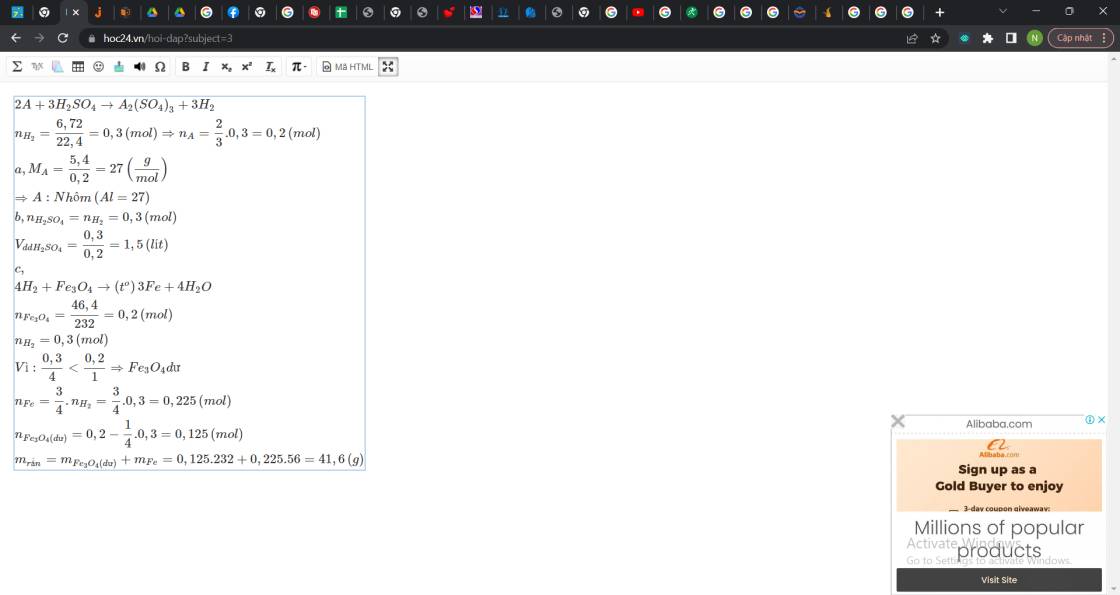
\(2A+3H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3H_2\\ n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\Rightarrow n_A=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ a,M_A=\dfrac{5,4}{0,2}=27\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Nhôm\left(Al=27\right)\\ b,n_{H_2SO_4}=n_{H_2}=0,3\left(mol\right)\\ V_{ddH_2SO_4}=\dfrac{0,3}{0,2}=1,5\left(lít\right)\\ c,\\ 3H_2+Fe_2O_3\rightarrow\left(t^o\right)2Fe+3H_2O\\ n_{Fe_3O_4}=\dfrac{46,4}{232}=0,2\left(mol\right)\\ n_{H_2}=0,3\left(mol\right)\\ Vì:\dfrac{0,3}{3}< \dfrac{0,2}{1}\Rightarrow Fe_3O_4dư\\ n_{Fe}=\dfrac{2}{3}.n_{H_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ n_{Fe_3O_4\left(dư\right)}=0,2-\dfrac{1}{3}.0,3=0,1\left(mol\right)\\ m_{rắn}=m_{Fe_3O_4\left(dư\right)}+m_{Fe}=0,1.232+0,2.56=34,4\left(g\right)\)

\(a,A+2HCl\rightarrow ACl_2+H_2\\ n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\Rightarrow n_A=n_{H_2}=0,15\left(mol\right)\\ \Rightarrow M_A=\dfrac{3,6}{0,15}=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow A\left(II\right):Magie\left(Mg=24\right)\\ b,Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{H_2}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\\ Vì:\dfrac{0,15}{1}< \dfrac{0,4}{2}\Rightarrow HCldư\\ \Rightarrow Sau.p.ứ:MgCl_2,HCldư\\ n_{MgCl_2}=n_{Mg}=0,15\left(mol\right)\\ \Rightarrow m_{MgCl_2}=95.0,15=14,25\left(g\right)\\ n_{HCl\left(dư\right)}=0,4-0,15.2=0,1\left(mol\right)\\ \Rightarrow m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\\ m_{chất.sau}=3,65+14,25=17,9\left(g\right)\)

Bài 1:
Gọi KL cần tìm là A.
PT: \(A+2HCl\rightarrow ACl_2+H_2\)
Ta có: \(n_{HCl}=0,1.6=0,6\left(mol\right)\)
Theo PT: \(n_A=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{7,2}{0,3}=24\left(g/mol\right)\)
Vậy: KL cần tìm là Mg.
Bài 2:
PT: \(2R+6HCl\rightarrow2RCl_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{9,408}{22,4}=0,42\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{3}n_{H_2}=0,28\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{7,56}{0,28}=27\left(g/mol\right)\)
Vậy: R là Al.

a)
Fe +2 HCl --> FeCl2+ H2
R + 2HCl --> RCl2 + H2
nhh = nH2= 0,672/22,3=0,03 mol
=> M trung bình =1,52/ 0,03= 50,6
Vì MFe=56> Mtb => R<50,6
nH2SO4= 49.8%/98= 0,04 mol
R + H2SO4 --> RSO4 +H2
axit dư => nR phản ứng = nH2SO4 phản ứng <0,04
=> R>1,52/0,04= 38
Suy ra 38< R< 50,6, R hóa trị II
Vậy R là Canxi (Ca) . R =40
b)
Có nFe +nCa= 0,03mol
m hh=56nFe +40nCa =1,52
=> n Fe = 0,02 mol ; n Ca = 0,01 mol
=> %mFe, %mCa
c)
nHCl = 2nH2 =0,06 mol
=> mddHCl =36,5.0,06.100/15=14,6g
mddB= m hhkl + m ddHCl - mH2 = 1,52+ 14,6 -0,03.2= 16,06 g
dd B có FeCl2 0,02 mol và CaCl2 0,01 mol
=> C%.
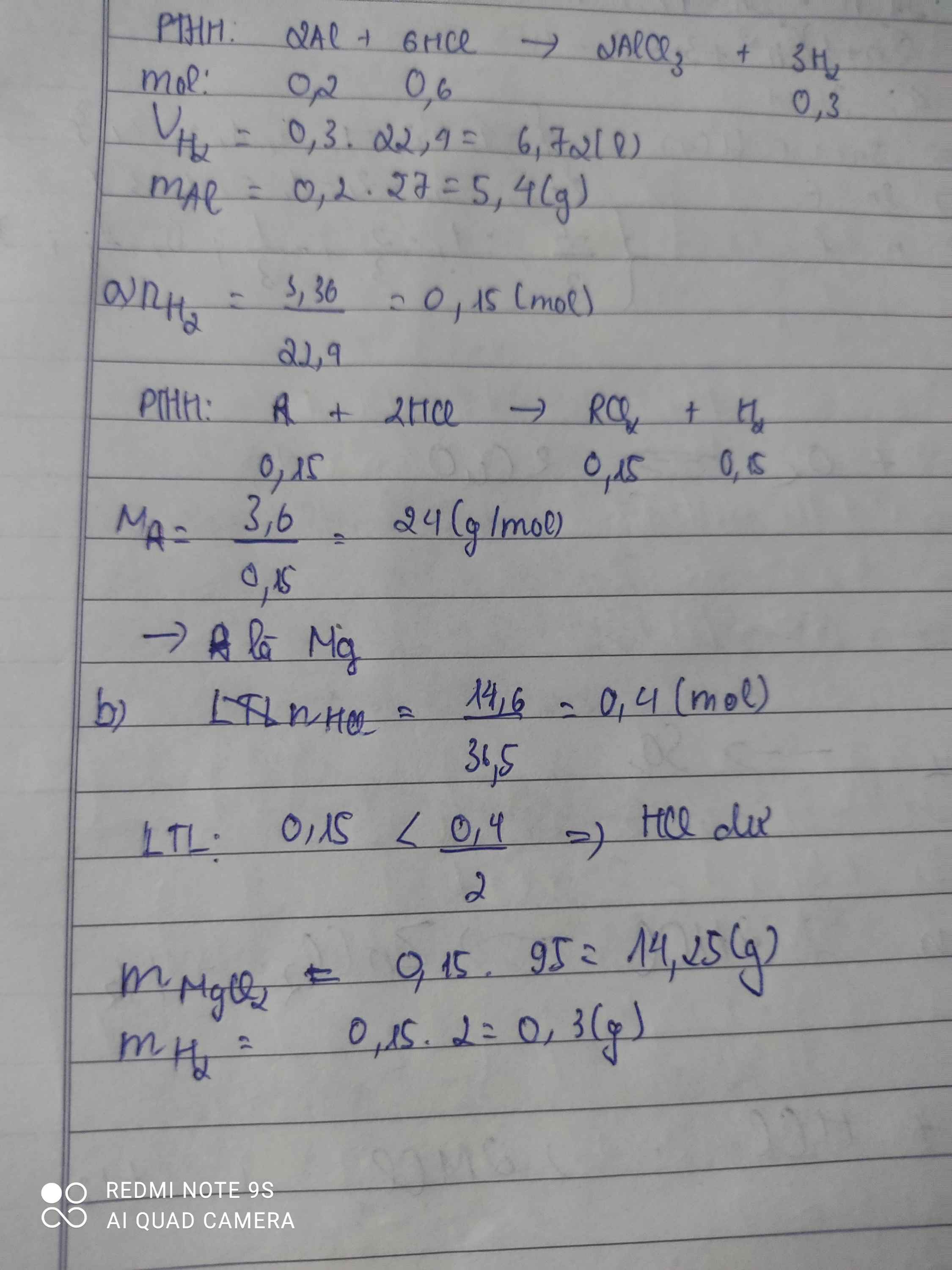
2) Gọi kim loại hóa trị II là x
X + 2H2O → X(OH)2 + H2
nH2 = 2,24:22,4 =0,1 mol
nX = \(\dfrac{4}{^MX}\)=nH2
=> \(\dfrac{4}{^MX}\)=0,1 => MX=40 => X là kim loại Canxi (Ca)
Bài 1:
a, Ta có: \(n_{P_2O_5}=\dfrac{14,2}{142}=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{45}{18}=2,5\left(mol\right)\)
PT: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{2,5}{3}\), ta được H2O dư.
Theo PT: \(n_{H_2O\left(pư\right)}=3n_{P_2O_5}=0,3\left(mol\right)\)
\(\Rightarrow n_{H_2O\left(dư\right)}=2,5-0,3=2,2\left(mol\right)\)
\(\Rightarrow m_{H_2O\left(dư\right)}=2,2.18=39,6\left(g\right)\)
b, Theo PT: \(n_{H_3PO_4}=2n_{P_2O_5}=0,2\left(mol\right)\)
\(\Rightarrow m_{H_3PO_4}=0,2.98=19,6\left(g\right)\)
Bạn tham khảo nhé!