1. Hỗn hợp khí A gồm khí N2, và khí H2 có tỉ khối đối với H2 là 7,5. Tính thành phần phần trăm theo khối lượng của mỗi khí có trong hỗn hợp khí A.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a.\)
\(GS:\)
\(n_{hh}=1\left(mol\right)\)
\(Đặt:n_{N_2}=a\left(mol\right),n_{CO_2}=b\left(mol\right)\)
\(\Rightarrow a+b=1\left(1\right)\)
\(m_A=28a+44b=18\cdot2=36\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(a=b=0.5\)
\(\%m_{N_2}=\dfrac{0.5\cdot28}{0.5\cdot28+0.5\cdot44}\cdot100\%=38.89\%\)
\(\%m_{CO_2}=61.11\%\)
\(b.\)
\(\dfrac{n_{N_2}}{n_{CO_2}}=\dfrac{0.5}{0.5}=\dfrac{1}{1}\)
\(n_{N_2}=n_{CO_2}=\dfrac{1}{2}\cdot n_A=\dfrac{0.2}{2}=0.1\left(mol\right)\)
\(Đặt:n_{CO_2}=x\left(mol\right)\)
\(\overline{M}=\dfrac{0.1\cdot28+0.1\cdot44+44x}{0.2+x}=20\cdot2=40\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow x=0.2\)
\(m_{CO_2\left(cầnthêm\right)}=0.2\cdot44=8.8\left(g\right)\)

Coi \(n_{khí} = 1(mol)\)
Gọi \(n_{H_2} = a(mol) ; n_{N_2} = b(mol)\)
Ta có :
a + b = 1
2a + 28b = 1.21,5
Suy ra a = 0,25 ; b = 0,75
Vậy :
\(\%V_{H_2} = \dfrac{0,25}{1}.100\% = 25\%\\ \%V_{N_2} = 100\% - 25\% = 75\%\)

Đặt x và y là số mol O 3 và O 2 có trong 1 mol hỗn hợp khí
Hỗn hợp khí A : (48x + 32y)/(x+y) = 19,2 x 2 = 38,4
→ 3x = 2y → 40% O 3 và 60% O 2
Đặt x và y là số mol H 2 và CO có trong 1 mol hỗn hợp khí
Hỗn hợp khí B : (2x + 28y)/(x+y) = 3,6 x 2 = 7,2
→ x = 4y → 80% H 2 và 20% CO

Gọi \(n_{H_2} = a(mol) ; n_{N_2} = b(mol)\)
Coi \(n_{hỗn\ hợp} = 1(mol)\)
Ta có :
\(n_{hỗn\ hợp} = a + b = 1(mol)\\ m_{hỗn\ hợp} = 2a + 28b = 21,5.1 = 21,5(gam)\\ \Rightarrow a = 0,25 ; b = 0,75\)
Vậy :
\(\%V_{H_2} = \dfrac{0,25}{1}.100\% = 25\%\\ \%V_{N_2} = 100\% - 25\% = 75\%\)

a) \(n_{N_2}+n_{CO_2}=\dfrac{15,68}{22,4}=0,7\left(mol\right)\)
Có: \(28.n_{N_2}+44.n_{CO_2}=24,4\)
=> \(\left\{{}\begin{matrix}n_{N_2}=0,4\left(mol\right)\\n_{CO_2}=0,3\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{N_2}=\dfrac{0,4}{0,7}.100\%=57,143\%\\\%V_{CO_2}=\dfrac{0,3}{0,7}.100\%=42,857\%\end{matrix}\right.\)
b) \(\left\{{}\begin{matrix}m_{N_2}=0,4.28=11,2\left(g\right)\\m_{CO_2}=0,3.44=13,2\left(g\right)\end{matrix}\right.\)

Đáp án B
Chọn thể tích ban đầu của N2 là 1 lít, H2 là 3 lít
→ Thể tích ban đầu là 4 lít
→Thể tích khí giảm là Vkhí giảm= 1/10.Vban đầu= 1/10.4= 0,4 lít
→VNH3 sinh ra= Vban đầu- Vsau= Vkhí giảm= 0,4 lít
N2+ 3H2![]() 2NH3
2NH3
VN2 pứ= 1/2VNH3 sỉnh = 0,2 lít,
VH2 pứ= 3/2.VNH3sinh= 0,6 lít
→VN2 dư= 0,8 lít, VH2 dư= 3-0,6= 2,4 lít
Tổng thể tích khí sau phản ứng là:
Vsau=9/10.Vban đầu= 0,9.4= 3,6 lít
→%VN2 dư= 0,8.100%/3,6=22,22%;
%VH2 dư= 2,4.100%/3,6=66,67%
%VNH3=11,11%

a) Gọi số mol N2, H2 là a, b (mol)
Có: \(\overline{M}_A=\dfrac{28a+2b}{a+b}=7,5.2=15\left(g/mol\right)\)
=> 13a = 13b
=> a = b
=> \(\left\{{}\begin{matrix}\%m_{N_2}=\dfrac{28a}{28a+2b}.100\%=93,33\%\\\%m_{H_2}=\dfrac{2b}{28a+2b}.100\%=6,67\%\end{matrix}\right.\)
b) Giả sử A chứa 1 mol N2, 1 mol H2
PTHH: N2 + 3H2 --to,p,xt--> 2NH3
Xét tỉ lệ: \(\dfrac{1}{1}>\dfrac{1}{3}\) => Hiệu suất tính theo H2
Gọi số mol H2 phản ứng là 3a
PTHH: N2 + 3H2 --to,p,xt--> 2NH3
Trc pư: 1 1 0
Pư: a<--3a--------------->2a
Sau pư: (1-a) (1-3a) 2a
=> \(\overline{M}_B=\dfrac{\left(1-a\right).28+\left(1-3a\right).2+17.2a}{\left(1-a\right)+\left(1-3a\right)+2a}=9,375.2=18,75\left(g/mol\right)\)
=> a = 0,2
=> \(H\%=\dfrac{0,2.3}{1}.100\%=60\%\)

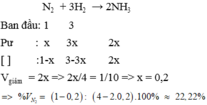
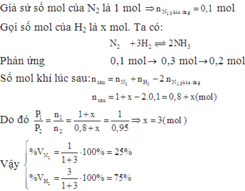
Ta có: dA/H2 = 7,5 ⇒ MA = 7,5.2 = 15 (g/mol)
\(\Rightarrow\dfrac{28n_{N_2}+2n_{H_2}}{n_{N_2}+n_{H_2}}=15\)
\(\Rightarrow n_{N_2}=n_{H_2}\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{N_2}=\dfrac{28n_{N_2}}{28n_{N_2}+2n_{H_2}}.100\%=\dfrac{28n_{N_2}}{28n_{N_2}+2n_{N_2}}.100\%\approx93,3\%\\\%m_{H_2}\approx6,7\%\end{matrix}\right.\)