Nhúng M vào 1lit dd FeSO4 x M , khối lượng tăng 16g. Nếu cũg nhúng kl trên vào 1 lít dd CuSO4 x M thấy Kl tăng 20g. Xác định M?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 1:
2M+nCuSO4\(\rightarrow\)M2(SO4)n+nCu
2M+nFeSO4\(\rightarrow\)M2(SO4)n+nFe
- Gọi a là số mol của M
- Độ tăng khối lượng PTHH1:
64na/2-Ma=20 hay(32n-M).a=20
- Độ tăng khối lượng PTHH2:
56.na/2-Ma=16 hay (28n-M)a=16
Lập tỉ số ta được:\(\dfrac{32n-M}{28n-M}=\dfrac{20}{16}=1,25\)
32n-M=35n-1,25M hay 0,25M=3n hay M=12n
n=1\(\rightarrow\)M=12(loại)
n=2\(\rightarrow\)M=24(Mg)
n=3\(\rightarrow\)M=36(loại)
Câu 2:Gọi A là khối lượng thanh R ban đầu.
R+Cu(NO3)2\(\rightarrow\)R(NO3)2+Cu
R+Pb(NO3)2\(\rightarrow\)R(NO3)2+Pb
- Gọi số mol Cu(NO3)2 và Pb(NO3)2 là x mol
- Độ giảm thanh 1: \(\dfrac{\left(R-64\right)x}{A}.100=0,2\)
- Độ tăng thanh 2: \(\dfrac{\left(207-R\right)x}{A}.100=28,4\)
Lập tỉ số: \(\dfrac{207-R}{R-64}=\dfrac{28,4}{0,2}=142\)
207-R=142R-9088 hay 143R=9295 suy ra R=65(Zn)

n C u S O 4 (bđ) = 0,5.1 = 0,5 mol
n C u S O 4 (sau pư) = 0,3.1 = 0,3 mol
⇒ n C u S O 4 (pư) = 0,5-0,3 = 0,2 mol
M + CuSO4 → MSO4 + Cu
⇒ n C u S O 4 ( p ư ) = n M = n M S O 4 = n C u = 0 , 2 m o l
m K L ( s a u ) = m K L ( b đ ) - m M + m C u
⇒ m K L ( s a u ) - m K L ( b đ ) = m C u - m M
⇒ 1 , 6 = 0 , 2 . 64 - 0 , 2 . M M
⇒ M M = 56
Vậy M là Fe.
⇒ Chọn B.

a)
$n_{AgNO_3\ pư} = 1.(0,5 - 0,3) = 0,2(mol)$
M + 2AgNO3 → M(NO3)2 + 2Ag
0,1.......0,2............................0,2.......(mol)
Suy ra : $0,2.108 - 0,1M = 19,2 \Rightarrow M = 24(Mg)$
Vậy M là kim loại Magie

![]()
Vì hai thanh kim loại M như nhau, nồng độ của hai dung dịch ban đầu bằng nhau và hóa trị của sắt và đồng trong dung dịch muối là II nên lượng kim loại M phản ứng ở hai dung dịch là bằng nhau.
Khối lượng các thanh kim loại tăng sau phản ứng là do M có khối lượng mol nhỏ hơn Fe và Cu.
Cứ 1 mol M phản úng tạo 1 mol Fe thì khối lượng kim loại tăng (56-M) gam.
Cứ 1 mol M phản ứng tạo 1 mol Cu thì khối lượng kim loại tăng (64-M) gam.
Gọi a là số mol M phản ứng.
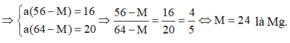
Đáp án A

Đáp án A.
M + Cu2+ → M2+ + Cu
Số mol Cu2+ phản ứng là: 1(0,5 – 0,3) = 0,2 mol
Độ tăng khối lượng của thanh kim loaị M:
M = mCu – mM tan
= 0,2(64 – M) = 1,6
Suy ra: M = 56 là Fe

Bài 2: a)gọi nKl bám( cả 2 PTHH) là a(mol)
PTHH: M + CuSO4-> MSO4+ Cu
a <- a (mol)
mKl giảm= Ma-64a
M + 2AgNO3-> M(NO3)2+2 Ag
a/2 a (mol)
mKl tăng= 108a-Ma/2
Theo đề bài ta có: 75,5(Ma-64a)= 108a-Ma/2
=> M = 65( Zn)
b)PTHH: Zn + CuSO4-> ZnSO4+ Cu(1)
đề: 0,3 0,1 (mol)
Zn + 2AgNO3-> Zn(NO3)2+2Ag(2)
0,05 0,1 (mol)
Ta có: nZn\(\approx\)0,3(mol)
nCuSO4=0,125.0,1(mol)
theo PTHH(1) ta thấy nZn>nCuSO4=> CuSO4 hết
nCu=nCuSO4
=> nCu=0,1(mol)
=> nAg=0,1(mol)
Theo PTHH(2) mKl tăng= 0,1.108-0,05.65=7,55(g)
%mKl tăng: \(\dfrac{7,55}{20}.100\%=37,75\%\)
gọi x,y,z la so mol cua Fe3O4 , MgO, CuO
MgO + H2 (ko pu)
Fe3O4 + 4H2 ---> 3Fe + 4H2O
x-------- 4x ------- 3x ----- 4x
CuO + H2 ---> Cu + H2O
z ------ z ------- z ---- z
theo de ta co: 232x + 40y + 80z = 26,5
56x + 64z + 40y = 20,8
Fe3O4 + 8HCl--->FeCl2 + 2FeCl3+ 4H2O
x ---------- 8x ----- x -------- 2x ------ 4x
MgO + 2HCl ----> MgCl2 + H2O
y -------- 2y -------- y ------- y
CuO + 2HCl ----> CuCl2 + H2O
z ------- 2z --------- z ------- z
\(n_{HCl}=0,225.2=0,45\left(mol\right)\)

Ta có: nFeSO4 = nCuSO4 = x (mol)
- Khi nhúng M vào FeSO4:
\(2M+nFeSO_4\rightarrow M_2\left(SO_4\right)_n+nFe\)
2x/n_______x_________________x (mol)
⇒ m tăng = mFe - mM = 56x - 2x.MM/n = 16 (1)
- Khi nhúng vào CuSO4:
\(2M+nCuSO_4\rightarrow M_2\left(SO_4\right)_n+nCu\)
2x/n________x_________________x (mol)
⇒ m tăng = mCu - mM = 64x - 2x.MM/n = 20 (2)
Từ (1) và (2) ⇒ x = 0,5 (mol)
⇒ MM = 12n
Với n = 2 thì MM = 24 (g/mol)
→ M là Mg.