Hấp thu hoàn toàn 7,84 lít khí SO 2 (đktc) vào 300 ml dung dịch NaOH 2M. Khối
lượng muối thu được sau phản ứng là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
n C O 2 = 0,35 mol; n B a ( O H ) 2 = 0,15 mol;
nKOH= 0,15 mol → n O H - = 0,45 mol
→ T = n O H - n C O 2 = 0 , 45 0 , 35 = 1 , 29
→ Tạo 2 loại muối : HCO3- và CO32-
CO2 + OH- → HCO3-
x x x mol
CO2 + 2OH- → CO32- + H2O
y 2y y mol
Có n C O 2 = x+ y = 0,35;
n O H - = x+ 2y = 0,45 suy ra x = 0,25; y = 0,1
Ba2+ + CO32- → BaCO3↓
0,15 0,1 mol 0,1 mol
m B a C O 3 = 0,1. 197 = 19,7 (gam)
m C O 2 = 0,35.44 =15,4 gam
Do m C O 2 < m B a C O 3 nên khối lượng dung dịch giảm một lượng là:
∆mgiảm= m B a C O 3 - m C O 2 = 19,7- 15,4 = 4,3 gam

Bài 7:
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\n_{NaOH}=0,2\cdot1=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Tạo 2 muối
PTHH: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
a_______2a__________a (mol)
\(CO_2+NaOH\rightarrow NaHCO_3\)
b_______b__________b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}a+b=0,15\\2a+b=0,2\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,05\\b=0,1\end{matrix}\right.\)
Mặt khác: \(m_{dd}=m_{CO_2}+m_{ddNaOH}=0,15\cdot44+200\cdot1,25=256,6\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{Na_2CO_3}=\dfrac{0,05\cdot106}{256,6}\cdot100\%\approx2,1\%\\C\%_{NaHCO_3}=\dfrac{0,1\cdot72}{256,6}\cdot100\%\approx2,8\%\end{matrix}\right.\)
Bài 8:
PTHH: \(RCO_3+2HNO_3\rightarrow R\left(NO_3\right)_2+CO_2\uparrow+H_2O\)
Giả sử \(n_{RCO_3}=1\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{HNO_3}=2\left(mol\right)\\n_{R\left(NO_3\right)_2}=1\left(mol\right)=n_{CO_2}\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{ddHNO_3}=\dfrac{2\cdot63}{20\%}=630\left(g\right)\\m_{R\left(NO_3\right)_2}=R+124\left(g\right)\\m_{CO_2}=44\left(g\right)\end{matrix}\right.\) \(\Rightarrow C\%_{R\left(NO_3\right)_2}=\dfrac{124+R}{R+60+630-44}=0,26582\)
\(\Leftrightarrow R=65\) (Kẽm) \(\Rightarrow\) CTHH của muối cacbonat là ZnCO3
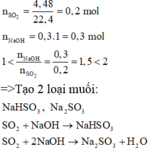

\(n_{SO_2}=\dfrac{7.84}{22.4}=0.35\left(mol\right)\)
\(n_{NaOH}=0.3\cdot2=0.6\left(mol\right)\)
\(\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{0.6}{0.35}=1.7\)
=> Tạo ra 2 muối
\(n_{Na_2SO_3}=a\left(mol\right),n_{NaHSO_3}=b\left(mol\right)\)
\(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
\(NaOH+SO_2\rightarrow NaHSO_3\)
\(BTNa:\) \(2a+b=0.6\)
\(BTS:a+b=0.35\)
\(a=0.25,b=0.1\)
\(m_M=0.25\cdot127+0.1\cdot104=42.4\left(g\right)\)
n NaOH = 0,3.2 = 0,6(mol)
n SO2 = 7,84/22,4 = 0,35(mol)
Ta có :
1 < n NaOH / n SO2 = 0,6/0,35 = 1,7 < 2 nên phản ứng sinh ra : Na2SO3(a mol) , NaHSO3(b mol)
Bảo toàn nguyên tố Na,S :
n NaOH = 2a + b = 0,6(mol)
n SO2 = a + b = 0,35(mol)
=> a = 0,25 ; b = 0,1
=> m muối = 0,25.126 + 0,1.104 = 41,9 gam