Hãy dựa vào khối lượng riêng ở cùng điều kiện nhiệt độ và áp suất của cùng một chất ở các thể khác nhau để chứng tỏ khoảng cách giữa các phân tử ở thể khí rất lớn so với ở thể lỏng và thể rắn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a,M_A=29.2,07\approx 60(g/mol)\\ b,n_X=n_{O_2}=\dfrac{1,76}{32}=0,055(mol)\\ \Rightarrow M_X=\dfrac{3,3}{0,055}=60(g/mol)\)

a, tính số mol rồi lấy số mol.6.1023
b, V=n.22,4
c d\(\frac{A}{B}\) = \(\frac{M_A}{M_B}\)
-Lấy số mol nhân cho 6.1023
-Lấy số mol nhân cho 22,4(ở đktc)
-\(d_{A/B}=\dfrac{M_A}{M_B}\)
Chúc bạn học tốt![]()

Đáp án : A
Gọi công thức phân tử của ankan X là CnH2n+2
Trong cùng điều kiện về nhiệt độ và áp suất thì tỉ lệ về thể tích cũng chính là tỉ lệ về số mol

=> mY = 24.nY = 24.3 = 72
Áp dụng định luật bảo toàn khối lượng ta có: mX = mY = 72
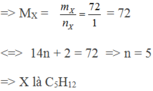

Đáp án D
Gọi công thức phân tử của ankan X là CnH2n+2.
Trong cùng điều kiện về nhiệt độ và áp suất thì tỉ lệ về thể tích cũng chính là tỉ lệ về số mol => 1 mol X → c r a c k i n g 3 mol Y.
Ta có: MY = 12.2 = 24 <=> m Y n Y = 24
=> mY = 24.nY = 24.3 = 72
Áp dụng định luật bảo toàn khối lượng ta có: mX = mY = 72
=> MX = m X n X = 72 1 = 72 ⇔ 14n + 2 = 72 => n = 5 => X là C5H12.

Giả sử ban đầu có V ankan
Đốt V ankan -> 3V hỗn hợp khí
=>số mol tăng 3 lần
Mà M hỗn hợp sau la 12*2=24 nên theo DLBTKL có m(trước)=m(sau)
=> M(trước)=3M(sau)
=> M(trước)=3*24=72
=> Ankan C5H12
=> Đáp án B
Khối lượng riêng của cùng một chất ở thể khí nhỏ hơn nhiều so với ở thể lỏng và thể rắn vì:
- Khối lượng riêng nhỏ chứng tỏ khoảng cách giữa các phân tử ở thể khí lớn hơn nhiều so với ở thể lỏng và thể rắn.
+ Ở thể khí, các phân tử có nhiều khoảng trống giữa chúng.
+ Ở thể lỏng, các phân tử xếp sát nhau hơn.
+ Ở thể rắn, các phân tử liên kết chặt chẽ với nhau.