Bài 11: Đốt cháy hoàn toàn 100ml hơi chất (A) cần 250ml Oxy tạo ra 200ml CO2 và 200ml hơi nước. Tìm CTPT của (A) biết rằng các thể tích đo trong cùng điều kiện nhiệt độ, áp suất? ĐS: C2H4O
Bài 12: Trộn 10ml Hydrocacbon A với 60ml O2 (dư) rồi đốt. Sau phản ứng làm lạnh thu được 40ml hỗn hợp khí, tiếp tục cho hỗn hợp khí qua nước vôi trong dư thì còn 10ml khí. Tìm CTPT của A ? Biết rằng tất cả các thể tích đo trong cùng điều kiện nhiệt độ, áp suất. ĐS: C8H12
Bài 13: Đốt 200cm3 hơi một chất hữu cơ chứa C; H; O trong 900cm3 O2 (dư). Thể tích sau phản ứng là 1,3 lít sau đó cho nước ngưng tụ còn 700cm3 và sau khi cho qua dung dịch KOH còn 100cm3. Xác định CTPT của chất hữu cơ? Biết rằng các khí đo trong cùng điều kiện nhiệt độ, áp suất. ĐS: C3H6O
Bài 14: Chất hữu cơ X ở thể khí, khi đốt 1 lít khí X cần đúng 5 lít khí oxi. Sau pư thu được 3 lít khí CO2 và 4 lít hơi nước. Xác định CTPT của A. biết thể tích các khí đo ở cùng điều kiện nhiệt độ và áp suất. ĐS:C3H8
Bài 15: Đốt cháy hoàn toàn 0,01 mol hợp chất hữu cơ X bằng 0,616 lít O2 (vừa đủ) thu được 1,344 lít hỗn hợp gồm CO2, N2 và hơi nước. Sau khi ngưng tụ hơi nước, hỗn hợp còn lại có thể tích là 0,56 lít và có tỉ khối so với hidro bằng 20,4. Thể tích các khí đo ở đktc. Xác định CTPT của X. ĐS: C2H7N
Bài 16: Đốt cháy hoàn toàn 0,1 mol hợp chất hữu cơ (D) cần vừa đủ 14,4 gam oxi, thấy sinh ra 13,2 gam CO2 và 7,2 gam nước.
a. Tìm phân tử khối cuả (D).
b. Xác định công thức phân tử của (D). ĐS: 60, C3H8O
Bài 17: Đốt cháy hoàn toàn 112 cm3 một hydrocacbon (A) là chất khí ở (đktc) rồi dẫn sản phẩm lần lượt qua bình (I) đựng H2SO4 đậm đặc và bình (II) chứa KOH dư người ta thấy khối lượng bình (I) tăng 0,18 gam và khối lượng bình (II) tăng 0,44 gam.Xác định CTPT (A). ĐS: C2H2

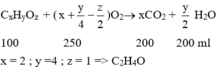
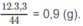
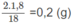
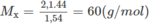
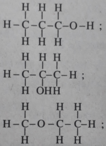
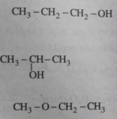
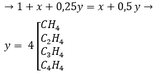
\(B16:\\ ĐLBTKL:m_D+m_{O_2}=m_{CO_2}+m_{H_2O}\\ \Leftrightarrow m_D+14,4=13,2+7,2\\ \Rightarrow m_D=6\left(g\right)\\ a,\Rightarrow M_D=\dfrac{6}{0,1}=60\left(\dfrac{g}{mol}\right)\\ b,n_C=n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right);n_H=2.n_{H_2O}=2.\dfrac{7,2}{18}=0,8\left(mol\right)\\ m_D=m_C+m_H+m_O=6\left(g\right)\\ \Leftrightarrow0,3.12+0,8.1+m_O=6\\ \Rightarrow m_O=1,6\left(g\right)\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\\ Đăt.CTTQ.D:C_aH_bO_c\left(a,b,c:nguyên,dương\right)\\ \Rightarrow a:b:c=n_C:n_H:n_O=0,3:0,8:0,1=3:8:1\Rightarrow a=3;b=8;c=1\\ Có:M_{C_3H_8O}=3.12+8.1+16.1=60\left(\dfrac{g}{mol}\right)\left(TM\right)\\ b,\Rightarrow D:C_3H_8O\)