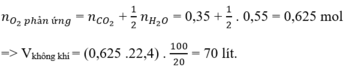Thể tích không khí (đktc) cần dùng để đốt cháy hoàn toàn 0,1 mol benzen là (biết trong không khí O2 chiếm 20% thể tích) :
A. 83 lít.
B. 82 lít.
C. 74 lít.
D. 84 lít.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$n_C = \dfrac{420}{12} = 35(mol)$
$C + O_2 \xrightarrow{t^o} CO_2$
$n_{CO_2} = n_{C\ pư} = 35.90\% = 31,5(mol)$
$V_{CO_2} = 31,5.22,4 = 705,6(lít)$
Đáp án B
Ta có: \(n_C=\dfrac{420}{12}=35\left(mol\right)\)
PT: \(C+O_2\underrightarrow{t^o}CO_2\)
___35_______35 (mol)
\(\Rightarrow V_{CO_2\left(LT\right)}=35.22,4=784\left(l\right)\)
Mà: H% = 90%
\(\Rightarrow V_{CO_2\left(TT\right)}=784.90\%=705,6\left(l\right)\)
→ Đáp án: B
Bạn tham khảo nhé!

nCH4 = 4,48/22,4 = 0,2 (mol)
PTHH: CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: 0,2 ---> 0,4
Vkk = 0,4 . 22,4 : 21% = 128/3 (l)

\(n_{CH_4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Theo PT: \(n_{O_2}=2n_{CH_4}=0,2\left(mol\right)\Rightarrow V_{O_2}=0,2.22,4=4,48\left(l\right)\)
\(\Rightarrow V_{kk}=\dfrac{V_{O_2}}{20\%}=22,4\left(l\right)\)

a) \(n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,5--->1
=> VO2 = 1.22,4 = 22,4 (l)
b) Vkk = 22,4.5 = 112 (l)

Đáp án A
Hỗn hợp khí gồm CH4, C2H6 và C3H8 là các hidrocacbon.
Mà khi đốt cháy 1 hidrocacbon bất kì ta luôn có: