Hòa tan một lượng Na dư vào 25 gam dung dịch H2SO4 9,8%. Tính thể tích H2 (đktc) thoát ra (coi hiệu suất các phản ứng đạt 100%)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


2Al+3H2SO4->Al2(SO4)3+3H2(khí)
mH2SO4=100*9.8:100=9.8(g)
nH2SO4=0.1(mol)
theo pthh:nAl=2/3 nH2SO4->nAl=2/3*0.1=0.07(mol)
mAl=0.07*27=1.89(g)
theo pthh:nH2=nH2SO4->nH2=0.1(mol)
VH2=0.1*22.4=2.24(l)
Theo pthh:nAl2(SO4)3=1/3 nH2SO4->nAl2(SO4)3=0.03(mol)
m muối=0.03*342=10.26(g)
mdd=1.89+100-0.1*2=101.69(g)
C% muối:10.26:101.69*100=10.09%

HD:
Thí nghiệm 1 chỉ có Na phản ứng:
Na + HOH \(\rightarrow\) NaOH + 1/2H2 (1)
0,4 0,2 mol
Thí nghiệm 2 chỉ có Al phản ứng (kim loại lưỡng tính):
Al + OH- + H2O \(\rightarrow\) AlO2- + 3/2H2 (2)
0,7/3 0,35 mol
Thí nghiệm 3 cả 3 chất đều phản ứng:
2Na + H2SO4 \(\rightarrow\) Na2SO4 + H2 (3)
Mg + H2SO4 \(\rightarrow\) MgSO4 + H2 (4)
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 (5)
Gọi x, y, z tương ứng là số mol của Na, Mg và Al trong a gam hh.
Ta có: x = 0,4 mol; z = 0,7/3 mol; x/2 + y + 3z/2 = 0,5. Suy ra: y = -0.5 < 0 (vô lí)
Bạn xem lại đề bài, đề bài ko đúng.

a) \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + H2SO4 ---> ZnSO4 + H2
0,1--->0,1------->0,1------>0,1
=> \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b) \(m_{\text{dd}H_2SO_4}=\dfrac{0,1.98}{19,6\%}=50\left(g\right)\)
=> \(m_{\text{dd}.sau.p\text{ư}}=50+6,5-0,1.2=56,3\left(g\right)\)
=> \(C\%_{ZnSO_4}=\dfrac{0,1.161}{56,3}.100\%=28,6\%\)

Đáp án : C
Bảo toàn e : 3nAl = 2 n H 2
=> n H 2 = 0,45 mol
=> V H 2 = 10,08 lit

\(CaCO_3+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Ca+CO_2+H_2O\\ a,n_{CH_3COOH}=0,2.1=0,2\left(mol\right)\Rightarrow n_{CO_2}=\dfrac{0,2}{2}=0,1\left(mol\right)\Rightarrow V_{CO_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\\ b,CH_3COOH+C_2H_5OH⇌\left(H^+,t^o\right)CH_3COOC_2H_5+H_2O\\ n_{CH_3COOH}=\dfrac{50}{200}.0,2=0,05\left(mol\right)\\ n_{C_2H_5OH}=\dfrac{23}{46}=0,5\left(mol\right)\\ Vì:\dfrac{0,5}{1}>\dfrac{0,05}{1}\Rightarrow Rượu.dư\\ \Rightarrow n_{este\left(LT\right)}=n_{axit}=0,05\left(mol\right)\\ \Rightarrow n_{este\left(TT\right)}=80\%.0,05=0,04\left(mol\right)\\ m_{CH_3COOC_2H_5}=88.0,04=3,52\left(g\right)\)
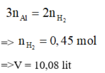
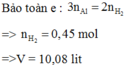
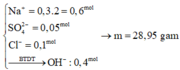

\(n_{H_2SO_4}=\dfrac{25\cdot9.8\%}{98}=0.0025\left(mol\right)\)
\(2Na+H_2SO_4\rightarrow Na_2SO_4+H_2\)
\(n_{H_2}=n_{H_2SO_4}=0.0025\left(mol\right)\)
\(V_{H_2}=0.0025\cdot22.4=0.056\left(l\right)\)