hòa tan hỗn hợp A gồm 16,8 g Mg và 28 g Fe vào 1850 ml dung dịch HNO3 2m vừa đủ Sau phản ứng thu được 11,2 lít hỗn hợp khí X gồm N2O NO2 N2 và dung dịch Y chứa m gam muối.tính % thể tích của N2 trong hh X và giá trị của m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(n_{N_2O}+n_{NO_2}+n_{N_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\left(1\right)\)
BT e, có: 2nMg + 3nFe = 8nN2O + nNO2 + 10nN2
⇒ 8nN2O + nNO2 + 10nN2 = 1,9 (2)
Có: nHNO3 = 10nN2O + 2nNO2 + 12nN2 = 2,4.1 = 2,4 (mol) (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}n_{N_2O}=0,1\left(mol\right)\\n_{NO_2}=0,1\left(mol\right)\\n_{N_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%V_{N_2}=\dfrac{0,1.22,4}{6,72.}100\%\approx33,33\%\)
\(n_{N_2O}=a\left(mol\right)\)
\(n_{NO_2}=b\left(mol\right)\)
\(n_{N_2}=c\left(mol\right)\)
\(\Rightarrow n_X=a+b+c=\dfrac{6.72}{22.4}=0.3\left(mol\right)\left(1\right)\)
Bảo toàn e :
\(8a+b+10c=0.65\cdot2+0.2\cdot3=1.9\left(2\right)\)
\(n_{H^+}=10a+2b+12c=2.4\left(mol\right)\left(3\right)\)
\(\left(1\right),\left(2\right),\left(3\right):a=b=c=0.1\left(mol\right)\)
\(\%V_{N_2}=\dfrac{0.1}{0.3}\cdot100\%=33.33\%\)

Ta có: nN2 = 0,22 (mol)
⇒ nNO3- = 10nN2 = 2,2 (mol)
⇒ m muối = mX + mNO3- = 31 + 2,2.62 = 167,4 (g)
nHNO3 = 12nN2 = 2,64 (mol)
\(\Rightarrow V_{HNO_3}=\dfrac{2,64}{2}=1,32\left(l\right)=1320\left(ml\right)\)

\(n_{HNO_3}=1.2\left(mol\right)\)
\(n_{NO}=a\left(mol\right)\)
\(n_{NO_2}=b\left(mol\right)\)
\(n_{N_2}=c\left(mol\right)\)
\(\Rightarrow a+b+c=\dfrac{5.6}{22.4}=0.25\left(1\right)\)
Bảo toàn e :
\(3\cdot0.2+1\cdot0.3=3a+b+10c\left(2\right)\)
\(n_{H^+}=4n_{NO}+2n_{NO_2}+12n_{N_2}\)
\(\Rightarrow4a+2b+12c=1.2\left(3\right)\)
\(\left(1\right),\left(2\right),\left(3\right):a=b=0.1,c=0.05\)
\(\%V_{NO_2}=\dfrac{0.1}{0.25}\cdot100\%=40\%\%0-\)

Đáp án : D
Ta có : nFe : nCu : nAl : nMg =1 : 1 : 2 : 2
=> nFe = nCu = 0,1 ; nAl = nMg = 0,2 mol
4 khí trong đó N2 và NO2 có số mol bằng nhau
=> có thể qui về N2O và NO với số mol lần lượt là x và y
n N O 3 m u ố i K L = ne KL = 3nFe + 2nCu + 3nAl + 2nMg = 1,5 mol
=> mmuối = mKL + m N O 3 m u ố i K L + m N H 4 N O 3
=> n N H 4 N O 3 = 0,025 mol
Bảo toàn N :
2 n N 2 O + n N O + 2 n N H 4 N O 3 + n N O 3 m u ố i K L = n H N O 3
=> 2x + y = 0,35 mol
Bảo toàn e :
2 n N 2 O + n N O + 2 n N H 4 N O 3 + n N O 3 m u ố i K L = n H N O 3
=> 8x + 3y = 1,3
=> x = 0,125 ; y = 0,1 mol
=> V = 5,04 lit

Chọn đáp án C
nH2O = nNO2 ⇒ ghép khí: N2O + NO2 = N2O3 = 3NO ⇒ quy A về N2 và NO.
Đặt nN2 = x mol; nNO = y mol ⇒ x + y = 0,1 mol và mhh khí = 28x + 30y = 0,1 × 14,5 × 2
⇒ giải ra: x = y = 0,05 mol. Hai kim loại Mg, Zn → chú ý có muối amoni!
Ta có: nHNO3 = 10nNH4+ + 12nN2 + 4nNO ⇒ nNH4+ = 0,04 mol.
Gọi số mol Mg là a và Zn là b ⇒ 24a + 65b = 19,225;
Lại theo bảo toàn electron: 2a + 2b = 0,04 × 8 + 0,05 × 10 + 0,05 × 3
||⇒ giải ra: a = 0,3 mol; b = 0,185 mol ⇒ %mMg = 0,3 × 24 ÷ 19,225 × 100% = 37,45%

Đáp án C
nH2O = nNO2 => ghép khí: N2O + NO2 = N2O3 = 3NO => quy A về N2 và NO.
Đặt nN2 = x mol; nNO = y mol ⇒ x + y = 0,1 mol và mhh khí = 28x + 30y = 0,1 × 14,5 × 2
=> giải ra: x = y = 0,05 mol. Hai kim loại Mg, Zn → chú ý có muối amoni!
Ta có: nHNO3 = 10nNH4+ + 12nN2 + 4nNO => nNH4+ = 0,04 mol.
Gọi số mol Mg là a và Zn là b => 24a + 65b = 19,225;
Lại theo bảo toàn electron: 2a + 2b = 0,04 . 8 + 0,05 . 10 + 0,05 . 3
=> giải ra: a = 0,3 mol; b = 0,185 mol => %mMg = [(0,3 . 24 ): 19,225] . 100% = 37,45%

Đáp án C
nH2O = nNO2 => ghép khí: N2O + NO2 = N2O3 = 3NO => quy A về N2 và NO.
Đặt nN2 = x mol; nNO = y mol ⇒ x + y = 0,1 mol và mhh khí = 28x + 30y = 0,1 × 14,5 × 2
=> giải ra: x = y = 0,05 mol. Hai kim loại Mg, Zn → chú ý có muối amoni!
Ta có: nHNO3 = 10nNH4+ + 12nN2 + 4nNO => nNH4+ = 0,04 mol.
Gọi số mol Mg là a và Zn là b => 24a + 65b = 19,225;
Lại theo bảo toàn electron: 2a + 2b = 0,04 . 8 + 0,05 . 10 + 0,05 . 3
=> giải ra: a = 0,3 mol; b = 0,185 mol => %mMg = [(0,3 . 24 ): 19,225] . 100% = 37,45%

Đáp án C
nH2O = nNO2 => ghép khí: N2O + NO2 = N2O3 = 3NO => quy A về N2 và NO.
Đặt nN2 = x mol; nNO = y mol ⇒ x + y = 0,1 mol và mhh khí = 28x + 30y = 0,1 × 14,5 × 2
=> giải ra: x = y = 0,05 mol. Hai kim loại Mg, Zn → chú ý có muối amoni!
Ta có: nHNO3 = 10nNH4+ + 12nN2 + 4nNO => nNH4+ = 0,04 mol.
Gọi số mol Mg là a và Zn là b => 24a + 65b = 19,225;
Lại theo bảo toàn electron: 2a + 2b = 0,04.8 + 0,05.10 + 0,05.3
=> giải ra: a = 0,3 mol; b = 0,185 mol => %mMg = [(0,3.24) : 19,225].100% = 37,45%

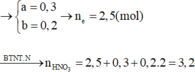
Ta có: \(n_{N_2O}+n_{NO_2}+n_{N_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\left(1\right)\)
\(n_{HNO_3}=1,85.2=3,7\left(mol\right)\)
⇒ 10nN2O + 2nNO2 + 12nN2 = 3,7 (2)
\(n_{Mg}=\dfrac{16,8}{24}=0,7\left(mol\right)\)
\(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\)
BT e, có: 8nN2O + nNO2 + 10nN2 = 2nMg + 3nFe = 2,9 (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}n_{N_2O}=0,15\left(mol\right)\\n_{NO_2}=0,2\left(mol\right)\\n_{N_2}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%V_{N_2}=\dfrac{0,15}{0,5}.100\%=30\%\)
m muối = mMg + mFe + 62.(8nN2O + nNO2 + 10nN2) = 224,6 (g)